子宫颈肿瘤包括良性肿瘤和恶性肿瘤。子宫颈癌是最常见的妇科恶性肿瘤,起源于子宫颈上皮内病变,两者病因相同,均为高危型HPV感染所致,在本章一并介绍。
子宫颈良性肿瘤以肌瘤为常见,在相应章节叙述,其余较为少见,不在本章范围。
可分为低级别和高级别病变,高级别病变为癌前病变。
发病与高危型IHPV持续感染密切相关,转化区是子宫颈状上皮内病变及子宫颈癌的好发部位。
组织学诊断是确诊和分級的依据。子宮颈锥切术是治疗高级别病变的主要手段。
疫苗接种和查是预防子宫颈癌的有效措施。
子宫颈鳞状上皮内病变(cervical squamous intraepithelial lesion,SIL),是与子宫颈浸润癌密切相关的一组子宫颈病变,常发生于25~35岁妇女。大部分低级别鳞状上皮内病变(low-grade squamous intraepithelial lesion,LSIL)可自然消退,但高级别鳞状上皮内病变(high- grade squamous intraepithelial lesion,HSIL)具有癌变潜能。SIL反映了子宫颈癌发生发展中的连续过程,通过筛查发现SIL,及时治疗高级别病变,是预防子宫颈浸润癌行之有效的措施。
高级别子宫颈腺上皮内瘤变(high-grade cervical glandular intraepithelial neoplasia,HG-CGIN)比较少见,本节仅介绍SIL。
【发病相关因素】
SIL和子宫颈癌与人乳头瘤病毒(human papilloma virus,HPV)感染、多个性伴侣、吸烟、性生活过早(<16岁)、性传播疾病、经济状况低下、口服避孕药和免疫抑制等因素相关。
1.HPV感染 目前已知HPV共有160多个型别,40余种与生殖道感染有关,其中13~15种与SIL和子宫颈癌发病密切相关。已在接近90%的SIL和99%的子宫颈癌组织发现有高危型HPV感染,其中约70%与HPV16和18型相关。高危型HPV产生病毒癌蛋白,其中E6和E7分别作用于宿主细胞的抑癌基因p53和Rb使之失活或降解,继而通过一系列分子事件导致癌变。接种HPV预防性疫苗可以实现子宫颈癌的一级预防。
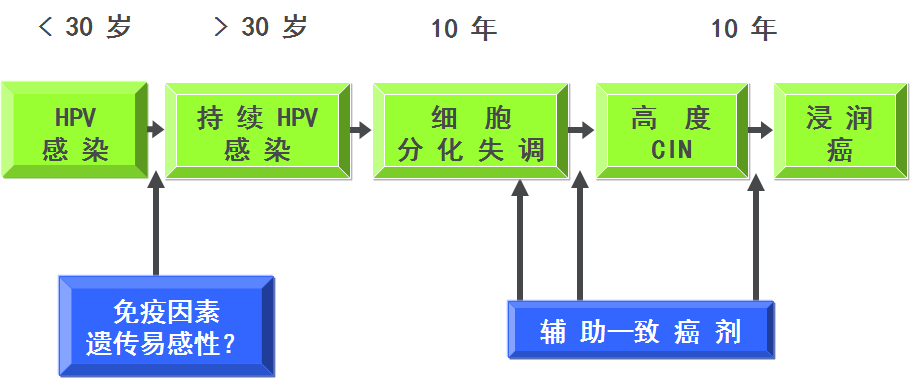
HPV感染致子宫颈癌机制示意图
2.性行为及分娩次数 多个性伴侣、初次性生活<16岁、早年分娩、多产与子宫颈癌发生有关。与有阴茎癌、前列腺癌或其性伴侣曾患子宫颈癌的高危男子性接触的妇女,也易虑子宫颈癌。
3.其他 吸烟可增加感染HPV效应,屏障避孕法有一定的保护作用。
【子宫颈组织学特点】
子宫颈上皮由子宫颈阴道部鳞状上皮和子宫颈管柱状上皮组成。
1.子宫颈阴道部鳞状上皮 由深至浅可分为基底带、中间带及浅表带3个带。基底带由基底细胞和旁基底细胞组成。基底细胞为储备细胞,无明显细胞增殖表现,在某些因素刺激下可以增生,也可以增生成为不典型鳞状细胞或分化为成熟状细胞。旁基底细胞为增生活跃的细胞,偶见核分裂象。中间带与浅表带为完全不增生的分化细胞,细胞渐趋死亡、脱落。
2.子宫颈管柱状上皮 柱状上皮为分化良好细胞,而柱状上皮下细胞为储备细胞,具有分化或增殖能力。
3.转化区(transformation zone) 也称为移行带,因其位于子宫颈鱗状上皮与柱状上皮交接部,又称为鳞-柱状交接部或鳞-柱交接。鳞0柱状交接部又分为原始鳞-柱状交接部和生理鳞-柱状交接部(图25-1)。
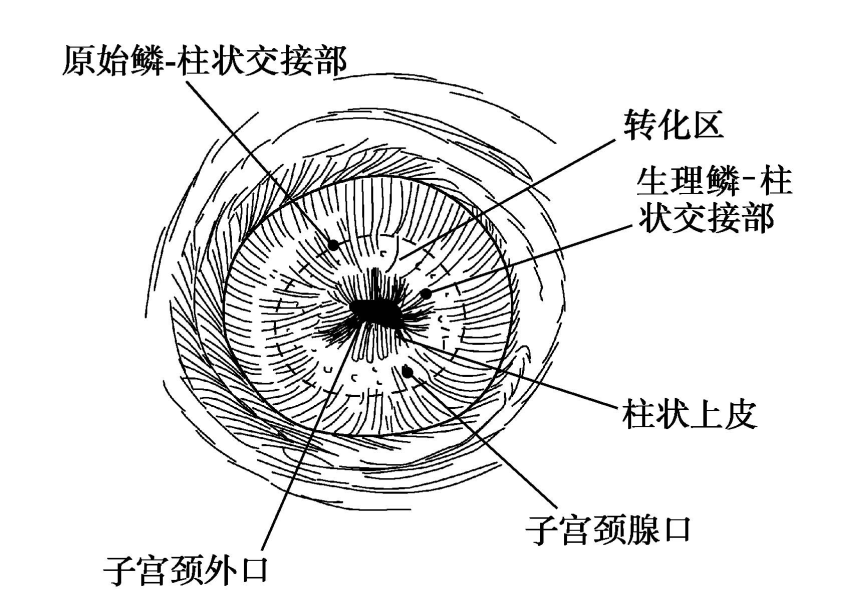
图25-1 子宫颈转化区
在胎儿期,来源于泌尿生殖窦的鳞状上皮向头侧生长,至子宫颈外口与子宫颈管柱状上皮相邻,形成原始鳞-柱状交接部。青春期后,在雌激素作用下,子宫颈发育增大,子宫颈管黏膜组织向尾侧移动,即子宫管柱状上皮及其下的间质成分到达子宫颈阴道部,使原始鳞-柱状交接部外移。原始鳞-柱状交接的内侧,由于覆盖的子宫颈管单层柱状上皮非薄,其下间质透出呈红色,外观呈细颗粒状的红色区,称为柱状上皮异位(columnar ectopy)。由于肉眼观似糜烂,过去称为“宫颈糜烂”,实际上并非真性糜烂;此后,在阴道酸性环境或致病菌作用下,外移的柱状上皮由原始鳞-柱状交接部的内侧向子宫颈口方向逐渐被鱗状上皮替代,形成新的鳞-柱状交接部,即生理鳞-柱状交接部。原始鳞-柱状交接部和生理鱗-柱状交接部之间的区域,称为转化区。在转化区形成过程中,新生的鳞状上皮覆盖子宫颈腺管口或伸人腺管,将腺管口堵塞,腺管周围的结缔组织增生或形成瘢痕压迫腺管,使腺管变窄或堵塞,腺体分泌物潴留于腺管内形成囊肿,称为子宫颈腺囊肿(Naboth cyst)。子宫颈腺囊肿可作为辦认转化区的一个标志。绝经后雌激素水平下降,子宫颈萎缩,原始鳞柱状交接部退回至子宫颈管内。转化区表面被覆的柱状上皮被鳞状上皮替代的机制有:①鳞状上皮化生(squamous metaplasia):暴露于子宫颈阴道部的柱状上皮受阴道酸性影响,柱状上皮下未分化储备细胞(reserve cell)开始增殖,并逐渐转化为鳞状上皮,继之柱状上皮脱落,被复层鳞状细胞所替代;②鳞状上皮化( squamous epithe-lization):子宫颈阴道部鳞状上皮直接长入柱状上皮与其基底膜之间,直至柱状上皮完全脱落而被鳞状上皮替代。
转化区成熟的化生鳞状上皮对致癌物的刺激相对不敏感,但未成熟的化生鳞状上皮却代谢活跃在人乳头瘤病毒等的作用下,发生细胞异常增生、分化不良、排列紊乱、细胞核异常、有丝分裂增加,最后形成SIL。
【病理学诊断和分级】
SIL既往称为“子宫颈上皮内瘤变"(cervical intraepithelial neoplasia,CIN),分为3级。WHO女性生殖器肿瘤分类(2014)建议采用与细胞学分类相同的二级分类法(即LSIL和HSIL),LSIL相当于CIN1,HSIL包括CIN3和大部分CIN2。CIN2可用p16免疫组化染色进行分流,p16染色阴性者按LSIL处理,阳性者按HSIL处理。二级分类法简便实用,提高了病理诊断的可重复性,较好地反映了HPV相关病变的生物学过程,能更好地指导临床处理及判断预后。
LSIL:鳞状上皮基底及副基底样细胞增生,细胞核极性轻度紊乱,有轻度异型性,核分裂象少,局限于上皮下1/3层,p16染色阴性或在上皮内散在点状阳性(图25-2)。
HSIL:细胞核极性素乱,核浆比例增加,核分裂象增多,异型细胞扩展到上皮下2/3层甚至全层,p16在上皮>2/3层面内呈弥漫连续阳性(图25-3)。
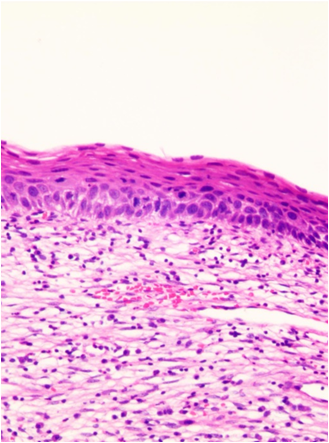
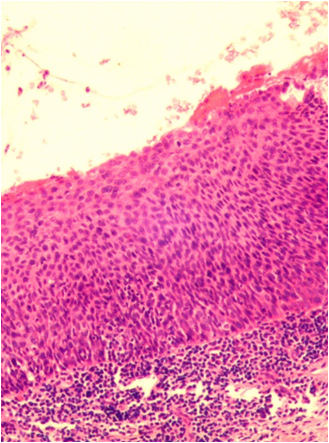
图25-2 LSIL 图25-3 HSIL
【临床表现】
无特殊症状。偶有阴道排液增多,伴或不伴臭味。也可在性生活或妇科检查后发生接触性出血。检查子宫颈可光滑,或仅见局部红斑、白色上皮,或子宫颈糜烂样表现,未见明显病灶。
【诊断】
1.子宫颈细胞学检查 是SIL及早期子宫颈癌筛查的基本方法,细胞学检查特异性高,但敏感性较低。可选用巴氏涂片法或液基细胞涂片法(详见第三十四章第三节“生殖道脱落细胞学检查”)。筛查应在性生活开始3年后开始,或21岁以后开始,并定期复查。子宫颈细胞学检查的报告形式主要有TBS(the Bethesda system)分类系统,该系统较好地结合了细胞学、组织学与临床处理方案,推荐使用。
2.HPV检测 敏感性较高,特异性较低。可与细胞学检查联合应用于25岁以上女性的子宫颈癌筛查;也可用于21~25岁女性细胞学初筛为轻度异常的分流,当细胞学为意义未明的不典型状细胞(ASCUS)时进行高危型HPV检测,阳性者行阴道镜检査,阴性者12个月后行细胞学检查;也可作为25岁以上女性的子宫颈癌初筛,阳性者用细胞学分流,阴性者常规随访。
3.阴道镜检查 筛査发现有异常,如细胞学 ASCUS伴HPV检测阳性、或细胞学LSIL及以上、或HPV检测16/18型阳性者,建议行阴道镜检查。
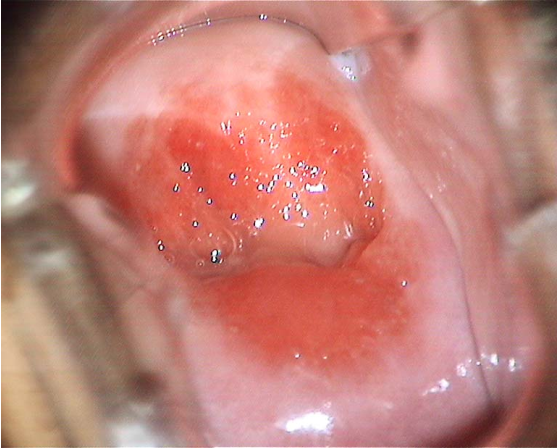
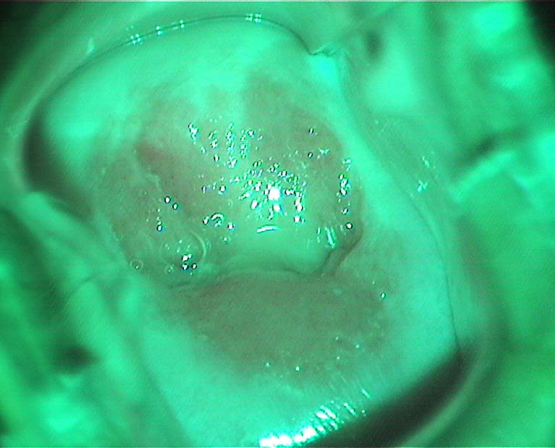
阴道镜检查(白光直接观察) 阴道镜检查(加用绿色滤光镜片观察宫颈血管)
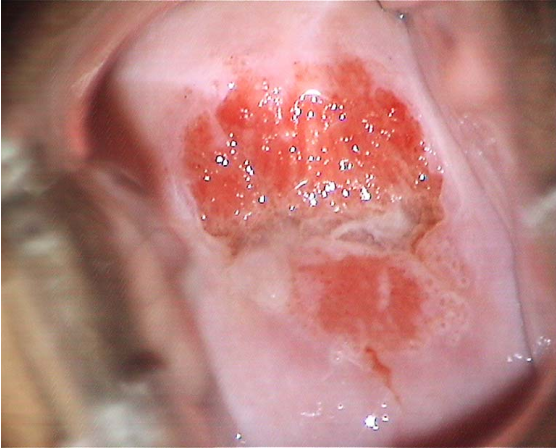
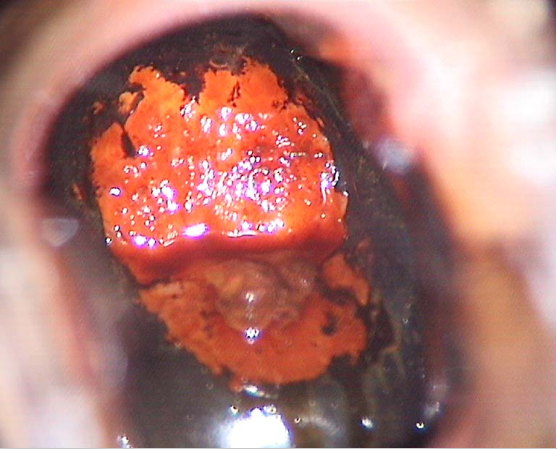
阴道镜检查(醋酸溶液作用,观察鳞柱上皮交界处) 阴道镜检查(碘溶液作用,观察)
4.子宫颈活组织检查 是确诊子宫颈鳞状上皮内病变的可靠方法。任何肉眼可疑病灶,或阴道镜诊断为高级别病变者均应行单点或多点活检。若需要了解子宫颈管的病变情况,应行子宫颈管搔刮术(endocervical curettage,ECC)。
【治疗】
1.LSIL 约60%会自然消退,细胞学检查为LSIL及以下者可仅观察随访。在随访过程中病变发展或持续存在2年者宜进行治疗。细胞学为HSIL,阴道镜检查充分者可采用冷冻和激光等消融治疗;若阴道镜检查不充分、或不能排除HSIL、或ECC阳性者采用子宫颈锥切术。
2.HSIL 可发展为浸润癌,需要治疗。阴道镜检查充分者可用子宫颈锥切术或消融治疗;阴道镜检查不充分者宜采用子宫颈锥切术,包括子宫颈环形电切除术(loop electrosurgical excisi-on procedure,LEP)和冷刀锥切术。经子宫颈锥切确诊、年龄较大、无生育要求、合并有其他妇科良性疾病手术指征的HSIL也可行筋膜外全子宫切除术。
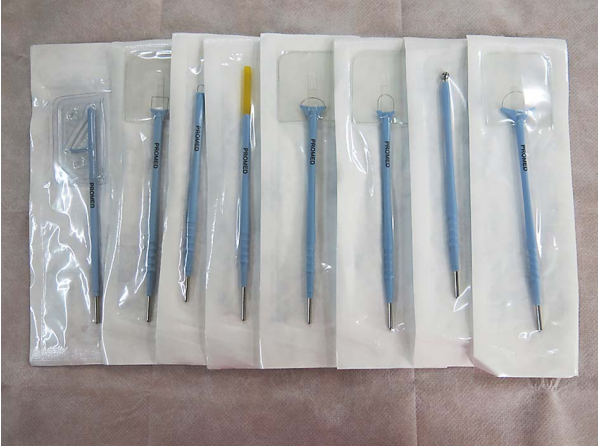
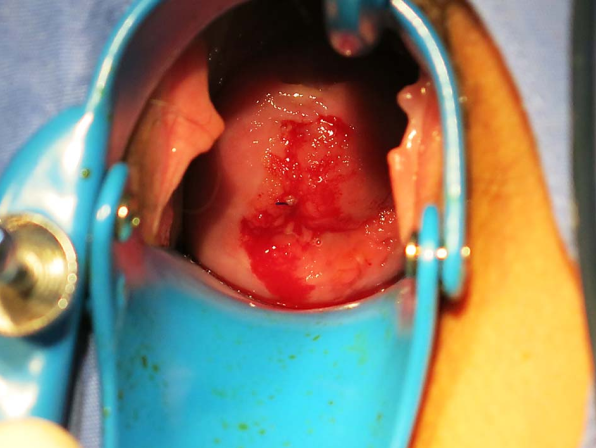
子宫颈环形电切术的器械 暴露宫颈
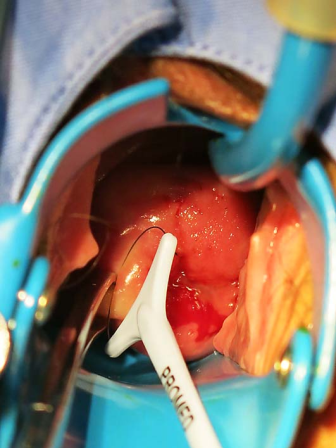
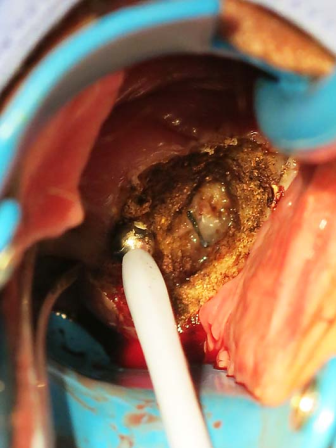
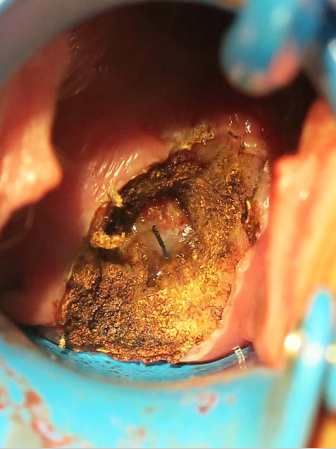
电环切除病变宫颈 电凝止血 宫颈创面
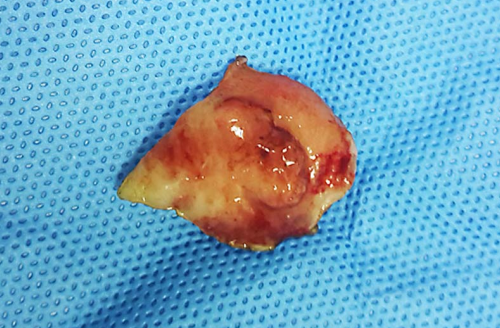
切除的部分宫颈组织
【妊娠合井子宫颈鳞状上皮内病变】
妊娠期间,增高的雌激素使柱状上皮外移至子宮颈阴道部,转化区的基底细胞出现不典型增生改变;妊期免疫功能可能低下,易患HPV感染。诊断时应注意妊娠时转化区的基底细胞可有核增大、深染等表现,细胞学检查易误诊,但产后6周可恢复正常。大部分妊娠期患者为LSIL,仅约14%为HSIL。妊娠期SIL仅作观察,产后复查后再处理。


