主要组织学类型是鳞癌,腺癌次之。
直接蔓延和淋巴转移是子宫颈癌的主要转移途径。
接触性出血是外生型子宫颈癌的早期症状。
根据FIGO临床分期选择治疔方法。一般早期采用手术治疗,晚期采用放射治疗。
子宫颈癌(cervical cancer)是最常见的妇科恶性肿瘤。高发年龄为50~55岁。由于子宫颈癌筛查的普及,得以早期发现和治疗子宫颈癌和癌前病变,其发病率和死亡率明显下降。
【发病相关因素】
同“子宫颈鳞状上皮内病变”。
【组织发生和发展】
SIL形成后继续发展,突破上皮下基底膜,浸润间质,形成子宫颈浸润癌(图25-4)。
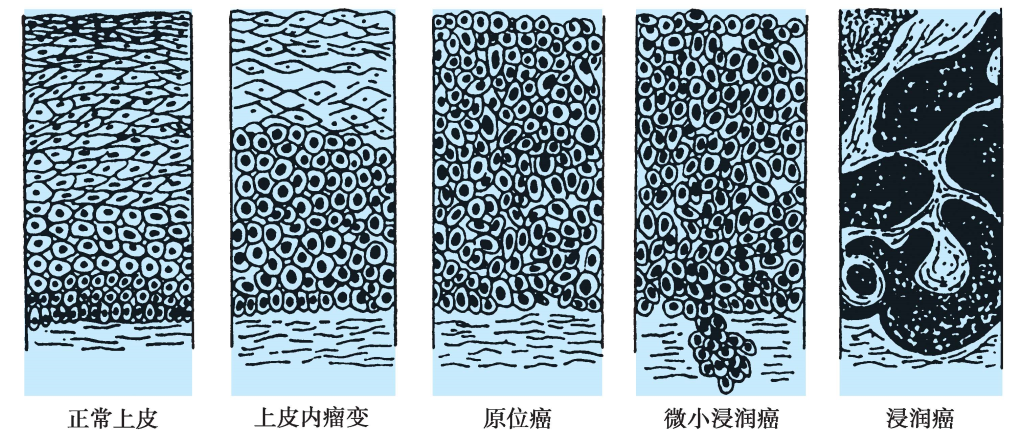
图25-4 子宫颈正常上皮-上皮内病变-浸润癌
【病理】
1.浸润性鱗状细胞癌 占子宫颈癌的75%~80%。
(1)巨检:微小浸润性鳞状细胞癌肉眼观察无明显异常,或类似子宫颈柱状上皮异位。随病变发展,可形成4种类型(图25-5)。
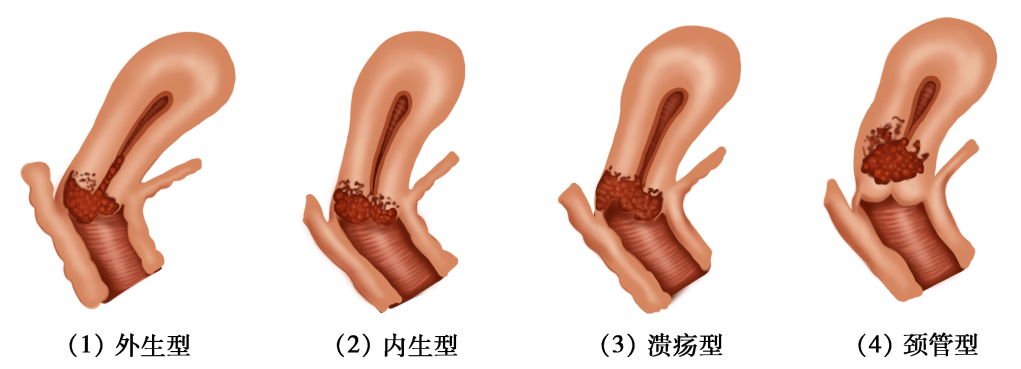
图25-5 子宫颈癌类型(巨检)
1)外生型:最常见,癌灶向外生长呈乳头状或菜花样,组织脆,触之易出血。常累及阴道。
2)内生型:癌灶向子宫颈深部组织浸润,子宫颈表面光滑或仅有柱状上皮异位,子宫颈肥大变硬,呈桶状。常累及宫旁组织。
3)溃疡型:上述两型癌组织继发展合并感染坏死,脱落后形成溃疡或空洞,似火山口状。
4)颈管型:癌灶发生于子宫颈管内,常侵人子宫颈管和子宫峡部供血层及转移至盆腔淋巴结。
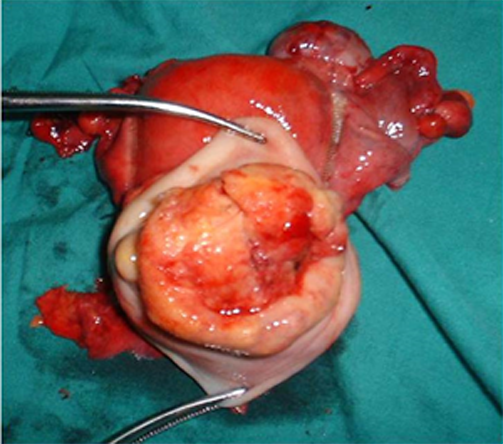
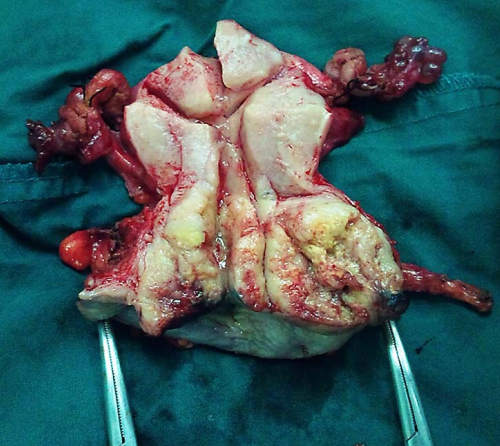
内生型 外生型
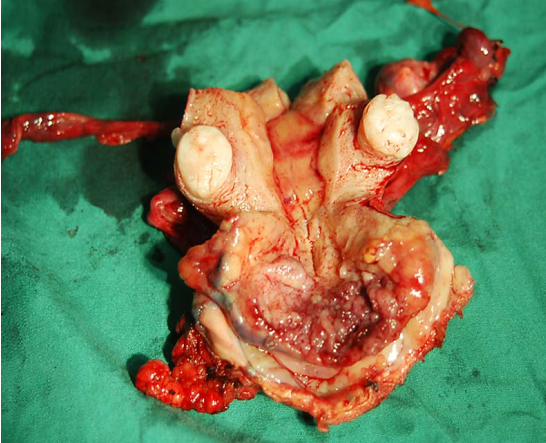
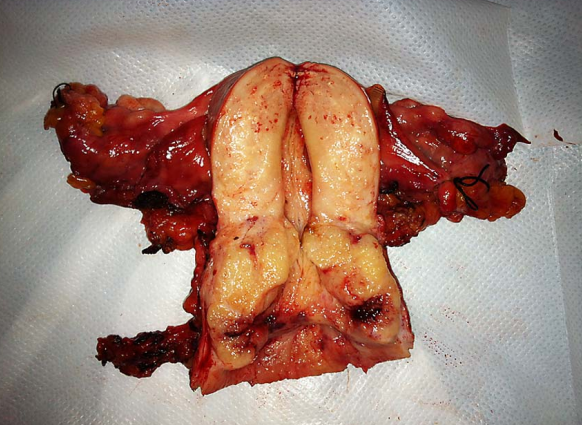
溃疡型 颈管型
(1)显微镜检
1)微小浸润性鱗状细胞癌:指在HSIL(CIN3)基础上镜检发现小滴状、锯齿状癌细胞团突破基底膜,浸润间质。诊断标准见临床分期。
2)浸润性鳞状细胞癌:指癌灶浸润间质范围超出微小浸润癌,多呈网状或团块状浸润间质。根据癌细胞核的多形性与大小及核分裂程度等可将状细胞癌分为高(Ⅰ级)、中(Ⅱ级)、低分化(Ⅲ级)3种,这种分级法可能提供了肿瘤对化疗和放疗相关的预后信息,但目前更倾向于分为角化型和非角化型。角化型:大致相当于高分化鳞癌,细胞体积大,有明显角化珠形成,可见细胞间桥,细胞异型性较轻,无核分裂或核分裂军见。非角化型:大致相当于中分化和低分化鳞癌。细胞体积大或较小,可有单细胞角化但无角化珠,细胞间桥不明显,细胞异型性常明显,核分裂象多见。除上述最常见的两种亚型外还有以下多种亚型:乳头状鳞状细胞癌、基底细胞样状细胞癌、湿疣样癌、疣状癌、鳞状移形细胞癌和淋巴上皮样瘤样癌。
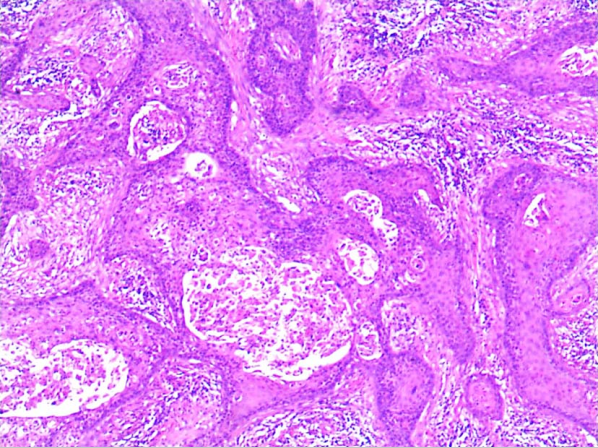
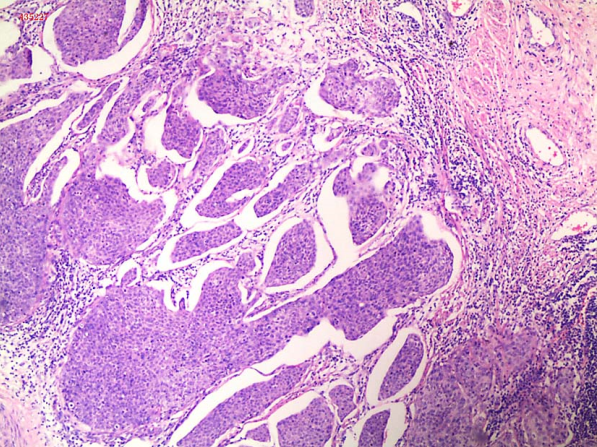
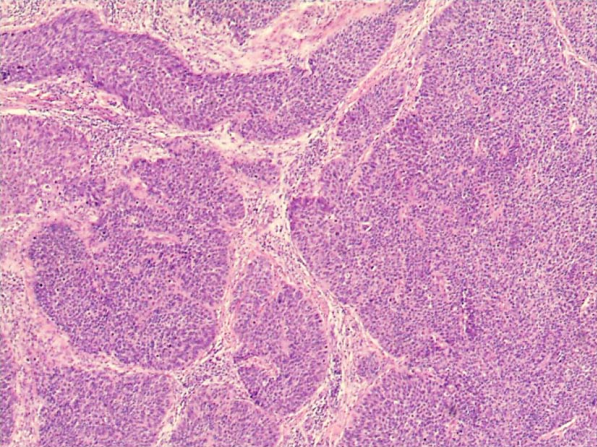
高分化鳞癌镜下观(40×) 中分化鳞癌镜下观(40×) 低分化鳞癌镜下观(40×)
2.腺癌 近年来子官腺癌的发生率有上升趋勢,占子宫颈癌的20%~25%。
(1)巨检:来自子宫管内,浸润管壁;或自子宫颈管内向子宫颈外口突出生长;常可侵犯宫旁组织;病灶向子宫颈管内生长时,子宫颈外观可正常,但因子宫颈管膨大,形如桶状。
(2)显微镜检
1)普通型宫颈腺癌:最常见的组织学业型,约占宫颈腺癌的90%。虽然来源于子宫颈管柱状黏液细胞、偶尔间质内可见黏液池形成,但肿瘤细胞内见不到明确黏液,胞浆双嗜性或嗜酸性。镜下见腺体结构复杂、呈筛状和乳头状,腺上皮细胞增生呈复层,核异型性明显,核分裂象多见。该亚型绝大部分呈高-中分化。
2)黏液性腺癌:该亚型的特征是细胞内可见明确黏液,又进一步分为胃型、肠型、印戒细胞样和非特指型。其中,高分化的胃型腺癌,既往称为微偏腺癌(minimal deviation adenocarcin-oma,MDA),虽然分化非常好,但几乎是所有宫颈腺癌中预后最差的一种亚型,5年生存率仅为普通宫颈腺癌的一半。
3.其他 少见类型如腺鳞癌、腺样基底细胞癌、绒毛状管状腺癌、内膜样癌等上皮性癌,神经内分泌肿瘤,间叶性肿瘤等。
【转移运径】
主要为直接蔓延和淋巴转移,血行转移极少见。
1.直接蔓延 最常见,癌组织向邻近器官及组织扩散。常向下累及阴道壁,极少向上累及宫腔向两侧扩散可累及主韧带及子宫颈旁、阴道旁组织直至骨盆壁;癌灶压迫或侵及输尿管时,可引起输尿管阻塞及肾积水。晚期可向前、后蔓延侵及膀胱或直肠。
2.淋巴转移 癌灶侵入淋巴管,形成瘤栓,随淋巴液引流进人局部淋巴结。淋巴转移一级组包括子宫旁、闭孔、髂内、髂外、髂总、骶前淋巴结;二级组包括腹股沟深浅淋巴结、腹主动脉旁淋巴结。
3.血行转移 极少见,晚期可转移至肺、肝或骨骼等。
【临床分期】
采用国际妇产科联盟(FIGO,2018年)的临床分期标准(表25-1)。临床分期在治疗前进行,治疗后不再更改(图25-6)。
表25-1 子宫颈癌临床分期(FIGO,2018年)
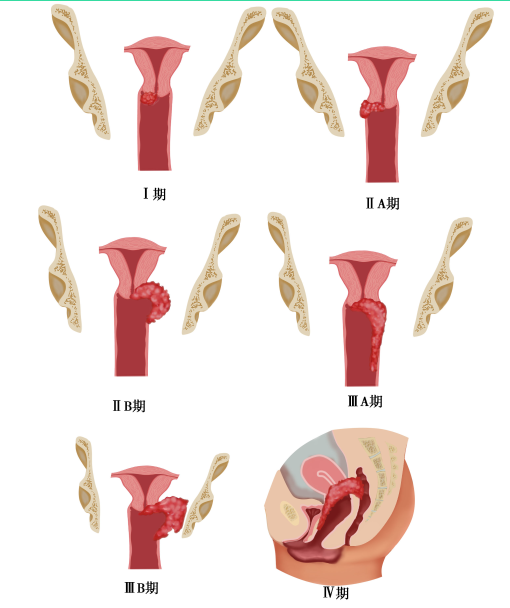
图25-6 子宫颈癌临床分期示意图
【临床表现】
早期子宫颈癌常无明显症状和体征。子宫颈管型患者因子宫颈外观正常易漏诊或误诊。随病变发展,可出现以下表现:
1.症状
(1)阴道流血:常表现为接触性出血,即性生活或妇科检查后阴道流血。也可表现为不规则阴道流血,或经期延长、经量增多。老年患者常为绝经后不规则阴道流血。出血量根据病灶大小、侵及间质内血管情况而不同,若侵性大血管可引起大出血。一般外生型癌出血较早,量多;内生型癌出血较晚。
(2)阴道排液:多数患者有白色或血性、稀薄如水样或米泔状、有腥臭味的阴道排液。晚期患者因癌组织坏死伴感染,可有大量米泔样或脓性恶臭白带。
(3)晚期症状:根据癌灶累及范围出现不同的继发性症状。如尿频、尿急、便秘、下肢肿痛等;癌肿压迫或累及输尿管时,可引起输尿管梗阻、肾盂积水及尿毒症;晚期可有贫血、恶病质等全身衰竭症状。
2.体征 微小浸润癌可无明显病灶,子宫颈光滑或糜烂样改变。随病情发展,可出现不同体征。外生型子宫颈癌可见息肉状、菜花状赘生物,常伴感染,质脆易出血;内生型表现为子宫颈肥大、质硬、子宫颈管膨大;晚期癌组织坏死脱落,形成溃疡或空洞伴恶臭。阴道壁受累时,可见赘生物生长或阴道壁变硬;宫旁组织受累时,双合诊、三合诊检查可扪及子宫颈旁组织增厚、结节状、质硬或形成冰冻骨盆状。
【诊断】
早期病例的诊断应采用子宫颈细胞学检查和(或)HPV检测、阴道镜检查、子宫颈活组织检查的“三阶梯”程序,确诊依据为组织学诊断。检查方法同本章第一节“子宫颈鳞状上皮内病变”。子宫颈有明显病灶者,可直接在癌灶取材。
对子宫颈活检为HSIL但不能除外浸润癌者、或活检为可疑微小浸润癌需要测量肿瘤范围或除外进展期浸润癌者,需行子宫颈锥切术。切除组织应作连续病理切片(24-36张)检查。
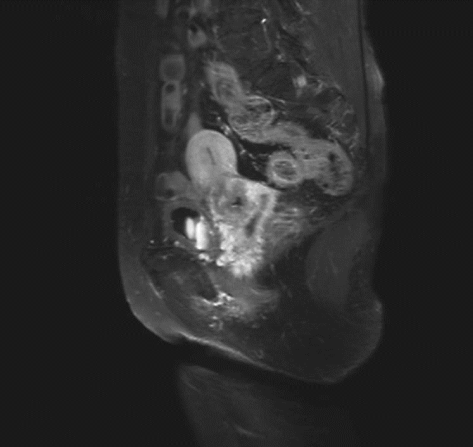
确诊后根据具体情况选择胸部X线或CT平扫、静脉肾盂造影、膀胱镜检査、直肠镜检查、超声检查及盆腔或腹腔增强CT或磁共振、PET-CT等影像学检查。
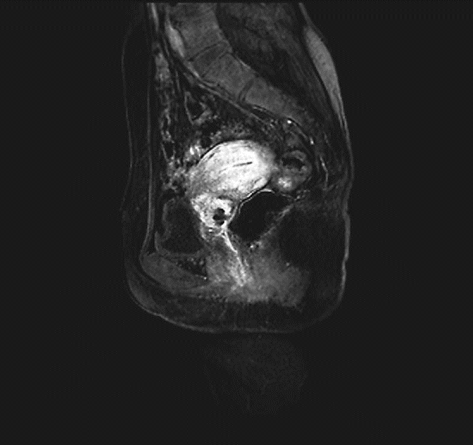
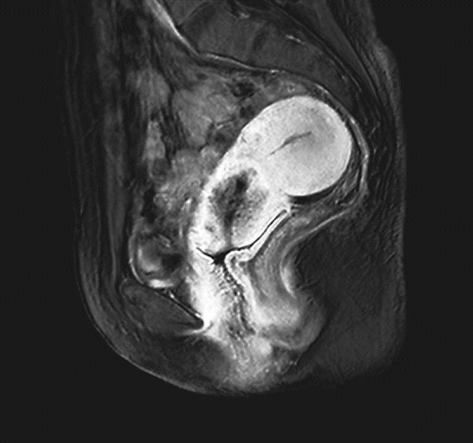
ⅠB1期宫颈癌MR ⅠB2期宫颈癌MR
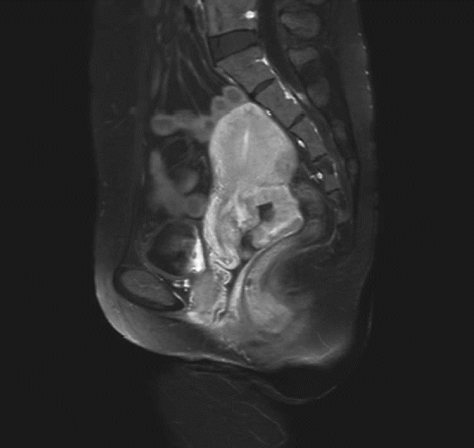
ⅡA1期宫颈癌MR ⅡA2期宫颈癌MR

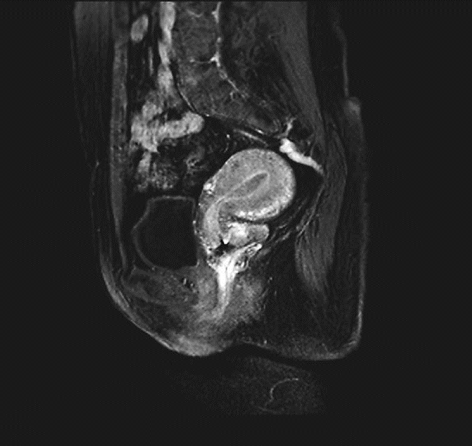
ⅡB期宫颈癌MR ⅢA期宫颈癌MR
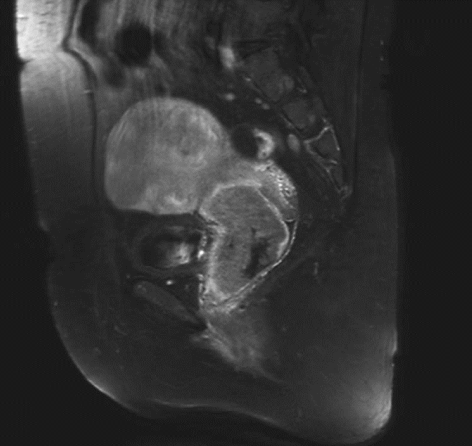
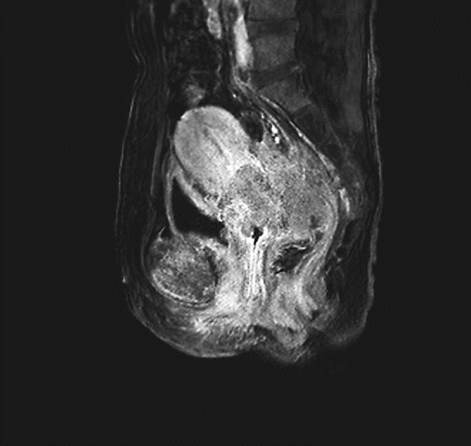
ⅢB期宫颈癌MR ⅣB期宫颈癌MR
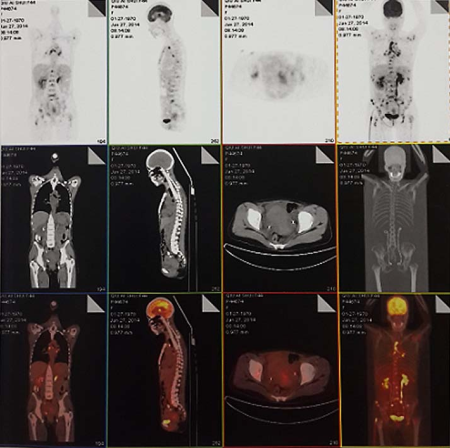
子宫颈癌全身广泛转移PET-CT
【鉴别诊断】
主要依据子宫颈活组织病理检查,与有类似临床症状或体征的各种子宫颈病变鉴别。包括:①子宫颈良性病变:子宫颈柱状上皮异位、子宫颈息肉、子宫颈子宫内膜异位症和子宫颈结核性溃疡等;②子宫颈良性肿瘤:子宫颈管肌瘤、子宫颈乳头瘤等;③子宫颈转移性癌等。
【处理】
根据临床分期、患者年龄、生育要求、全身情况、医疗技术水平及设备条件等,综合考虑制定适当的个体化治疗方案。采用手术和放疗为主、化疗为辅的综合治疗。
1.手术治疗 手术的优点是年轻患者可保留卵巢及阴道功能。主要用于早期子宫颈癌(ⅠA~ⅡA期)患者。①ⅠA1期:无淋巴脉管间隙浸润者行筋膜外全子宫切除术,有淋巴脉管间隙浸润者按ⅠA2期处理。②ⅠA2期:行改良广泛性子切除术及盆腔淋巴结切除术或考虑前哨淋巴结绘图活检(sentinel lymphnode mapping)。③ⅠB1期、和ⅠB2期ⅡA1期:行广泛性子宫切除术及盆腔淋巴结切除术或考虑前哨淋巴结绘图活检,必要时行腹主动脉旁淋巴取样。④部分ⅠB2期和ⅡA2期:行广泛性子宫切除术及盆腔淋巴结切除术和选择性腹主动脉旁淋巴结取样;或同期放、化疗后行全子宫切除术;也有采用新辅助化疗后行广泛性子宫切除术及盆腔淋巴结切除术和选择性腹主动脉旁淋巴结取样。未绝经、<45岁的鳞癌患者可保留卵巢。要求保留生育功能的年轻患者,ⅠA1期无淋巴脉管间隙浸润者可行子宫颈锥形切除术(至少3cm阴性切缘);ⅠA1期有淋巴脉管间隙浸润和ⅠA2期可行子宫颈锥形切除术加盆腔淋巴结切除术或考虑前哨淋巴结绘图活检,或和ⅠB1期处理相同;一般推荐ⅠB1期行广泛性子宫颈切除术及盆腔淋巴结切除术或考虑前哨淋巴结绘图活检,但若经腹或腹腔镜途径手术,手术指征也可扩展至ⅠB2期。
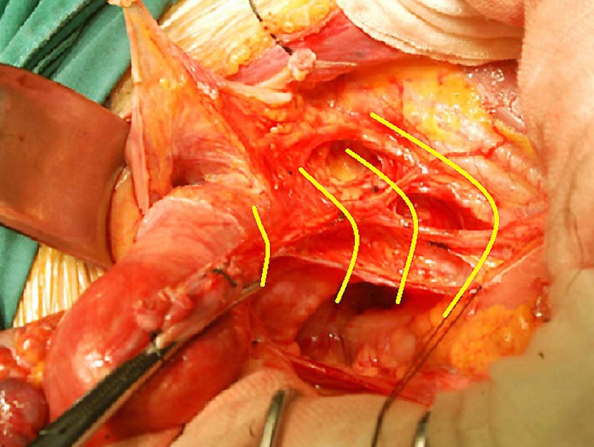
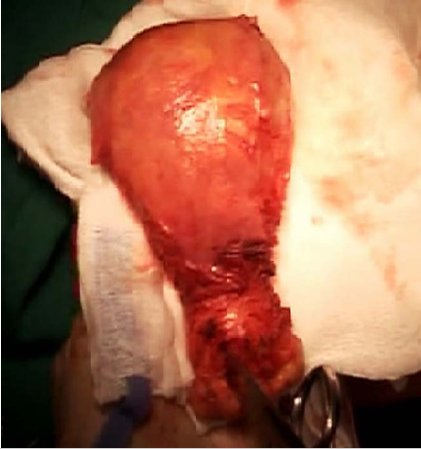
从左至右依次为Ⅰ、Ⅱ、Ⅲ及Ⅳ型子宫切除术的范围 Ⅰ型即筋膜外子宫切除术标本
Ⅲ型即广泛子宫切除术标本 盆腔淋巴结切除术标本
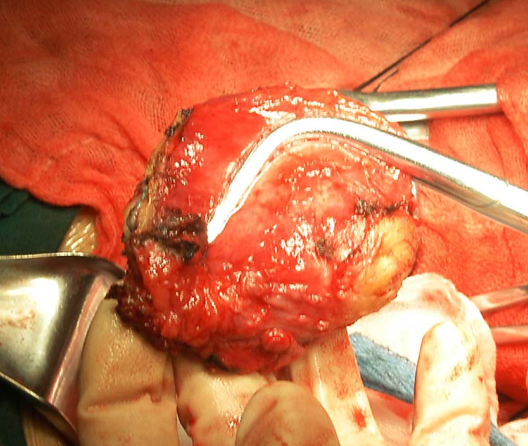
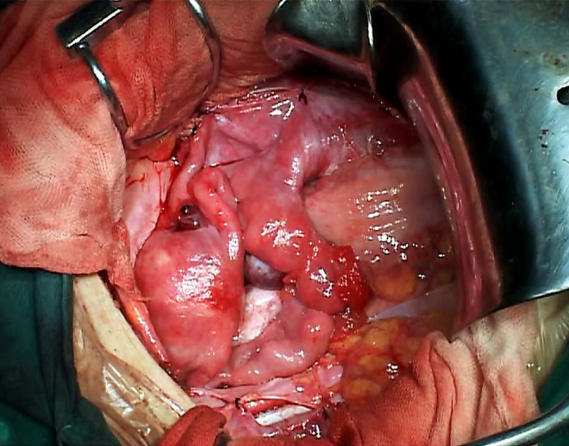
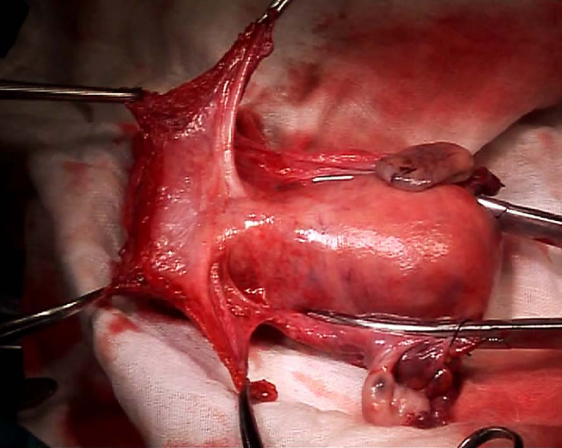
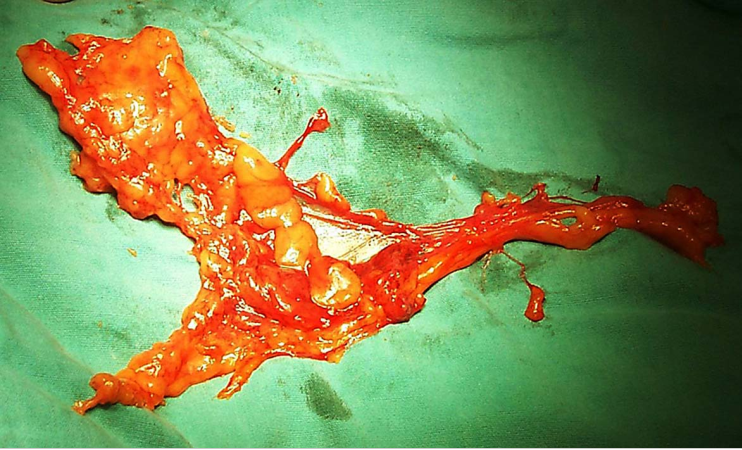
广泛子宫颈切除术切除的子宫颈及宫旁组织 广泛子宫颈切除术后功能重建的子宫及双附件
2.放射治疗 ①根治性放疗:适用于部分ⅠB2期和ⅡA2期和ⅡB~ⅣA期患者和全身有适宜手术的ⅠA1~ⅠB2/ⅡA1期患者;②辅助放疗:适用于手术后病理检查发现有中、高危因素的患者;③姑息性放疗:适用于晚期患者局部减瘤放疗或对转移病灶姑息放疗。放射治疗包括体外照射和腔内放疗。外照射放疗以三维适形放疗及调强放疗为主,主要针对子宫、宫旁及转移淋巴结。腔内放疗多采用铱-192(192Ir)高剂量率腔内及组织间插值放疗,主要针对宫颈、阴道及部分宫旁组织给以大剂量照射。外照射和腔内放疗的合理结合,使病变部位的剂量分布更符合肿瘤生物学特点,可提高局部控制率。
3.全身治疗 包括全身化疗和靶向治疗、免疫治疗。化疗主要用于晚期、复发转移患者和根治性同期放化疗,也可用于手术前后的辅助治疗。常用抗癌药物有顺铂、卡铂、紫杉醇、拓扑替康等,多采用静脉联合化疗,也可用动脉局部灌注化疗。靶向药物主要是贝伐珠单抗,常与化疗联合应用。方案如顺铂/紫杉醇/贝伐珠单抗、顺铂/紫杉醇、拓扑替康/紫杉醇/贝伐珠单抗、卡铂/紫杉醇方案等。免疫治疗如PD-1/PD-L1抑制剂等也被推荐用于晚期和复发子宫颈癌。
【预后】
与临床期别、病理类型等密切相关,有淋巴结转移者预后差。
【随访】
治疗后2年内应每3~6个月复查1次;3~5年内每6个月复査1次;第6年开始每年复查1次。随访内容包括妇科检查、阴道脱落细胞学检査、胸部X线摄片、血常规及子宫颈鳞状细胞癌抗原(SCCA)、超声、CT或磁共振等。
【预防】
子宫颈癌是可以预防的肿瘤。①推广HPV预防性疫苗接种(一级预防),通过阻断HPV感染预防子宫颈癌的发生;②普及、规范子宫颈癌筛查,早期发现SIL(二级预防);及时治疗高级别病变,阻断子宫颈浸润癌的发生(三级预防);③开展预防子宮颈癌知识宣教,提高预防性疫苗注射率和筛查率,建立健康的生活方式。
【子宫颈癌合并妊娠】
较少见。妊娠期出现阴道流血时,在排除产科因素引起的出血后,应做详细的妇科检查,对子宫颈可疑病变作子宫颈细胞学检查、HPV检测、阴道镜检查,必要时行子宮颈活检明确诊断。因子宫颈锥切可能引起出血、流产和早产,只有在细胞学和组织学提示可能是浸润癌时,才作子宫颈锥切。
治疗方案的选择取决于患者期别、孕周和本人及家属对维持妊娠的意愿,采用个体化治疗。对于不要求维持妊娠者,其治疗原则和非妊娠期子宫颈癌基本相同。对于要求维持妊娠者,妊娠20周之前经锥切确诊的ⅠA1期可以延迟治疗,一般不影响孕妇的预后,其中锥切切缘阴性可延迟到产后治疗;妊娠20周之前诊断的ⅠA2期及其以上患者应终止妊娠并立即接受治疗。妊娠28周后诊断的各期子宫颈癌可以延迟至胎儿成熟再行治疗。对于妊娠20~28問诊断的患者,可以根据患者及家属的意愿采用延迟治疗或终止妊娠立即接受治疗,延迟治疗至少不明显影响ⅠA2期及ⅠB1期子宫颈癌的预后。1B2期及以上期别决定延迟治疗者,建议采用新辅助化疗来延缓疾病进展。在延迟治疗期间,应密切观察病情,如肿瘤进展,应及时终止妊娠。除ⅠA期外,延迟治疗应在妊娠34周前终止妊娠。分娩方式一般采用子宫体部剖宫产。
(林仲秋)


