-
1 章节内容
-
2 章节讨论
-
3 章节测验











第一节 药物的化学结构与生物活性的关系
Structure- Activity Relationships of Drugs
药物化学研究的中心内容之一是药物的化学结构如何影响生物活性。药物的化学结构决定了它的理化性质( physicochemical properties)并直接影响药物分子在体内的吸收(absorption)、分布( distribution)、代谢( metabolism)和排泄( excretion)。理化性质是指一个分子所包含的官能团对其酸碱性、水溶性、分配系数、晶体结构和立体化学等的影响。为了设计更好的药物分子,药物化学工作者需要知道每一个官能团对分子全部理化性质的相对贡献,即进行通常所指的构效关系研究。
药物在体内的基本过程是给药、吸收、转运、分布并到达作用部位、产生药理作用(包括副作用)和排泄。分布到作用部位并且在作用部位达到有效的浓度是药物产生活性的重要因素之一,药物的转运过程与其理化性质有关;药物在作用部位与受体的相互作用则是产生药效的另一个重要因素。因此药物产生药效的两个主要的决定因素是药物的理化性质以及药物和受体的相互作用。
一、理化性质与生物活性
( Physicochemical Propertiesand Biological Activities of Drugs)
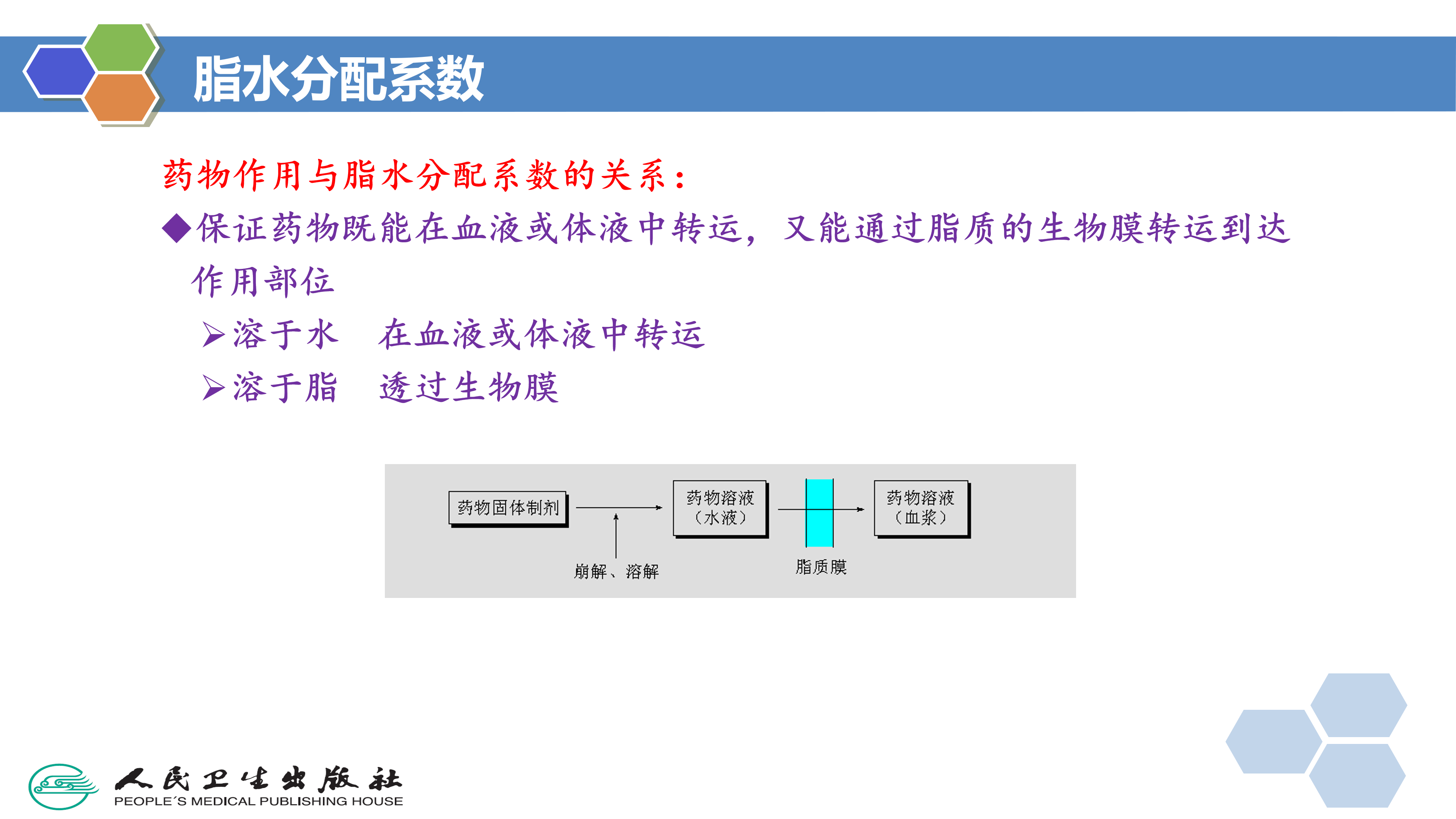
药物口服给药后,药物经胃肠道吸收进入血液。药物在转运过程中,必须通过各种生物膜,才能到达作用部位或受体部位。药物分布到作用部位并且在作用部位达到有效浓度,是药物与受体结合的基本条件。但是,能和受体良好结合的药物并不一定具有适合转运过程的最适宜理化性质参数,如有些酶抑制剂在体外实验具有很强活性,但因它的脂水分配系数过高或过低,不能在体内生物膜的脂相-水相-脂相间的生物膜组织内转运,无法到达酶所在的组织部位,造成体内实验几乎无效。因此,设计新药时必须考虑到化合物的理化性质。
(一) 脂水分配系数与生物活性
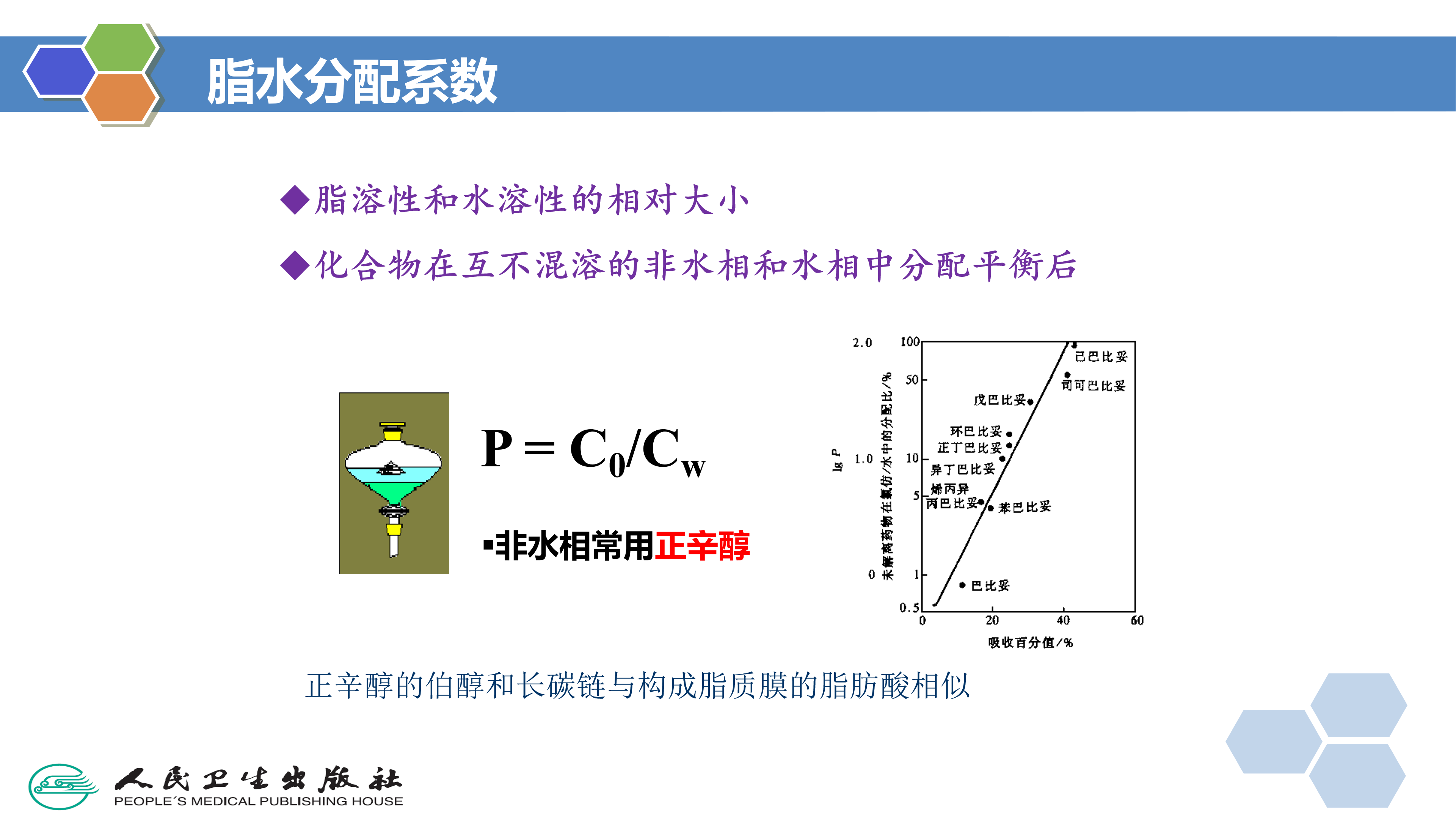
脂水分配系数(lipid-water partition coefficient,P)是化合物在有机相和水相中分配达到平衡时的浓度之比值,即P=C0/w,常用logP表示,logP=log(Co/Cw)。在构效关系研究中,常选用正辛醇(1-octanol).为有机相测定脂水分配系数,因为正辛醇有一个极性基团(伯醇)和一个长的碳链,与构成脂质膜的脂肪酸相似。药物转运扩散至血液或体液,需有一定的亲水性( hydrophilicity);药物通过脂质的生物膜转运,需有一定的亲脂性( lipophilicity))或疏水性(hydrophobicity)。
Log P是构成整个分子的所有官能团的亲水性和疏水性的总和,分子中的每一个取代基对分子整体的亲水性和疏水性都有影响,即LogP=∑m( fragments)。当药物结构中增加氢键的给予体官能团或氢键的接受体官能团时,可增加药物的整体水溶性。这种官能团越多,药物的亲水性越强,这种官能团主要有羟基、氨基和羧基。通过这些官能团的数目,可以判断药物的溶解度趋势。分子中如含有亲脂性的烷基、卤素和芳环等,一般会增加药物的脂溶性。P值越大,则药物的亲脂性越高。一般来说,脂水分配系数应在一个适当的范围,才能显示最好的药效。例如,中枢神经系统的药物需要穿过血脑屏障,适当增加药物亲脂性可增强活性,降低亲脂性可使活性降低。易于穿过血脑屏障的适宜的分配系数logP为2左右。
(二)酸碱性与生物活性性
人体70%-75%是由水组成的,人服用药物后可按照稀溶液理论解释和预测药物的酸碱酸。多数药物为弱酸或弱碱,其解离度由化合物的解离常数pKa,和溶液介质的pH决定。药物解离后以部分离子型和部分分子型两种形式存在,以醋酸和甲胺为例,pKa,的计算方法为
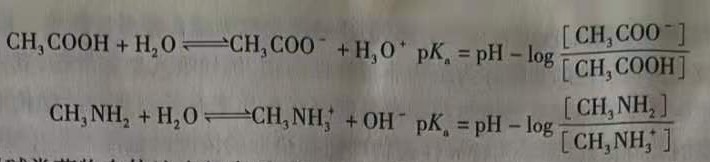
弱酸或弱碱类药物在体液中解离后,离子型与非离子型(分子型)分子的比率由解离常数pKa和介质的pH决定。
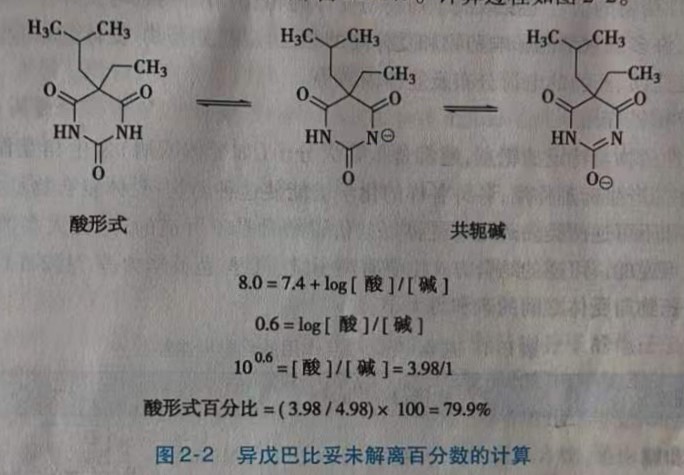
如果知道分子中的官能团是酸性还是碱性,便可预测该分子在给定pH下是否可以被离子化。如果知道该分子中官能团的pKa和分子周围环境的pH,可定量预测分子的离子化程度。例如,巴比妥酸( barbital acid)的pKa为4.12,在pH7.4时,99%以上解离,以离子状态存在,不能透过细胞膜和血脑屏障,故无镇静作用。异戊巴比妥( amobarbital)pKa为8.0,在pH为7.4时未解离(酸形式)占79.9%,离子化(共轭碱)占20.1%。计算过程如图2-2。
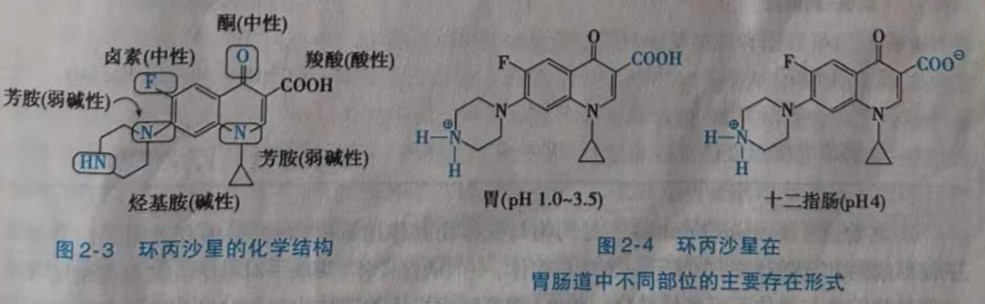
一个分子中可能含有多种官能团,而具有酸碱两性。例如,喹诺酮类抗菌药环丙沙星(ciprofloxacin)(图2-3)含有一个烷基仲氨基和一个羧酸基,根据溶液的pH,这个分子既可以接受一个质子,也可以给出一个质子,或同时发生,是一个两性化合物,其pKa(HA)、pKa,(HB+)分别为6.0和8.8。在胃肠不同阶段,有不同的酸碱性,因此环丙沙星有不同的解离形式,在pH4.0时,烷氨基和羧基均被离子化;在pH为1.0~3.5时,只有烷氨基团离子化(图2-4)。
药物常以分子型通过生物膜,在膜内的水介质中解离成离子型再起作用。因此药物需要有适宜的解离度。
一、药物-受体相互作用
( Drug-receptor Interaction)
根据药物在体内的作用方式,把药物分为结构特异性药物(structurally specific drug)和结构非特异性药物( structurally nonsespecific drug)。大多数药物通过与受体或酶的相互作用而发挥药理作用,药物结构上细微的改变将会影响药效,这种药物称为结构特异性药物。相反,结构上微小的改变不改变生物活性的药物称为结构非特异性药物,例如吸入型麻醉药,其药理活性主要与药物在周围空气中的局部蒸气压与药物本身的蒸气压比率有关。典型的结构非特异性药物只有在高浓度时才有活性,而结构特异性药物即使在很低的浓度时也能产生生物效应,其原因之一是该类药物能利用某些效能扩增机制,例如它们能激活受体,产生第二信使,从而在细胞内发挥作用。
通常,受体是指体内的激素和神经递质所作用的生物分子,通过作用在细胞间实行信号转导,这些生物分子通常都是药物作用的靶点。除了这些生物分子,还有其他一些蛋白质分子如酶也有重要的生理功能,也是药物作用的靶点,因此,广义的受体是指所有的生物大分子,如激素和神经递质的受体、酶、其他蛋白质和核酸等。
结构特异性药物的活性主要取决于药物与受体的相互作用,药物与受体形成复合物后才能产生药理作用,许多因素都能影响药物和受体间的相互作用,如药物-受体的结合方式和结合强度、药物的各官能团、药物的电荷分布及立体因素等。
(一) 化学键的作用
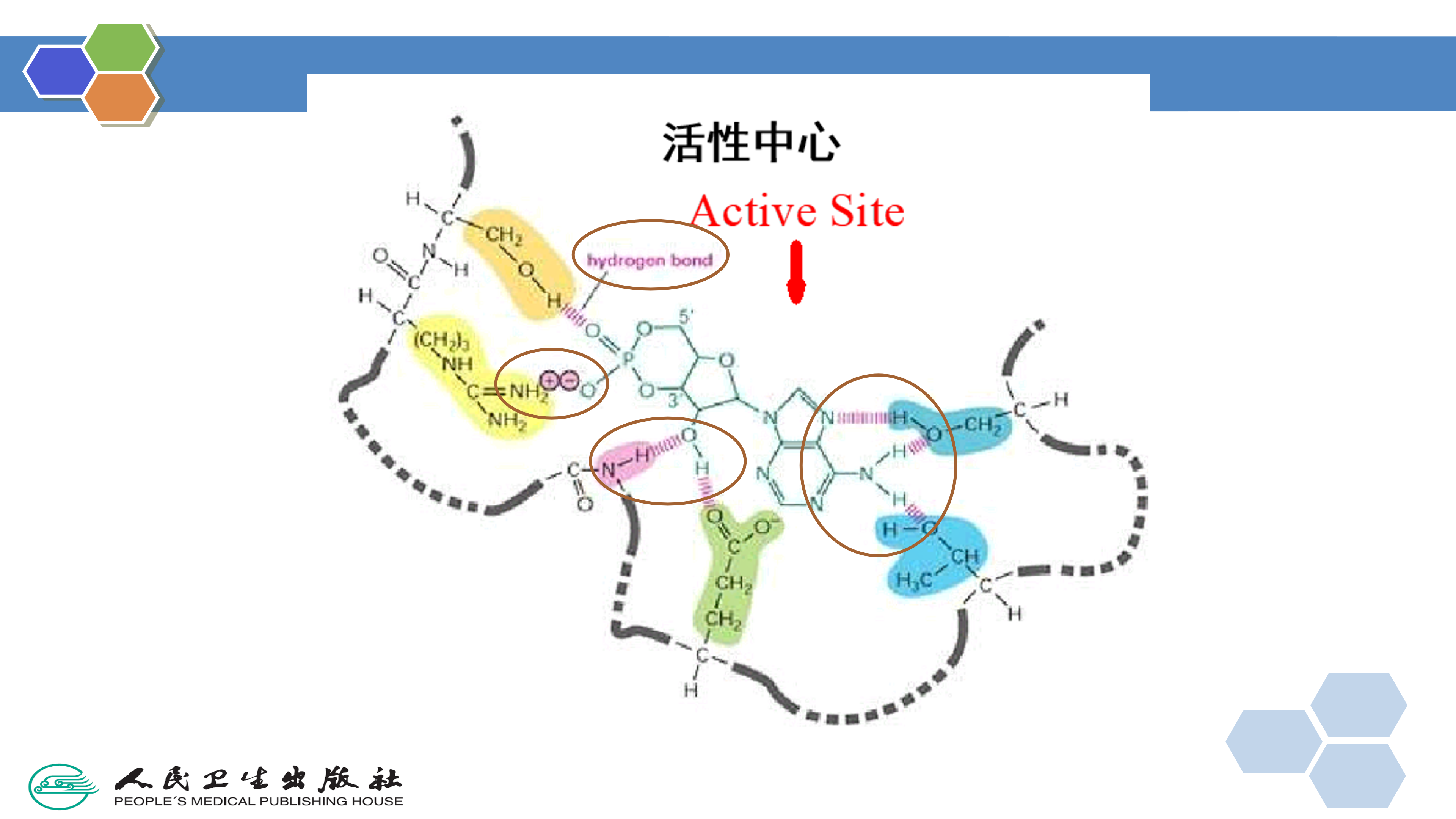
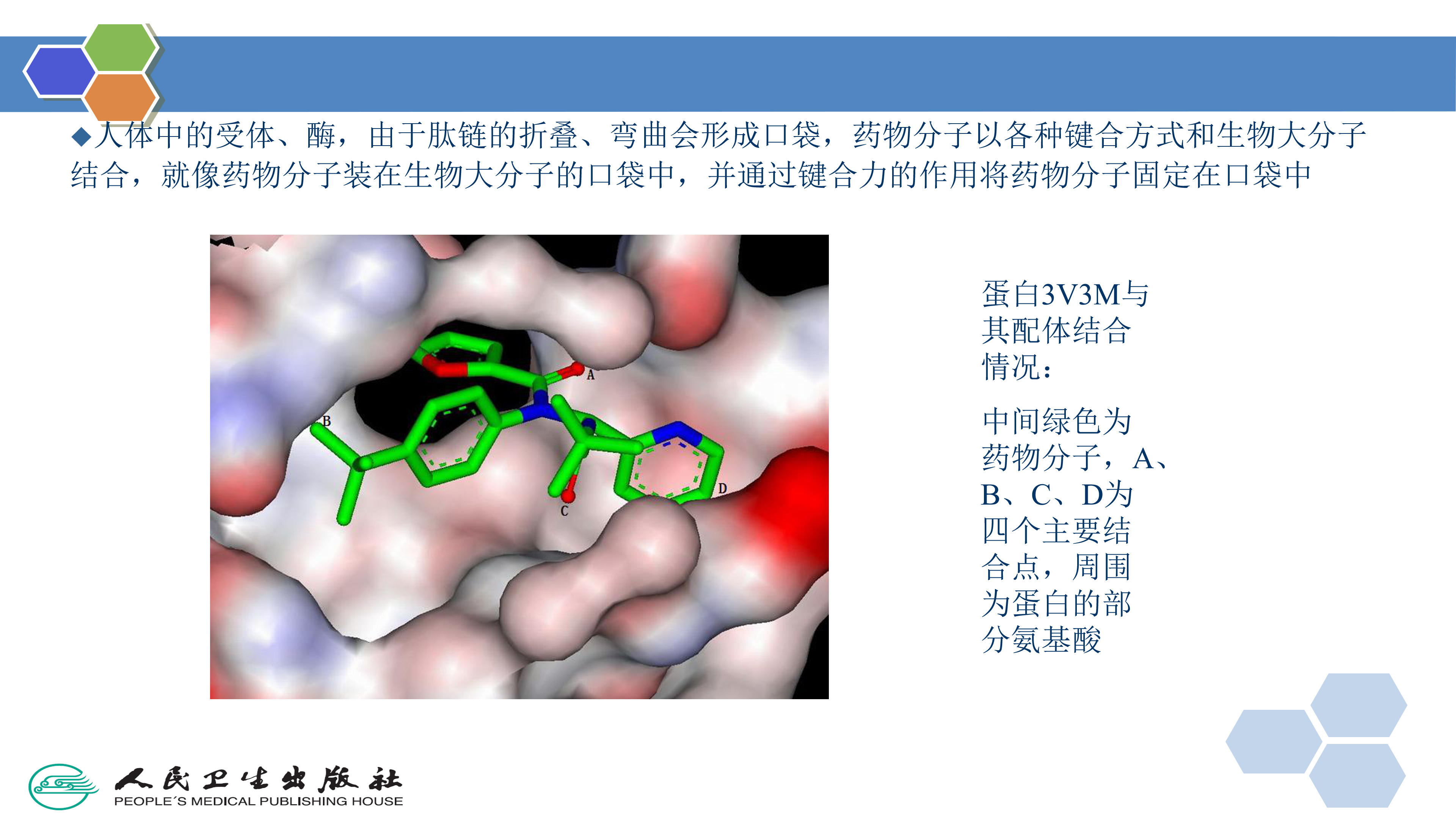
结构特异性药物与特定的靶点,通常是生物大分子(如受体或酶)发生相互作用形成药物-受体复合物,才能产生药理作用,各种各样的化学键能使这种药物-受体复合物稳定。这些化学键可分为可逆和不可逆两类。药物与受体以共价键结合是不可逆的,但在大多数情况下,药物与受体结合是可逆的。可逆的结合方式主要有离子键、氢键、范德华力等(表2-1)。这些化学键的总强度决定药物与受体之间的亲和力大小。

1.共价键( covalent bonds) 是药物与受体相互作用最强的键,是由有关原子间共享电子而形成的,即成键的两个原子一个来自配体,一个来自受体共享一对电子。共价键的结合通常能导致配体与受体不可逆的结合。如β-内酰胺类抗生素和烷化剂类抗肿瘤药都是通过与其作用的受体间形成共价键结合而发挥作用的。
2.离子键( ionic bonds) 是指药物带电荷的正(负)离子与受体的负(正)离子之间,因静电引力而产生的电性作用。在生理pH时,药物分子中的羧基、磺酰氨基和脂肪族氨基等基团,均呈电离状态,季铵盐在任何时都呈离子状态。另一方面,主要由蛋白质构成的受体,其分子表面也有许多可以电离的基团,如精氨酸和赖氨酸含有的胍基和游离氨基是碱性基团,在生理pH时全部质子化,生成带正电荷的阳离子。组氨酸的咪唑环,色氨酸的吲哚环也可以质子化,但程度较低,视环境条件而异。门冬氨酸和谷氨酸均含有游离羧基,在生理pH时通常完全电离,生成阴离子基团。
3.氢键( hydrogen bonds) 与电负性较强的原子(如氧、氮、硫)共价结合的氢可与另带有相对负电荷(或富电子)的原子形成氢键。氢键是药物与受体结合时普遍存在的形式。另外,氢键对药物的理化性质也有较大影响。如药物与水形成氢键,可增加药物的水溶性。如果药物分子内形成氢键,则在水中的溶解度减小。
4.疏水键( hydrophobic interactions) 当药物分子中含有烷基链等非极性结构时,水分子在非极性结构外周有序的排列,体系的熵值很小。当药物亲脂部分与受体亲脂部分相互接近时,在两个非极性区之间的水分子有序状态减少,导致体系的熵值增加,体系的自由能降低,稳定了两个非极性部分的结合,这种结合称为疏水键或疏水作用。
5.范德华力( Van der Waals forces) 是指当两个原子核之间的距离为0.4~0.6nm时,其中一个原子核对另一个原子核的外围电子产生吸引作用。其键能与两个原子之间距离的6次方成反比。是所有键合作用中最弱的一种,但非常普遍。
6.离子-偶极键及偶极-偶极键( ionic- dipole and dipole- dipoleinteractions) 当药物分子中存在电负性的N、O、S等原子时,由于这些原子的诱导,使分子中的电荷分布不均匀,形成偶极。该偶极与另一个带电离子形成相互吸引的作用,称为离子-偶极键;如果和另一个偶极产生相互静电作用,则称为偶极-偶极键。偶极作用常常发生在酰胺、酯、酰卤及羰基等化合物之间。
7.电荷转移复合物( charge-transfer complexes) 又称电荷迁移络合物,是电子相对丰富的分子与电子相对缺乏的分子之间通过电荷转移而形成的复合物。形成复合物的键既不同于离子键,又不同于共价键,键能较低。一些含多个杂原子的药物分子的电子云密度分布不均匀,有些原子周围的电子云密度较高,有些较低,所以这些分子既是电子给予体,又是电子接受体。电荷转移复合物的形成可增加药物的稳定性及溶解度,并增加药物与受体的结合。
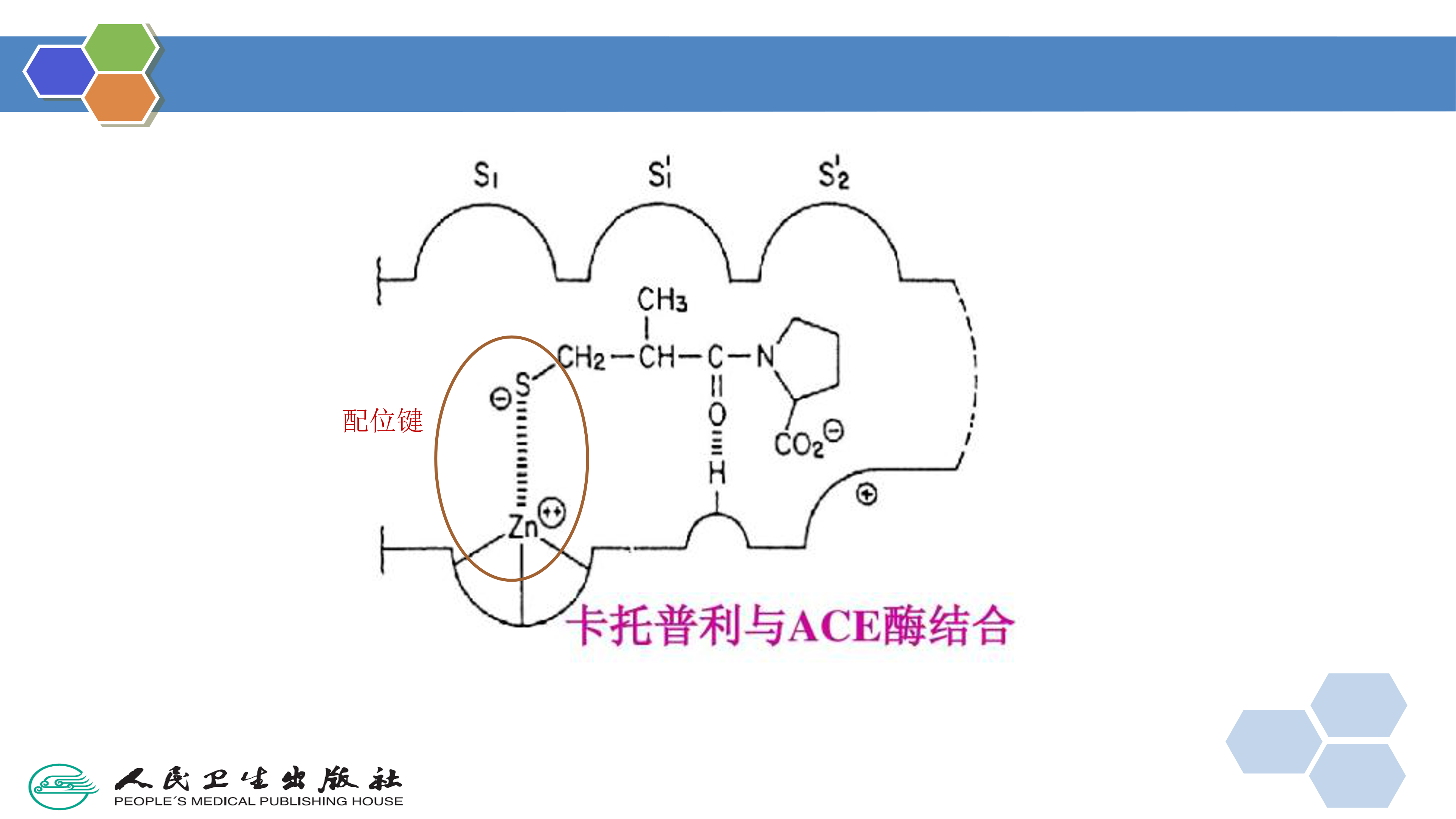
8.金属配合物( metal complexes) 金属配合物又称金属络合物,是由缺电子的金属离子和电荷密度相对丰富的配位体组成。一个金属离子可以与两个或两个以上的配位体形成配合物,如果是二齿以上的配位体,在形成配合物时往往形成环状化合物,通常有四、五和六元环,一般五元环以上较稳定。卡托普利( captopril)与血管紧张素转化酶的作用方式是巯基与酶的锌离子形成金属配合物而起作用,而依那普利则是通过羧基与酶的锌离子形成四面体过渡态而起作用,是一种类似金属配合物的结合方式。
(二)立体化学的作用
蛋白质和其他生物大分子是非对称的,药物与受体分子的识别和结合过程是在三维空间中发生的,立体互补性是实现该过程的重要因素。药物要与受体结合形成复合物,在立体结构上必须互相适应,即在立体结构上有互补性。药物与受体的互补性愈大,其作用愈强。互补性是结构特异性药物分子与受体识别的一个决定因素。它不仅包括药物与受体间电学特性的互补,表现为各种分子间力的形成,而且也包括空间结构的互补,也就是药物的构型与构象也应与受体互补。药物分子中某些有效官能团大小的改变或由不对称中心转换引起的基团空间排列或分子内偶极方向的改变,均能强烈影响药物和受体的结合,对药物活性也有明显影响。立体化学的作用主要介绍几何异构、光学异构和构象异构对药物活性的影响。
1.几何异构( geometric isomers) 当药物分子中含有双键,或有刚性或半刚性的环状结构时,可产生几何异构体。几何异构体的理化性质和生物活性都有较大的差异,如顺式己烯雌酚、反式己烯雌酚的例子(图2-5)。
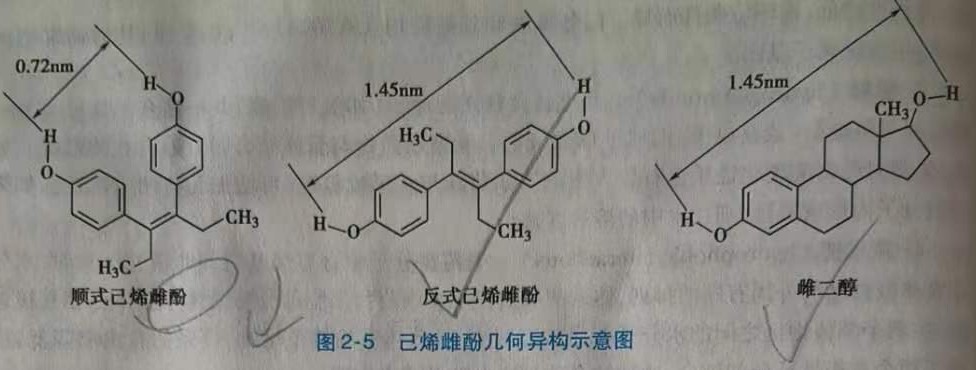
在雌激素的构效关系研究中,发现两个含氧官能团及氧原子间的距离对生理作用是必需的,而甾体母核对雌激素并非必需结构。人工合成的反式已烯雌酚中,两个羟基的距离是1.45nm,这与雌二醇两个羟基的距离近似,表现出较强的生理活性。顺式已烯雌酚羟基间距离为0.72nm,作用大大减弱。
1. 光学异构( optical isomers) 光学异构分子中存在手性中心,两个对映体互为实物和镜像,又称为对映异构体。对映异构体有着相同的物理性质和化学性质,但它们能使偏振光等量的向相反的方向旋转。生物体内的生物大分子都有特定的立体结构,如蛋白质都是由L-构型的α-氨基酸组成。因此,蛋白质(受体)也是手性物质。受体与两个对映异构体形成的复合物为非对映异构体,而不是对映异构体,因而它们具有不同的能量和化学性质,这意味着对映异构体药物与受体形成的药物-受体复合物的解离常数可能存在差异,也可能它们有不同的结合部位在生物学效应方面,对映异构体可能会显示下列不同情况:
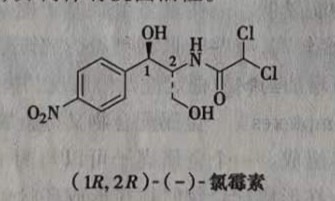
(1) 一个对映异构体有活性,另一个对映异构体没有活性。例如,氯霉素有两个手性碳,其四个异构体中只有(1R,2R)-(-)异构体有抗菌活性。
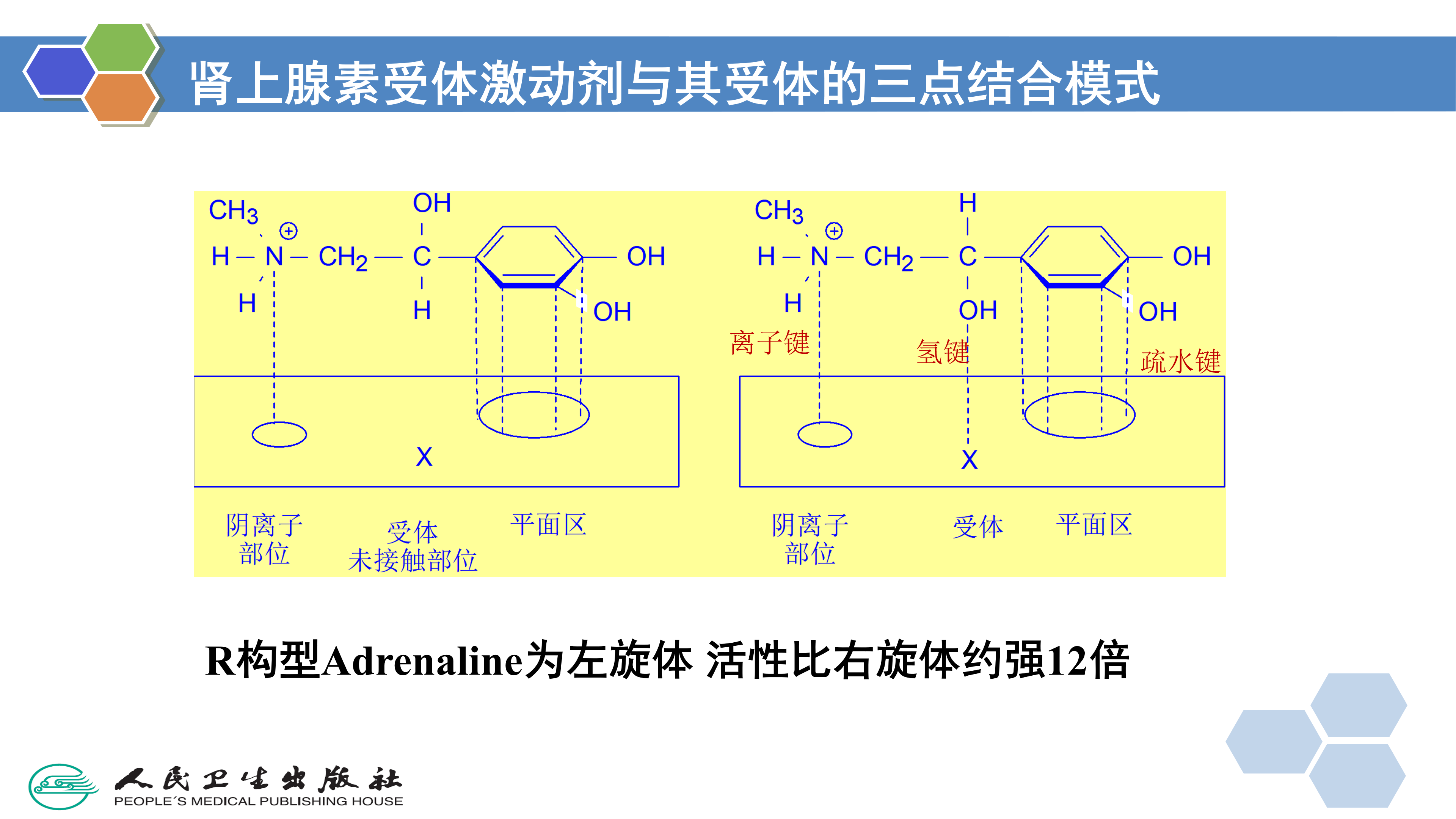
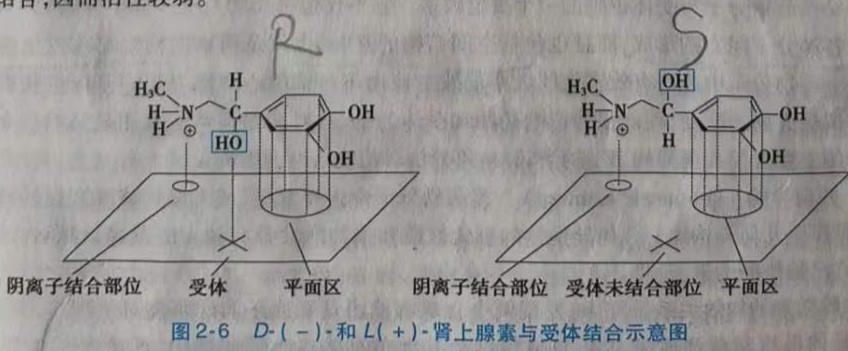
(2) 两个对映异构体均具有同类型的活性,但活性强度可能相同或不同。例如,左旋和右旋氯喹具有相同的抗疟活性;而在有的药物中,左旋体和右旋体的生物活性则不相同,例如,D-(-)-异丙肾上腺素的支气管扩张作用为L-(+)-异构体的异丙肾上腺素的800倍;D-(-)-去甲肾上腺素的支气管舒张作用为L-(+)-异构体的70倍;D-(-)-肾上腺素的血管收缩作用为L-(+)-肾上腺素的12~20倍,其生物活性的差异反映了光学异构体与受体结合时的立体选择性。一般认为,这类药物需要通过三点与受体结合,如图2-6中D-(-)-肾上腺素通过下列三个基团与受体在三点结合:氨基;苯环及其二个酚羟基;侧链上的醇羟基。而L-异构体只能有两点结合,因而活性较弱。
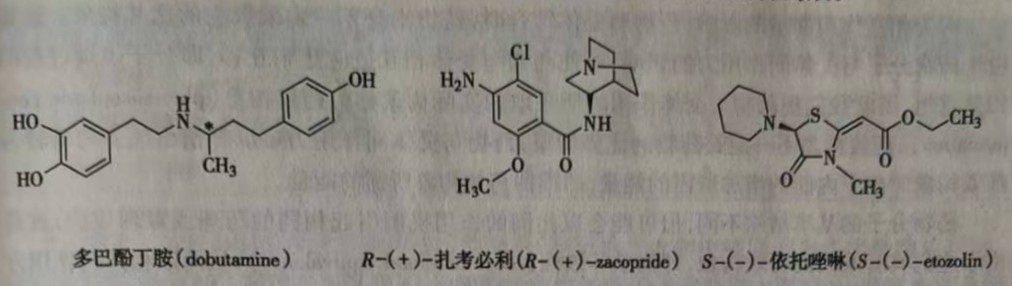
(3) 两个对映异构体显示相反的生物活性。例如,多巴酚丁胺( dobutamine)的左旋体可以激动α1受体,而其右旋体却拮抗α1受体。扎考必利( zacopride)是通过拮抗5-HT3,受体而起作用,为一类新型的镇吐药,深入的研究证明,扎考必利的R-异构体为5-HT3受体的拮抗剂,而S-异构体则为5HT3受体的激动剂。又如S-(-)-依托唑啉( etozolin)具有利尿作用,R-(+)-依托唑啉则有抗利尿作用。这类药物中,一个对映体能抵消另一对映体的部分药效。
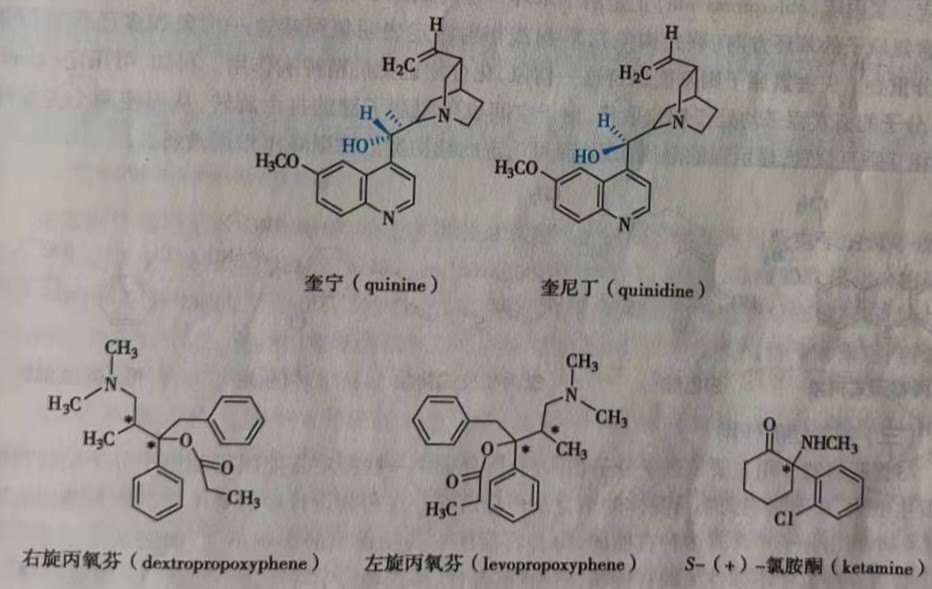
(4) 两个对映异构体显示不同类型的生物活性,例如,异构体奎宁( quinine)和奎尼丁( quinidine),奎宁主要用于解热和抗疟,而奎尼丁用于心房纤颤和心律不齐。右旋丙氧芬( dextroprop-oxyphene)是镇痛药,而其对映体,左旋丙氧芬( levopropoxyphene)为镇咳药。又如氯胺酮(ketamine),其右旋体(S-(+)-氯胺酮)是静脉麻醉药(具有催眠止痛作用),而其左旋体(异构体R-(-)-氯胺酮)则有产生噩梦幻觉的副作用。
由于对映异构体具有不同的三维结构,可能会产生不同的生物学反应,其原因可能是药物受体立体互补性(亲和力)的差别。如果含有光学异构体的药物存在立体选择性,由于生物膜、血浆和组织上的受体蛋白和酶,对药物进入机体后的吸收、分布和排泄过程均有立体选择性地优先通过与结合的情况,也可导致药效上的差别。如胃肠道对D-葡萄糖、L-氨基酸、L-甲氨蝶呤和L-(+)-维生素C等有立体选择性,可优先吸收,主动转运。在药物代谢过程中,代谢酶(多为光学活性的大分子)对药物的立体选择性可导致代谢差异,而出现代谢速率和药效、毒性的差异。因此,当考虑体内活性时,观察到的两个对映异构体的活性差异不完全取决于配体-受体匹配程度,有可能是体内药代动力学过程(吸收、分布、代谢和排泄)引起的。
3.构象异构( conformational isomers)由于碳碳单键的旋转或扭曲(键不断开)而引起的分子中原子或基团在空间的不同排列形式称为构象( conformation)。这种因单键的旋转或扭曲而产生的异构体称为构象异构体。由于旋转所需能量较小,一般低于5kcal/mol,理论上一个分子可以同时有无数构象式存在,但由于分子中较大基团(或原子)的立体障碍,一些需要克服的立体能垒大的构象存在的可能性较小,大多以分子势能最低的构象存在的可能性最大。我们称分子势能最低的构象为优势构象( preferential conformation),一般由X-射线结晶学测定的构象为优势构象。
因为相互作用能量的影响,药物和受体结合时,药物本身不一定采取它的优势构象。这是由于药物分子与受体间作用力的影响,可使药物与受体相互适应达到互补,即分子识别过程的构象重组,因此我们把药物与受体作用时所采取的实际构象称为药效构象( pharmacophoric conformation),药效构象不一定是药物的优势构象,药物与受体间作用力可以补偿由优势构象转为药效构象时分子内能的增加所需的能量,即维持药效构象所需的能量。
药物分子的基本结构不同,但可能会以相同的作用机制引起相同的药理或毒理效应,这是由于它们具有共同的药效构象,即构象等效性( conformational equivalence),从而以相同的作用方式与受体部位相互作用。构象等效性不仅存在于同系化合物和(或)同型化合物,而且在结构差异很大或化学类型不同的化合物之间,也可能有相同的药效构象。
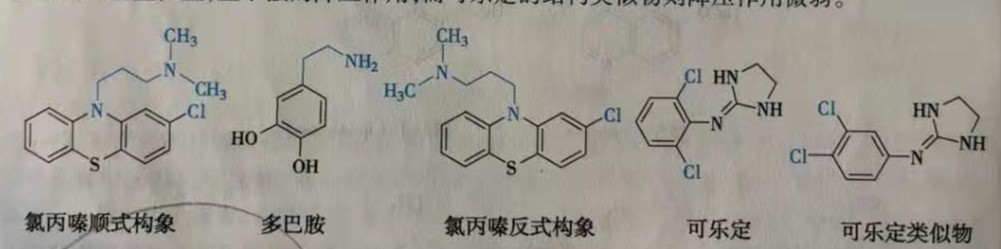
一些结构相似的药物,往往由于某个部位取代基的变化使化合物的构象发生了重大改变,进而使活性强弱发生改变,甚至显示出不同的生理活性。经典的抗精神病药物是多巴胺受体阻断剂,要求其构象和多巴胺( dopamine)有一定的构象相似性,才能和多巴胺受体更好的结合发挥效应。氯丙嗪( chlorpromazine)正是由于苯环2位的氯原子引起了分子的不对称性,使侧链倾斜于含氯原子的苯环方向(顺式构象),X-射线衍射测定表明氯丙嗪这一构象和多巴胺的构象能部分重叠。失去氯原子则不能保持这一构象,化合物也无抗精神病作用。再如,可乐定( clonidine)分子的卤素原子均处于邻位取代,由于空间位阻限制了键的自由旋转,从而使两个芳香环保持相互垂直位置,显示强的降压作用;而可乐定的结构类似物则降压作用微弱。
(三)官能团的作用
尽管药物的作用主要依赖于分子整体性,但分子中一些特定官能团可使整个分子结构和性质发生变化,从而影响药物与受体的结合及药理活性。在药物设计中需要考虑这些官能团的影响。一个药物分子中常有多种官能团,每种官能团对药物性质的影响不同,如诺氟沙星分子结构中含有6种以上不同性质的官能团,对活性、毒性、药代动力学等产生不同影响及综合影响。
1.烷基 烷基链的改变,例如增加或缩短烷基链、形成支链或改变环的大小,都能深刻影响分子的药理活性和强度。烷基链上仅改变一个-CH2-的长度,或增加一个支链,都能改变分子的亲脂性,从而改变其吸收、分布和排泄。如果烷基链直接参与受体的相互作用,那么碳链长度或支链的变化,能影响与受体的结合。如果在一个烷基链的关键位置引入一个支链,将使较易改变构象的分子的构象不易改变。构象的变化能影响分子中官能团的空间位置,从而能影响与受体的结合。
烷基的给电子效应会影响到化合物中电子的分布,因而影响其解离度,进而影响生物活性。例如磺胺嘧啶,由于嘧啶环的吸电子效应,使磺酰氨基有较大的解离度,磺胺甲嘧啶和磺胺二甲嘧啶,由于嘧啶环上一个甲基和两个甲基的给电子效应,同时甲基的存在阻碍了分子间氢键和偶极-偶极相互作用,减少了分子间的缔合,从而使解离度降低,见表2-2。
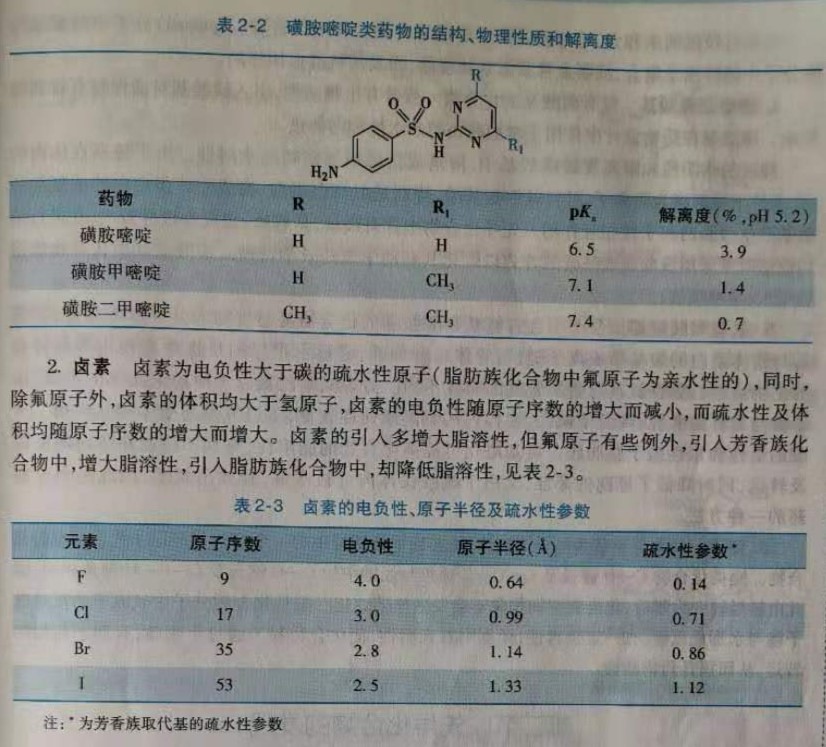
卤素取代氢原子形成碳-卤键,由于卤素的电负性大于碳原子而显示出吸电子的诱导效应。又由于卤原子有三对未共享电子,可以与Π体系产生共轭效应。因此,以卤素取代化合物碳原子上的氢时,分子中的电子分布将发生变化,如果化合物的生物活性与电子分布情况有关时,则生物活性将发生变化。例如吩噻嗪类药物,2位没有取代基时,几乎没有抗精神病作用;当2位引入氯原子或三氟甲基时,活性增强。
氟原子体积较小,范德华半径接近于氢原子,且C—F键(键能114kcal/mol)强于C—H键(93kcal/mol),常常连接于分子易受代谢攻击的部位,以阻止代谢作用。
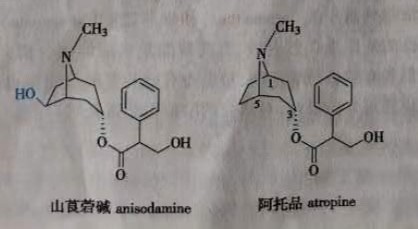
3.羟基与巯基 由于羟基中的氧原子电负性大于碳原子,且氧原子有两对未共享电子,在脂肪链上羟基表现为吸电子的诱导效应,在芳环上的羟基由于p-Π共轭效应而成为供电基团,使化合物的理化性质发生了较大变化。引入醇羟基或酚羟基会改变分子的分配系数,使分子的亲水性增加,从而提高其水溶性。用羟基替换氢原子会在很大程度上影响生物活性。例如,山莨菪碱( anisodamine)在C-6上比阿托品( atropine)多一个羟基其脂溶性降低,对中枢的作用也随之降低。
巯基有较强的亲和力,可与金属离子形成络合物。如卡托普利( captopril)分子中的巯基与酶分子中的锌离子络合,抑制血管紧张素转移酶,而发挥抗高血压作用。
4.磺酸基和羧基 仅有磺酸基的化合物一般没有生物活性,引入磺酸基对活性没有特别的影响。磺酸基在药物设计中常用于增加药物的亲水性和溶解度。
羧酸的水溶性和解离度较磺酸基小,羧基成盐可增加药物的水溶性。由于羧基在体内的pH条件下可解离为阴离子,可与碱性氨基酸,特别是血清白蛋白、酶或受体蛋白中的赖氨酸的氨基产生很强的离子性相互作用。先导化合物中含有羧基,易解离,表现为极性较大,在进行结构改造时常采用成酯或成酰胺的方式以优化其药动学或药效学特性。羧酸成酯后化合物脂溶性增大,易被吸收。
5.氨基和酰胺基 分子中含有氨基和酰胺基的化合物易与生物大分子形成氢键;氨基易与受体蛋白的羧基形成离子键,与受体结合加强,常显示很好的活性并表现出多种特有的生物活性。芳香氨基与脂肪氨基的碱性不同。芳香氨基的氮原子中的未共享电子对,由于参与苯环的共轭,降低了碱性,在体内的解离倾向性较低,多以氢键与受体相互作用。芳胺的活性和毒性强于脂肪胺。氨基酰化可提高化合物的脂溶性,有利于药物在体内的吸收及转运,同时降低了原药的毒性,又由于酰胺在体内可被水解,释放出氨基,因此是做成前药的一种方法。
6.醚键 氧和亚甲基为电子等排体,醚相当于将链烃中的一个CH2用氧原子代替而成的化合物。醚类化合物C—0键长及C—0—C键角与烃键中的C—C键长及C—C—C键角相近,因此由链烃转变为醚后,化合物空间构象不会发生显著变化。醚类化合物分子中氧原子的孤对电子能与水形成氢键,有一定亲水性,烃基则有亲脂性,使化合物易于通过生物膜,有利于药物的转运,从而提升药物活性。