









第三节 先导化合物的优化
Optimization of Lead Compound
在新药研究过程中,发现的先导化合物可能存在某些缺陷,如活性不够高,化学结构不稳定,毒性较大,选择性不高,药代动力学性质不合理等,需要对先导化合物进行结构修饰或改造,使之成为理想的药物,这一过程称为先导化合物的优化。
对先导化合物的优化有多种方法,大体可分为两大类:传统的药物化学方法和现代的方法。现代的方法指利用计算机辅助药物设计的手段和利用定量构效关系的方法,这些新方法在药物设计中发挥的作用越来越重要,是发现和优化先导化合物的常用手段,这部分内容在第四节和第五节介绍。以下介绍对先导化合物进行优化的传统的药物化学方法。
一、生物电子等排替换(Bioisosteric Replacement)
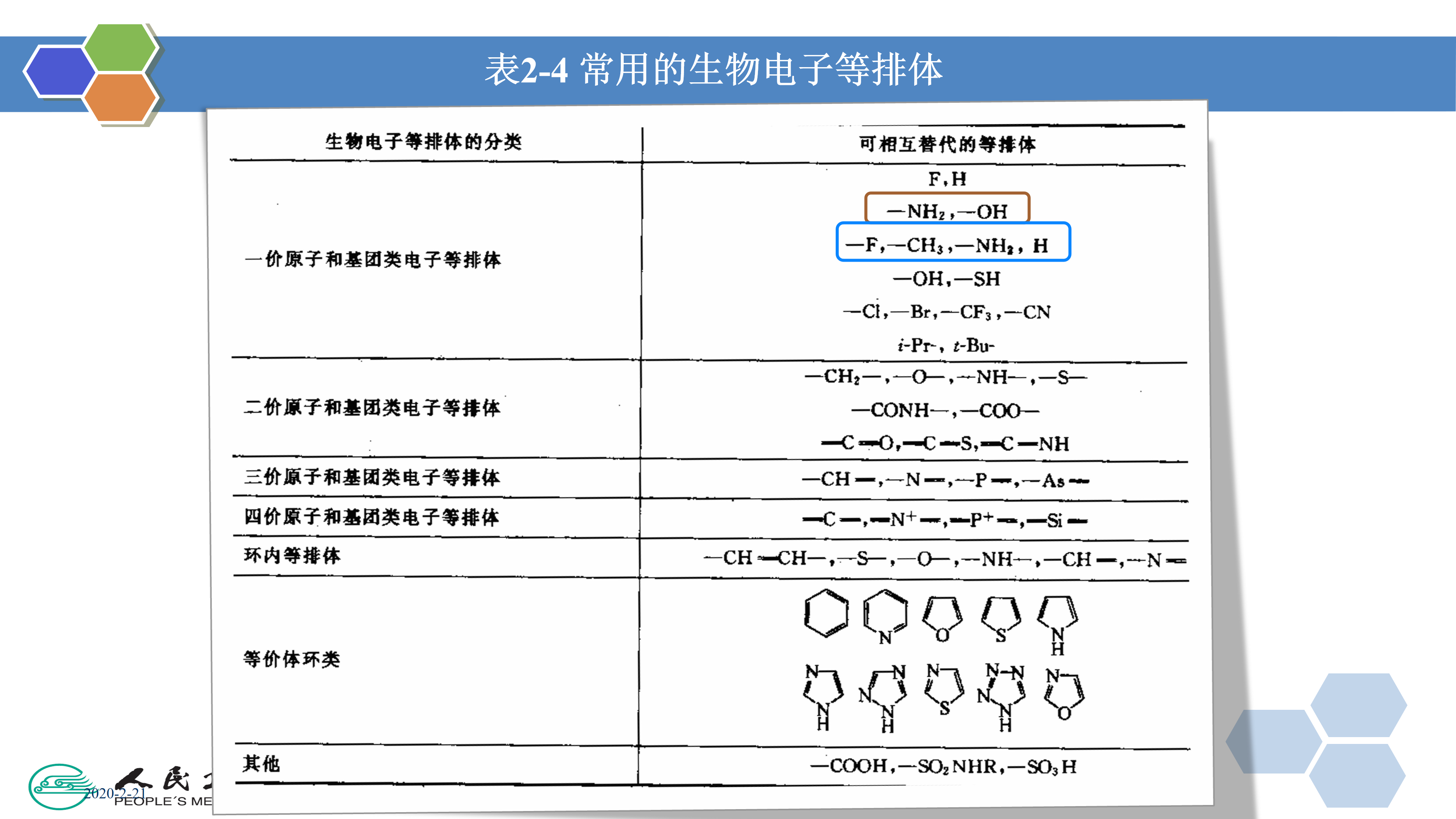
生物电子等排体(bioisostere)是由化学电子等排体( chemical isostere)演化而来。1919年Langmuir首先提出化学电子等排体的概念,最初定义是电子等排体为具有相同电子数和电子分布的原子、基团或分子,例如元素周期表中同一族的原子是电子等排体,重氮甲烷和乙烯酮是电子等排体,N2O和CO2是电子等排体。1925年 Grimm提出了氢化物置换规则,即将氢原子加到某一原子上形成的基团具有高一个原子序数的原子的性质。即元素周期表中C、N、O等原子每结合一个氢原子,即与下一列原子或基团互为电子等排体,如—0—、—NH—和—CH2—互为电子等排体,—F、—OH、—NH2和一CH3互为电子等排体,它们价电子数相同而原子数不同。后来, Friedman提出了生物电子等排体的概念,用来描述具有相同类型生物活性的电子等排体,而且, Friedman将具有相反生物活性的电子等排体(如拮抗剂)也定义为生物电子等排体,因为它们通常作用于相同的结合位点上(如对氨基苯甲酸和对氨基苯磺酰胺)。因此,生物电子等排体定义为:是指那些具有相似的物理和化学性质,并能产生相似的或相反(拮抗)的生物活性的分子或基团。 Burger进一步扩大了这个定义:生物电子等排体是具有相似的分子形状和体积、相似的电荷分布,并由此表现出相似的物理性质(如疏水性),对同一靶标产生相似或拮抗的生物活性的分子或基团。
生物电子等排体可分为经典和非经典的生物电子等排体两类。经典的生物电子等排体包括外层价电子相同的原子或基团、元素周期表中同一主族的元素以及环等价体。非经典的生物电子等排体指具有相似的空间排列、电性或其他性质的分子或基团,相互替换会产生相似或相反的生物活性。
药物设计中常用的生物电子等排体见表2-4。
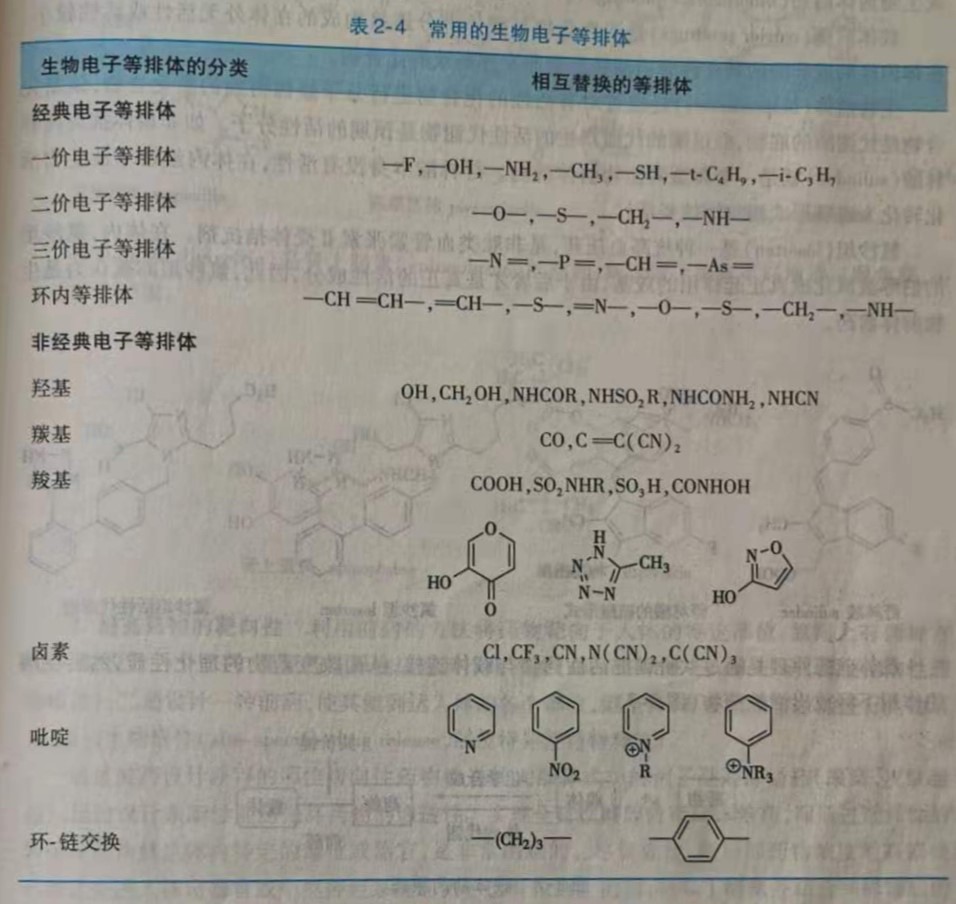
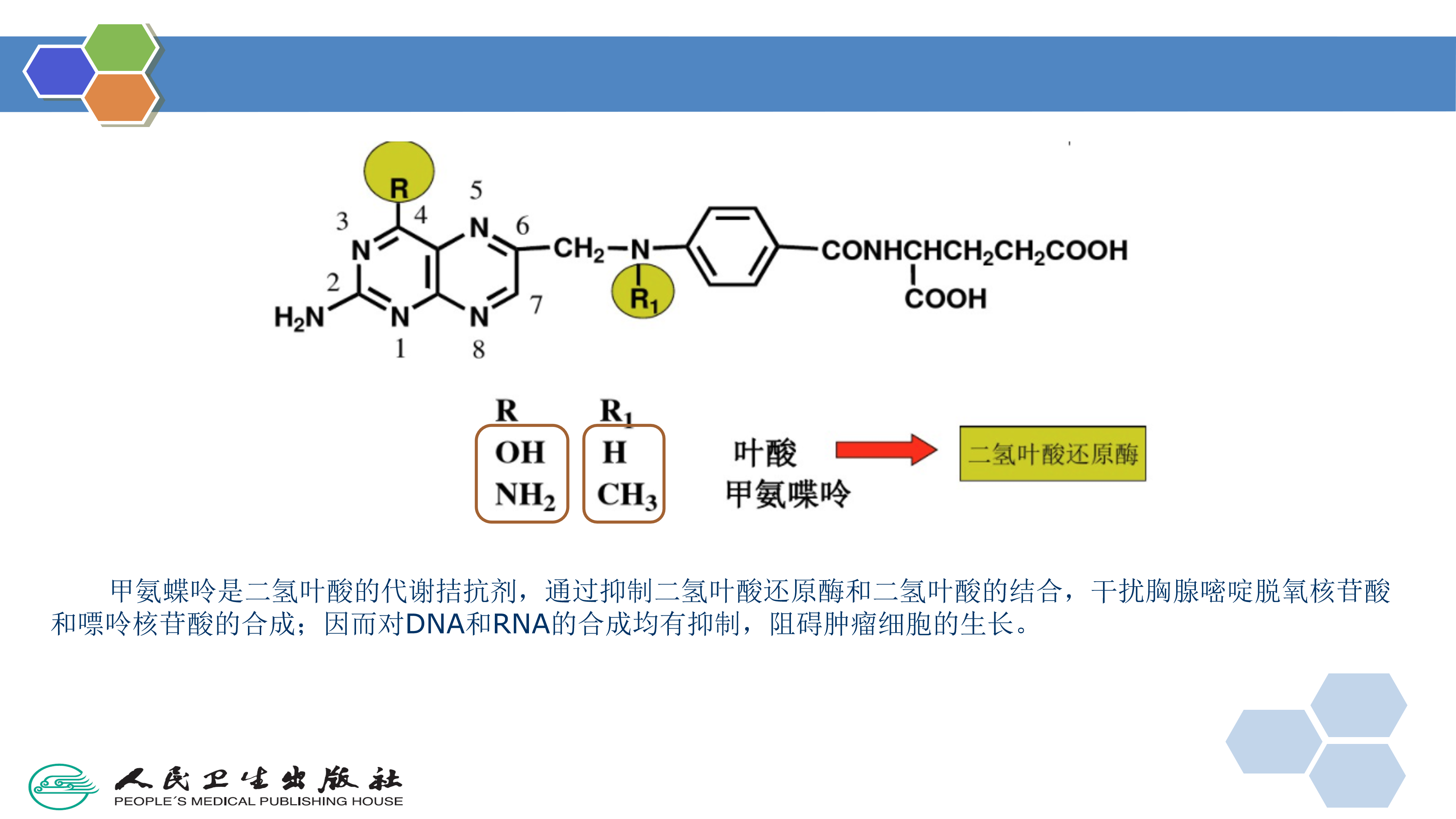
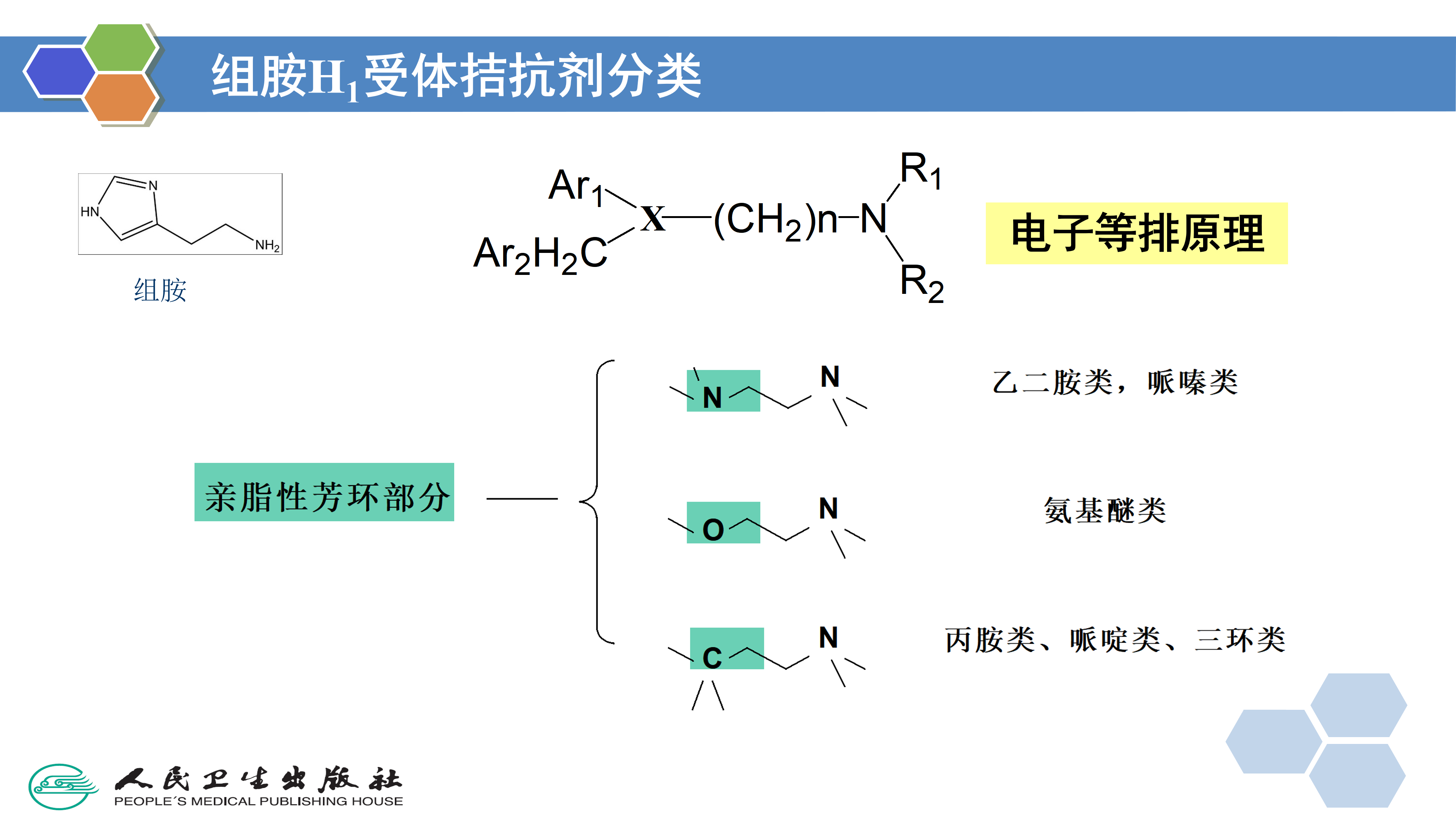
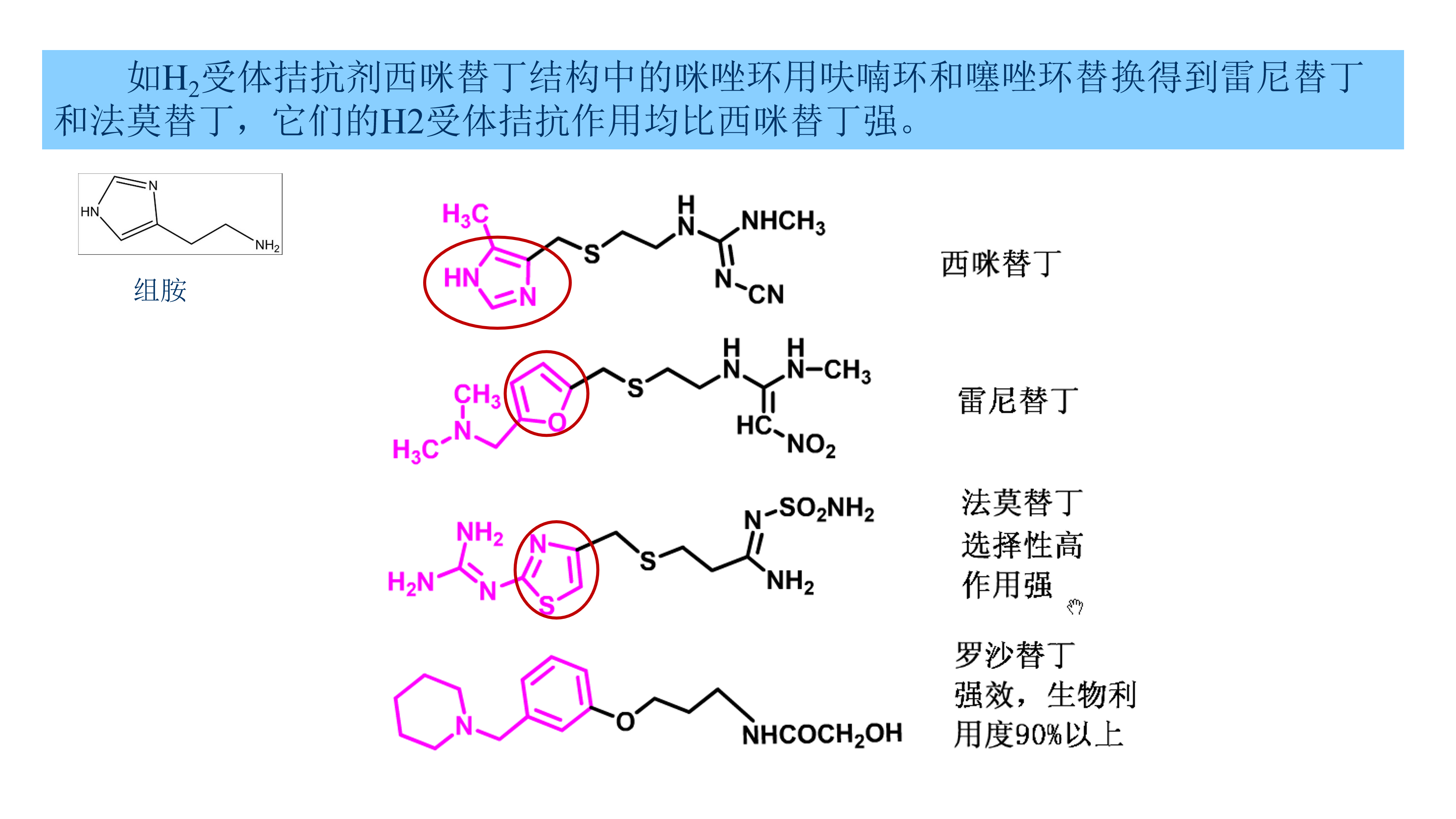
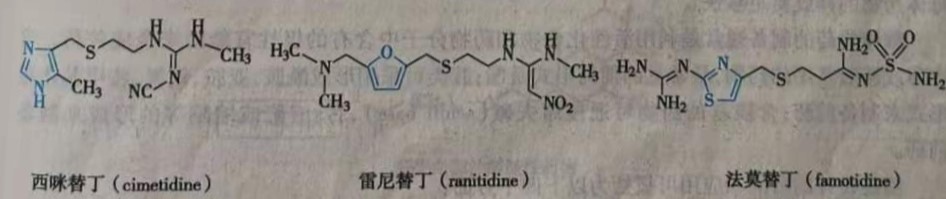
利用生物电子等排体对先导化合物中的某一个基团逐个进行替换得到一系列的新化合物,是药物化学家设计研究药物的经典方法,有许多成功例子。例如将H2受体拮抗剂西咪替丁(cimetidine)结构中的咪唑环用呋喃环和噻唑环替换得到雷尼替丁( ranitidine)和法莫替丁( famotidine),它们的H2受体拮抗作用均比西咪替丁强。
二、前药设计(Prodrug Design)
前药( prodrug)的概念最初由 Albert提出,用来描述经过生物转化后才显示药理作用的任何化合物。这一广泛定义包括偶然发现的前药、活性代谢物和为改善活性化合物的药代动力学性质而制备的化合物。基于这一观点, Harper提出了药物潜伏化的概念来表达前药设计的意图。药物潜伏化( drug latentiation)是通过对生物活性化合物的化学修饰形成新的化合物,该新化合物在体内酶的作用下释放出母体药物( parent drug)而发挥作用。虽然这个概念广泛,但通过对大量专业文献调研,可将前药分为两大类:载体前药( carrier prodrugs))和生物前体( bioprecursors)或生物前体前药( bioprecursor prodrugs)。
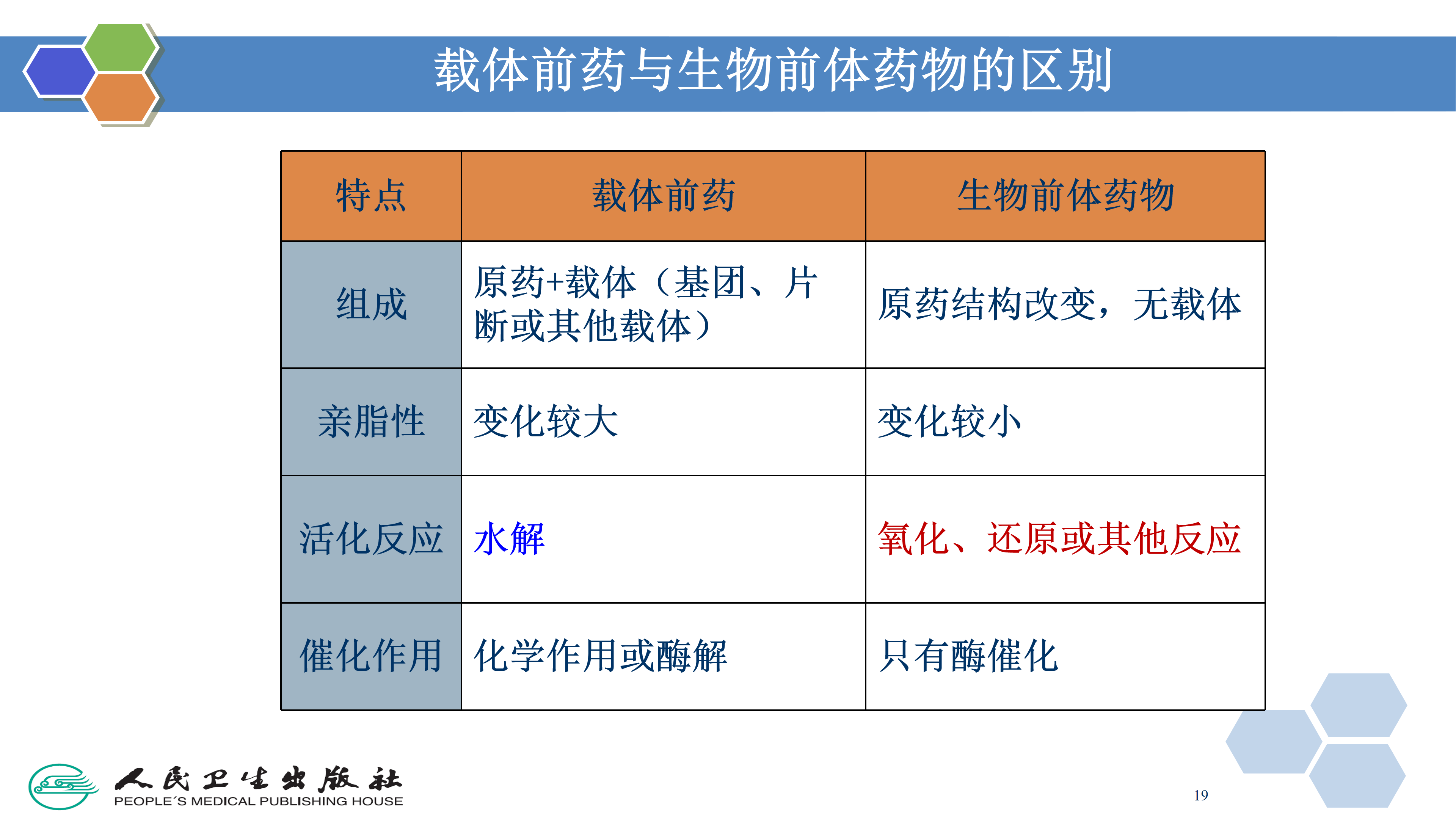
载体前药( carrierprodrugs)是活性药物与载体部分连接构成的在体外无活性或活性较小,在体内经酶或非酶的转化释放出活性药物而发挥药效的化合物。
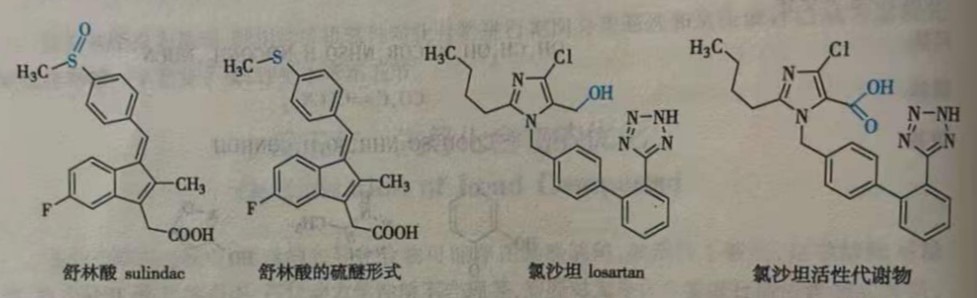
生物前体(bioprecursors)是通过对有活性的化合物进行分子修饰得到的新化合物,该新化合物是代谢酶的底物,经过酶的代谢产生的活性代谢物是预期的活性分子。如非甾体抗炎药舒林酸( sulindac)就是一个典型的生物前体前药。舒林酸本身没有活性,在体内经还原性生物活化转化为硫醚形式而发挥抗炎活性。
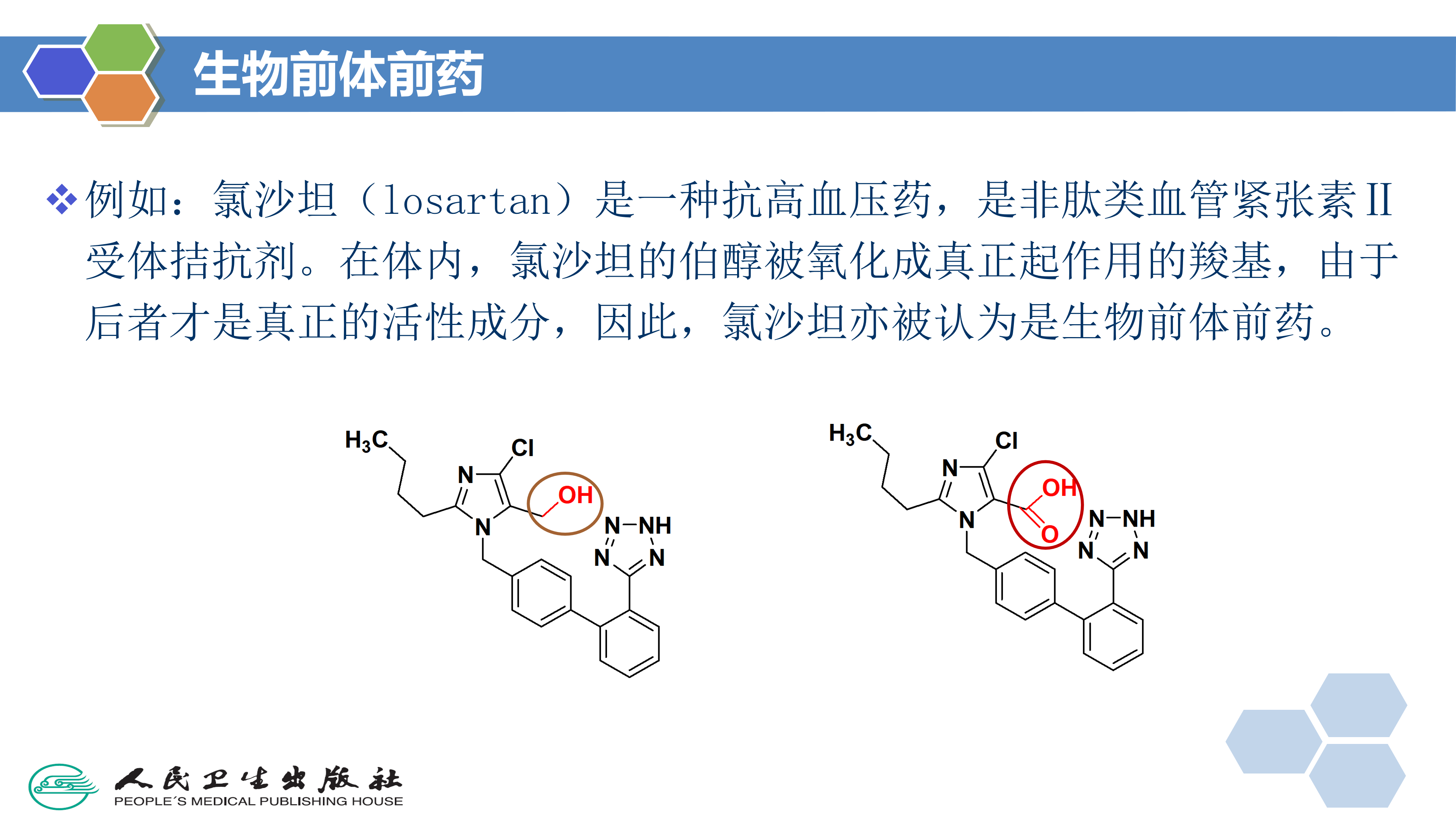
氯沙坦(losartan)是一种抗高血压药,是非肽类血管紧张素Ⅱ受体拮抗剂。在体内,氯沙坦的伯醇被氧化成真正起作用的羧基,由于后者才是真正的活性成分,因此,氯沙坦亦被认为是生物前体前药。
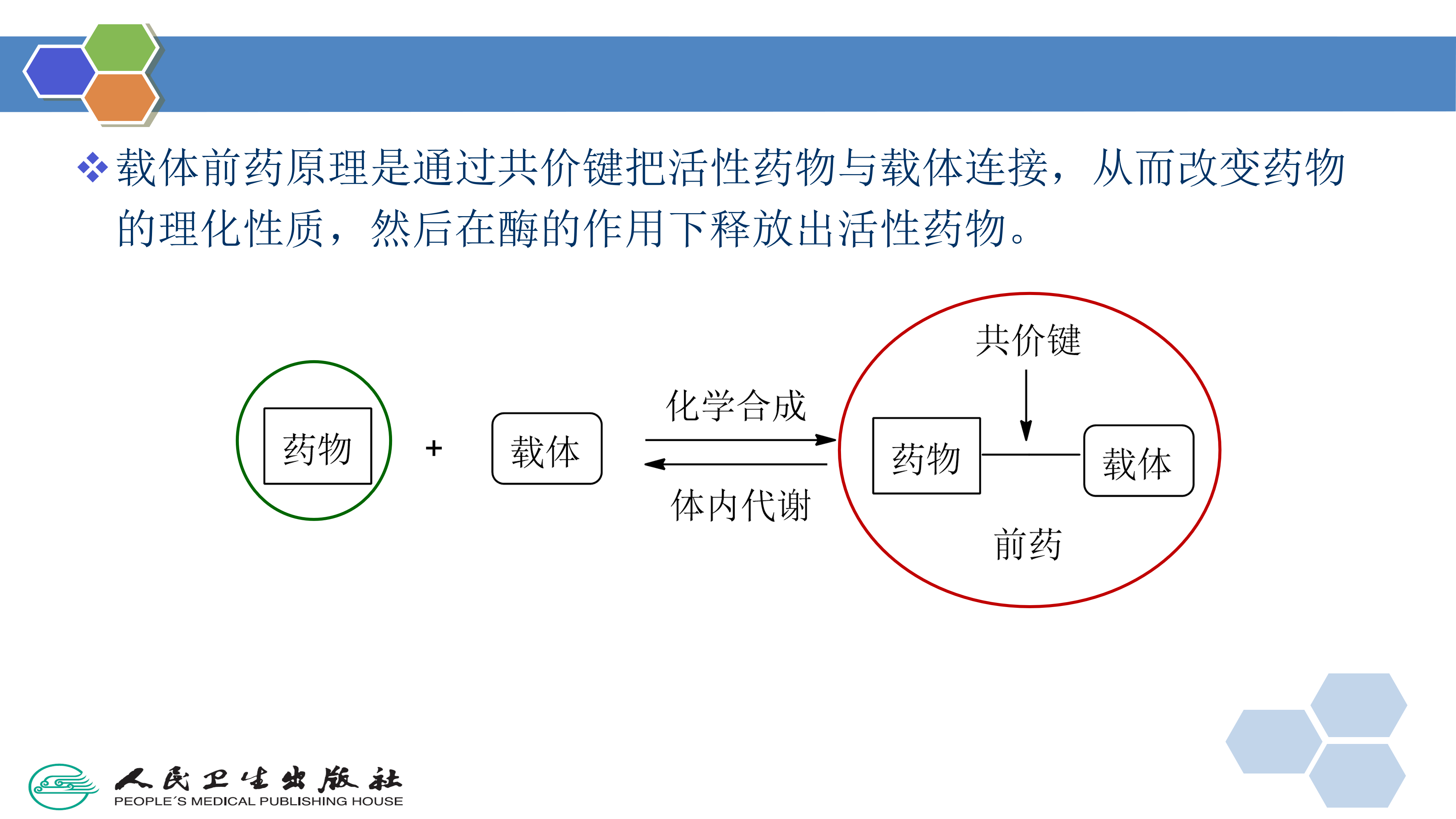
载体前药原理是通过共价键把活性药物与载体连接,从而改变药物的理化性质,然后在酶的作用下释放出活性药物(图2-7)。
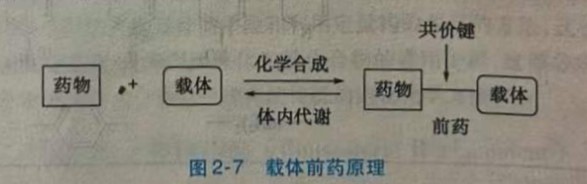
一个设计优良的载体前药应符合以下标准:前药应无活性或活性低于母体药物;药物与载体一般以共价键连接;药物与载体间的连接在体内一定能断开;前药以及在体内释放出来的载必须是无毒的;为保证在作用部位达到有效浓度以及尽量减少前药的直接代谢或逐渐失活,母体药物的释放要足够快。
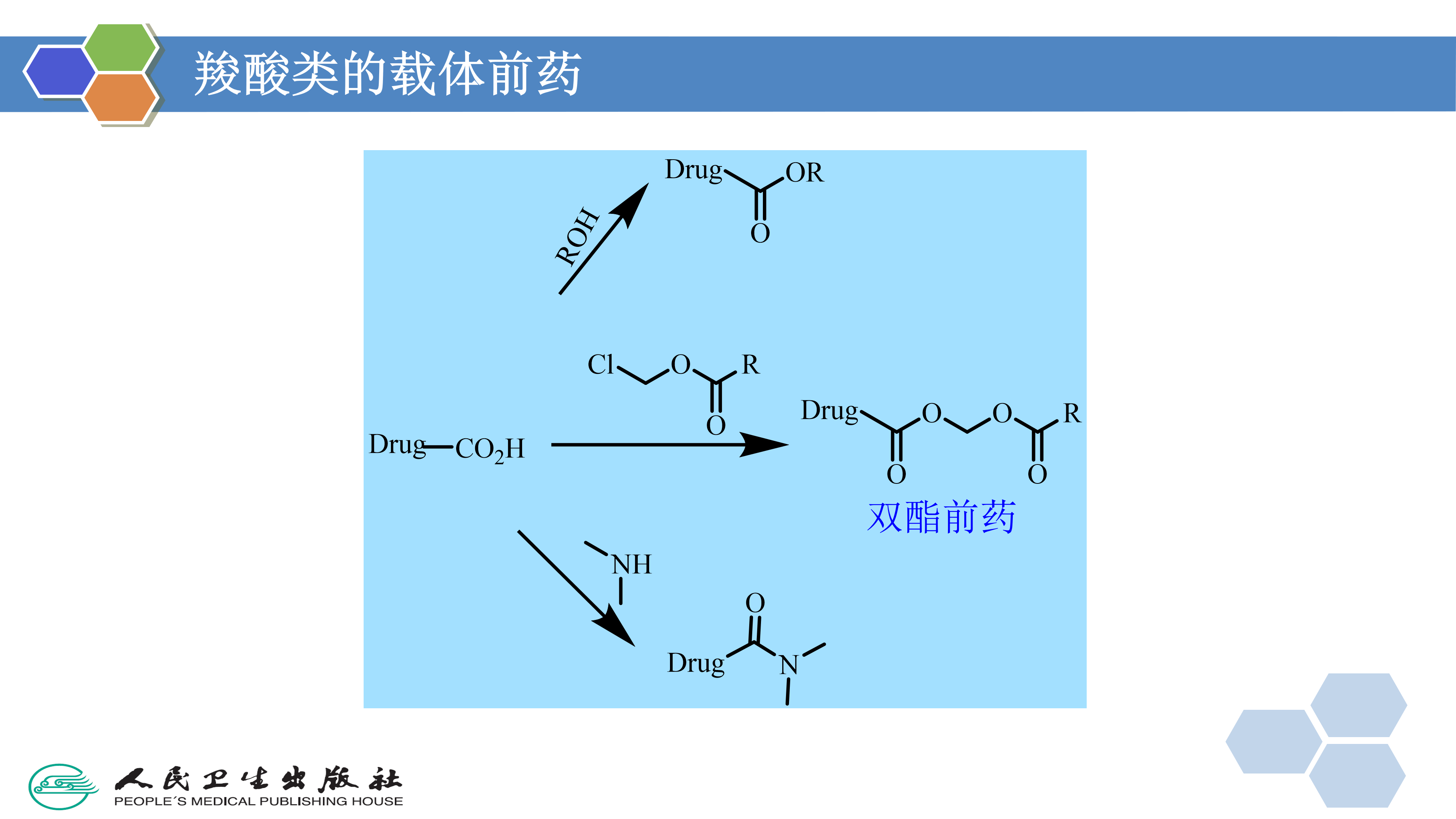
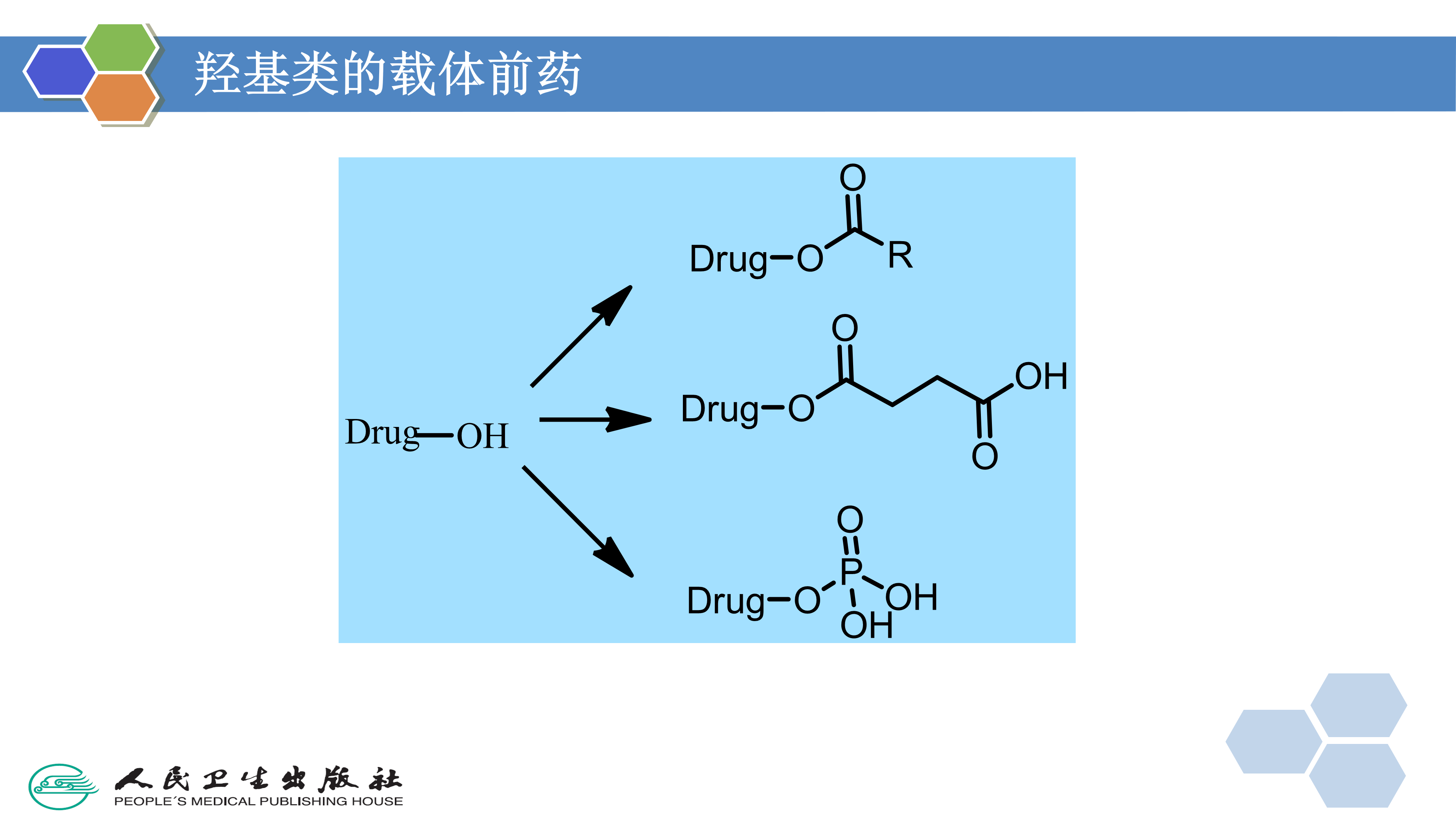
载体前药的制备通常是利用活性化合物和药物分子中含有的极性官能团来合成前药。含有醇或羧酸基团的药物,最常见的前药形式是酯;胺类可采用形成酰胺、亚胺、偶氮、胺甲基化等形式来制备前药;含羰基的药物可通过席夫碱( schiff base)、肟、缩醛或缩酮等的形成来制备前药。
前药设计的目的和应用可概括为以下四个方面:
1. 提高生物利用度和生物膜通透性
药物的生物膜通透性主要取决于其理化性质,特别是其脂水分配系数,因此,将药物与亲脂性载体连接可改善其生物利用度,使其更容易通过被动扩散跨过细胞膜。口服吸收、直肠给药、眼部给药和皮肤给药这几种给药方式的药物吸收都依赖于被动扩散。
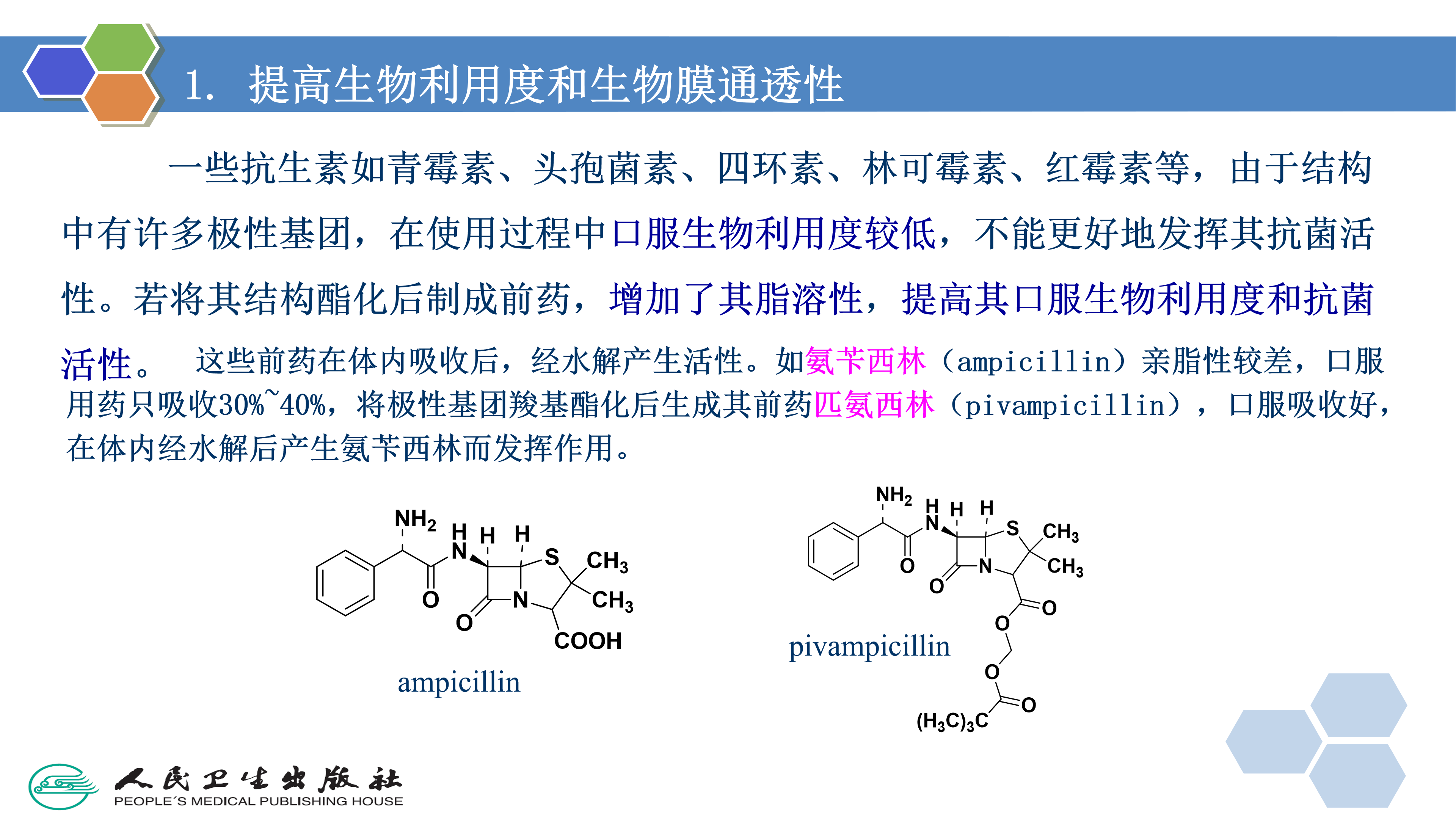
氨苄西林( ampicillin)口服吸收较差(大约为40%),将其羧基酯化形成易被酶裂解的酯—匹氨西林( pivampicillin)和巴氨西林( bacampicillin),口服时几乎定量吸收,这两种前药的给药剂量较氨苄西林低,安全有效。
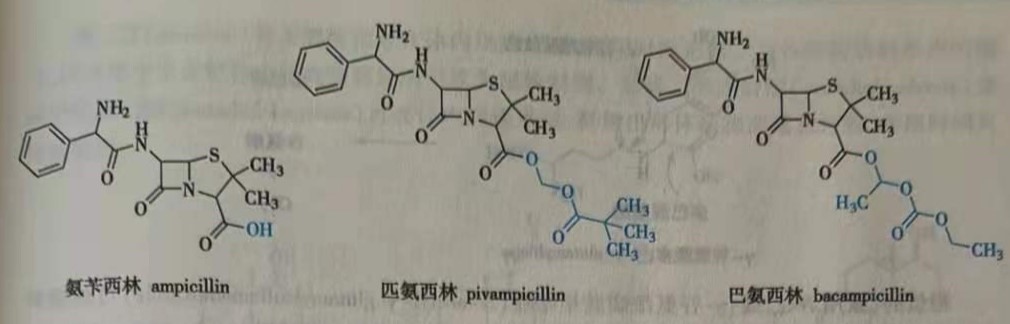
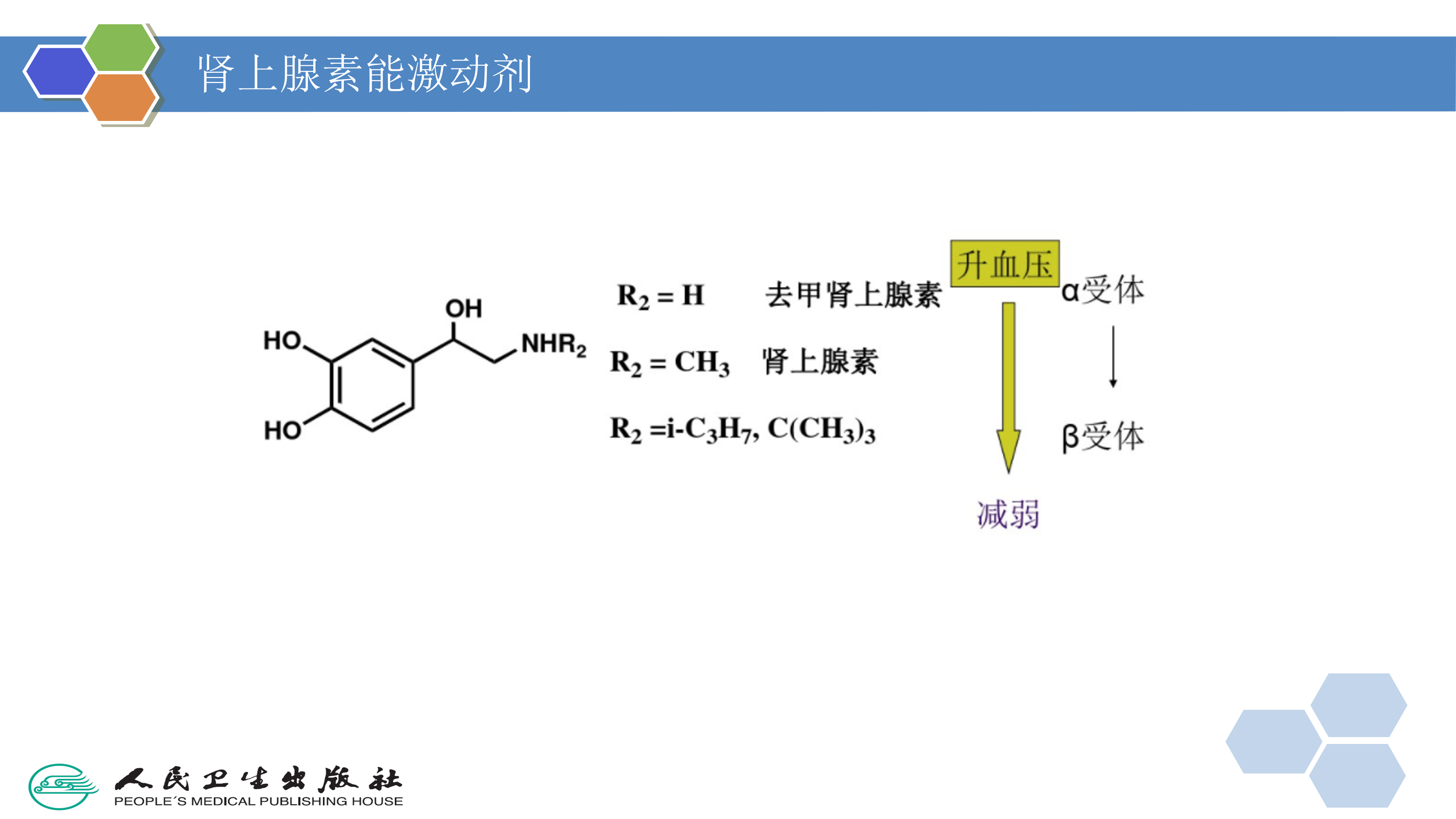
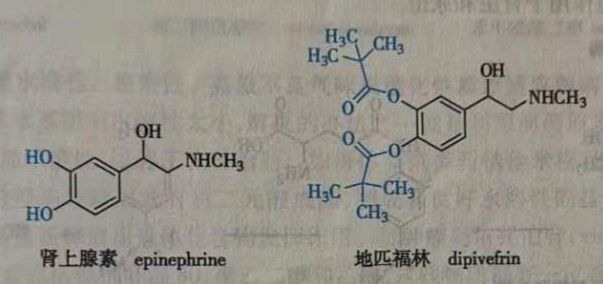
地匹福林( dipivefrin)是肾上腺素( epinephrine)的前药,能比肾上腺素更好地透过眼角膜,用于治疗青光眼。
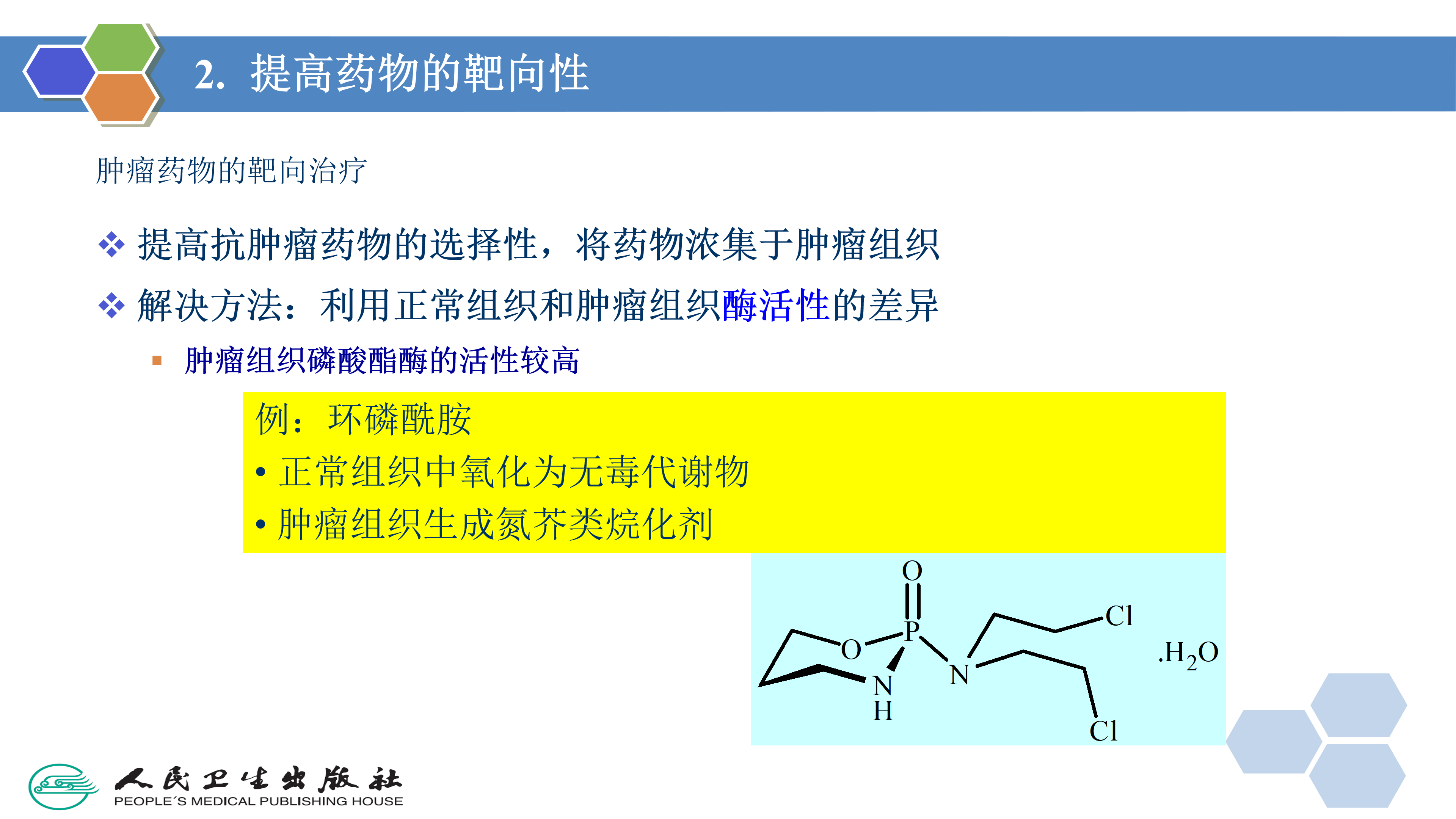
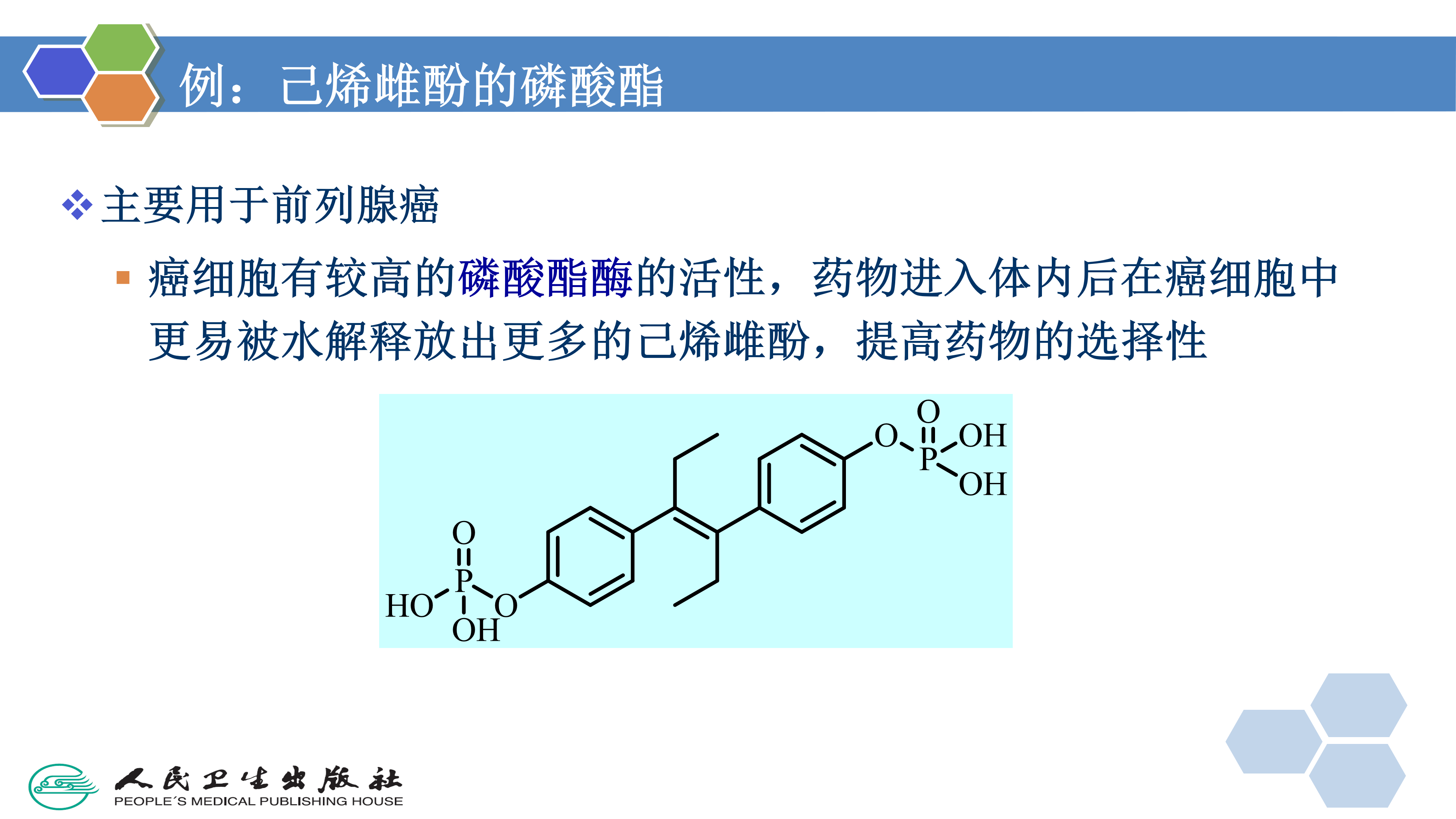
2. 提高药物的靶向性
利用前药的方法将药物靶向于人体的特定部位,原则上有两种方法,一是设计一个前药,使原药选择性运输到作用部位( site-directed drug delivery),部位指向性药物输送);二是设计一种前药,使其能到达人体的各个部位,但是,只有在靶器官才能进行生物活化,显示生物活性(site- specific drug release,部位特异性药物释放)。
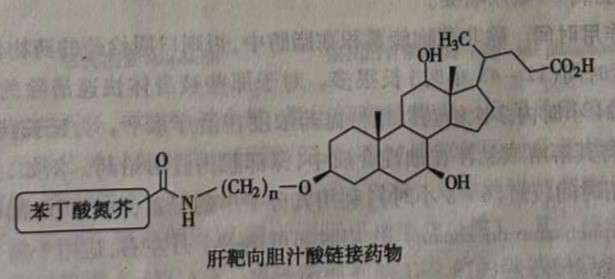
通过前药设计获得的部位指向性药物输送的大部分成功的例子是局部给药(眼睛、皮肤给药),通过设计亲脂性前药提高药物的通透性。实现全身性的部位指向性给药,即通过选择性的转运使药物到达体内特定的部位或器官,是非常困难的。尽管如此,使局部药物浓度增高或使药物优先进入指定器官或中枢神经系统的例子已有报道。例如,将苯丁酸氮芥结合到修饰后的胆汁酸上使其具有肝靶向性,其合理的解释是内源性的胆汁酸转运系统能够识别胆汁酸连接的药物。
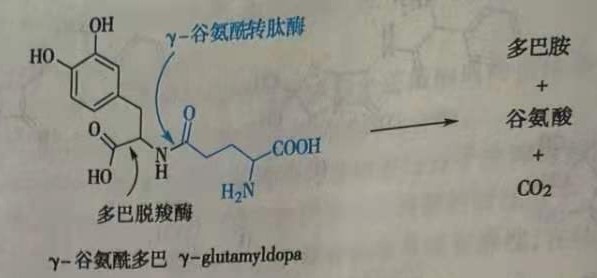
设计部位特异性药物释放的前药,总体的策略是发现一种在靶器官浓度高、而在其他器官几乎没有的酶,根据酶对底物特有的选择性裂解性质来设计合适的前药。例如,服用γ-谷氨酰多巴( γ- glutamyldopa)可选择性扩张肾血管。γ-谷氨酰多巴是L-多巴(L-dopa)的前药,在肾脏蓄积并被选择性代谢。在肾脏中存在的两种高浓度的酶γ-谷氨酰转肽酶(γ-glutamyl transpeptidase)和L-芳香氨基酸脱酸酶( L-aromatic amino aciddecarboxylase)的连续作用下,γ-谷氨酰多巴在肾脏释放出多巴胺( dopamine),从而产生特异性的肾脏组织血管舒张作用。
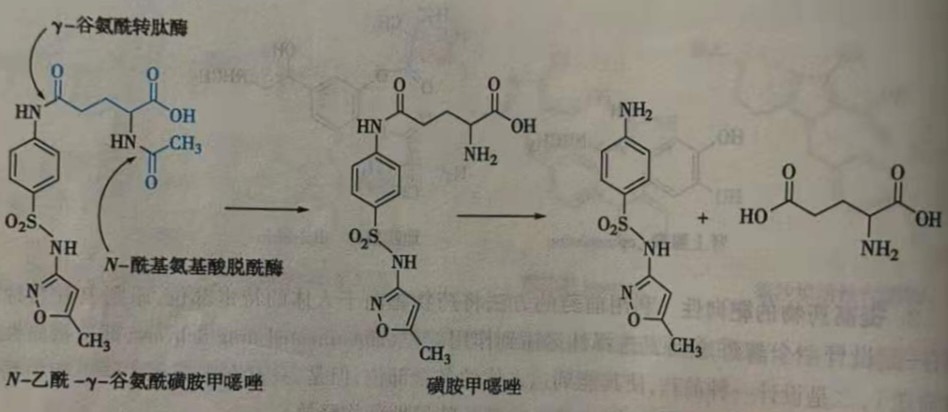
相似的,服用N-乙酰-γ-谷氨酰磺胺甲噁唑(N-acetyl- γ--glutamylsulfamethoxazole)可使磺胺甲噁唑( sulfamethoxazole)选择性地蓄积在肾脏。N-酰基氨基酸脱酰酶(N- acylamino acid deacylase)在肾脏中的浓度也很高,在γ-谷氨酰转肽酶和N-酰基氨基酸脱酰酶作用下释放出磺胺甲噁唑,使其选择性地作用于肾脏和尿道。
结肠微生物群落所特有的葡萄糖苷酶活性已被用于选择性地裂解甾体类前药治疗肠道炎症。前药地塞米松21-β-D-葡萄糖苷( dexamethasone2l-β-D- glucoside)口服后约有60%的地塞米松到达盲肠,如果口服母体药物地塞米松,大部分在小肠被吸收,只有不到1%到达盲肠。在各种肿瘤组织中,尿苷磷酸化酶( uridine phosphorylase)的活性显著高于周围正常组织,这一发现在促进了5-氟尿嘧啶前药的研究。5’-脱氧-5-氟尿嘧啶(5' -deoxy-5-fluorouracil)显示出了很高的抗肿瘤活性和较小的毒性。之所以具有良好的治疗指数,是因为肿瘤细胞中尿苷磷酸化酶选择性地活化前药5′-脱氧-5-氟尿嘧啶。
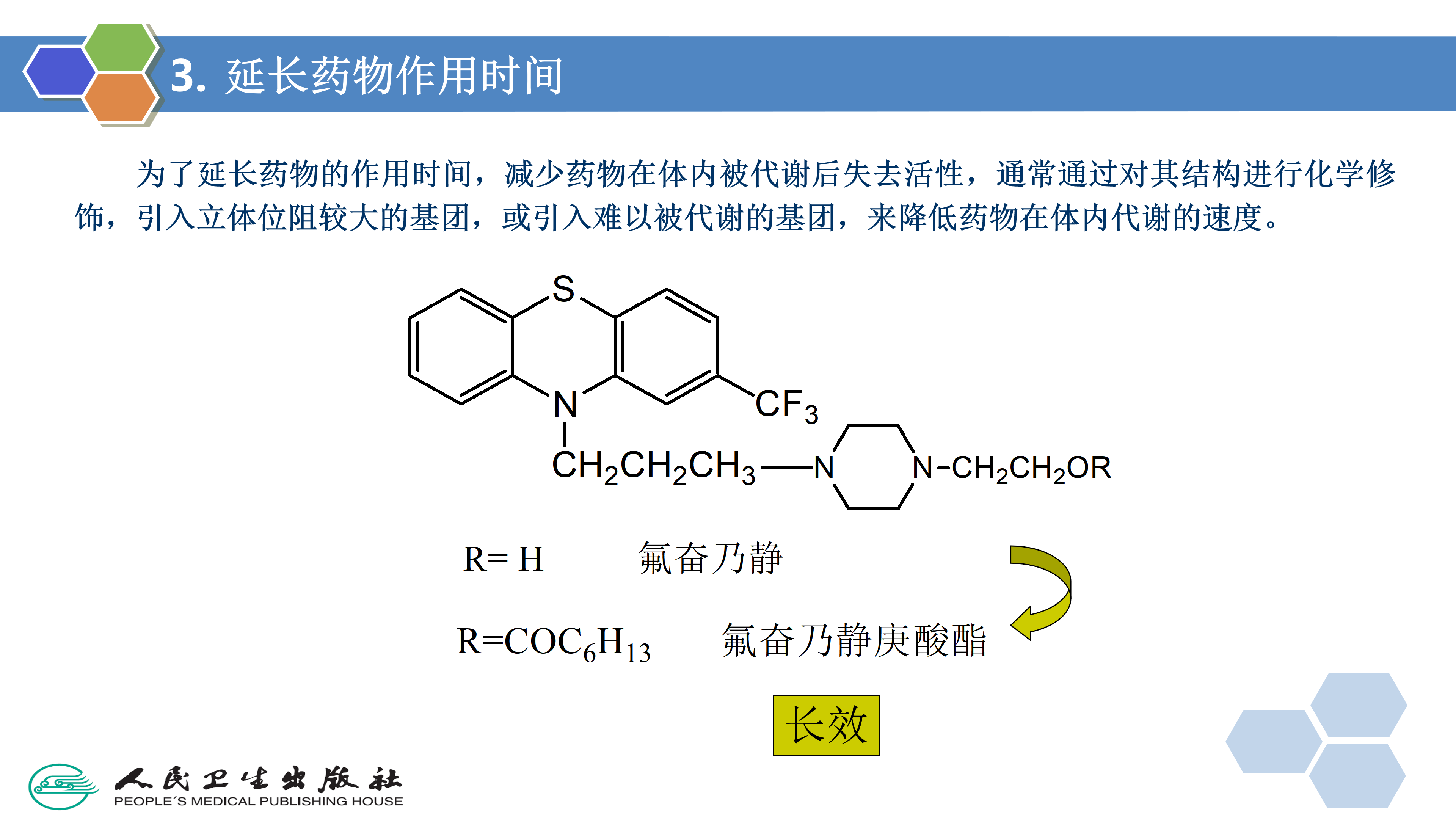
3. 延长药物作用时间
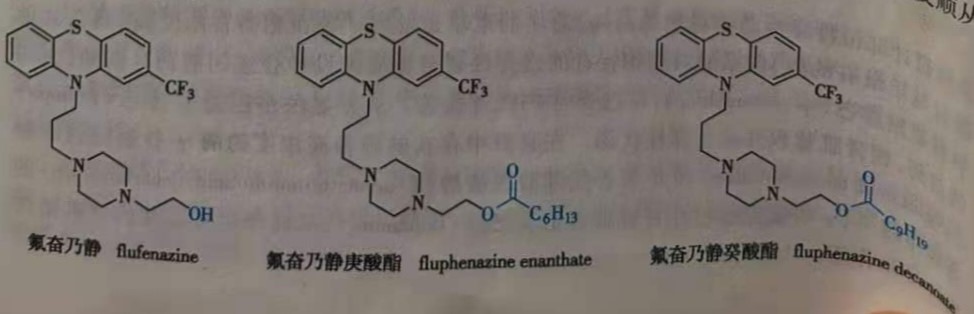
除非药物能蓄积在脂肪中,否则口服给药的药物作用时间不会比它们在胃肠道的转运时间(12~48小时)长很多。对于那些被身体快速清除的药物,其作用时间更短,因此需要在24小时内多次给药以维持血药浓度在治疗水平。为延长药物的作用时间,可制备亲脂性前药,将其溶解或悬浮在油性介质中,深部肌内注射给药。例如,抗精神病药氟奋乃静(flufenazine)作用时间较短(6~8小时),利用其分子中的羟基,制成庚酸酯( fluphenazine enanthate)和癸酸酯( fluphenazine decanoate),作用时间可达一个月左右,适用于需要长期用药及顺从性不好的精神分裂症患者
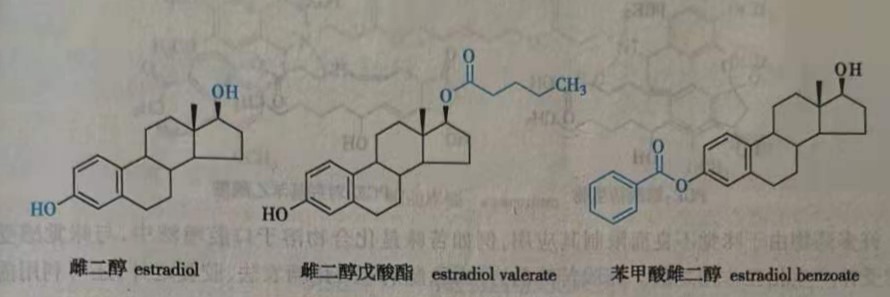
雌二醇(estradiol)等天然雌激素在体内迅速代谢,作用时间短暂。与长链脂肪酸形成的酯类,因不溶于水而贮存于体内脂肪组织中成为延效制剂。如雌二醇戊酸酯( estradiol valerate)及苯甲酸雌二醇( estradiol benzoate)可在体内缓慢水解,释放出母体药物而延长疗效,作用时间可持续数周。
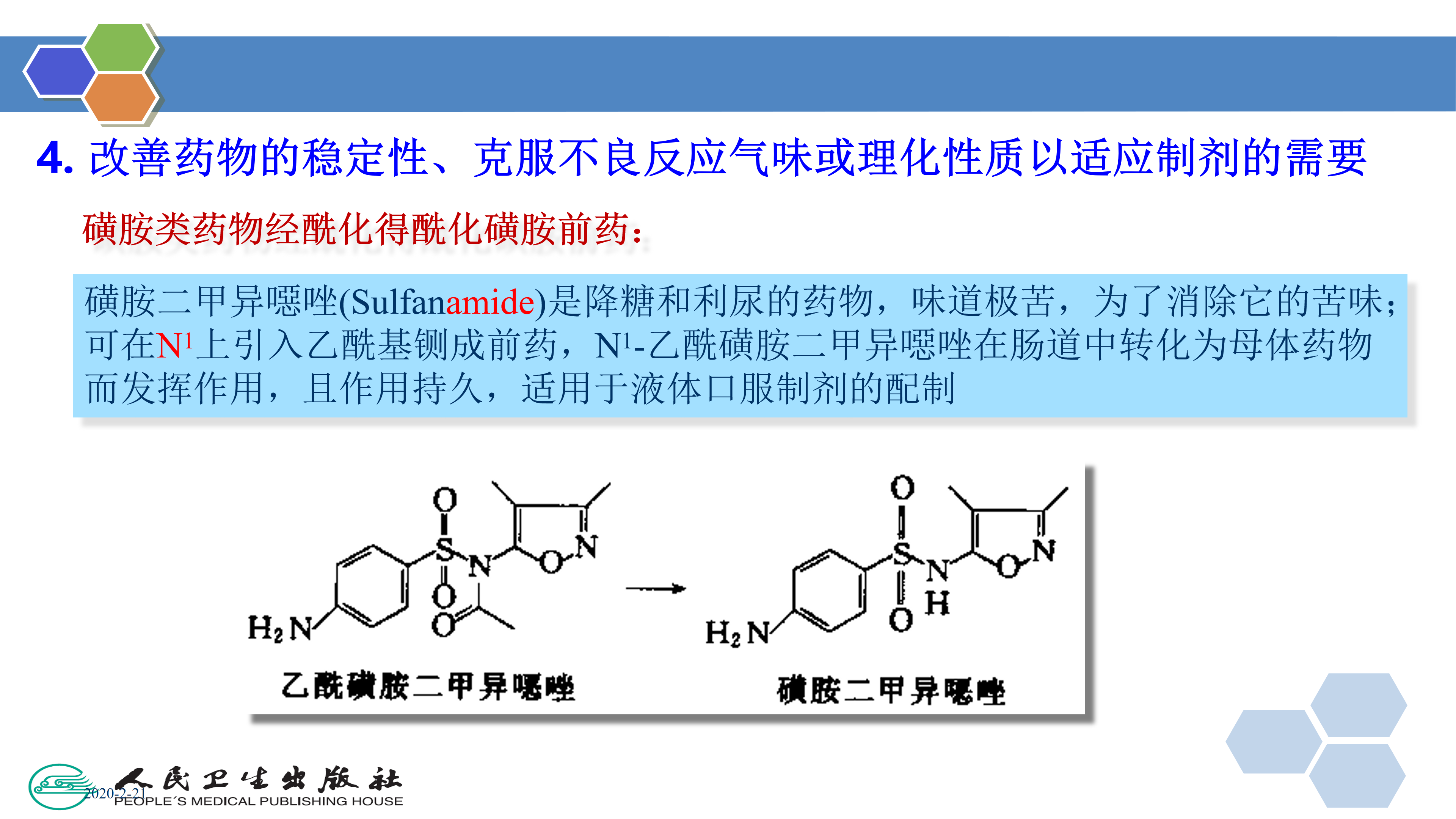
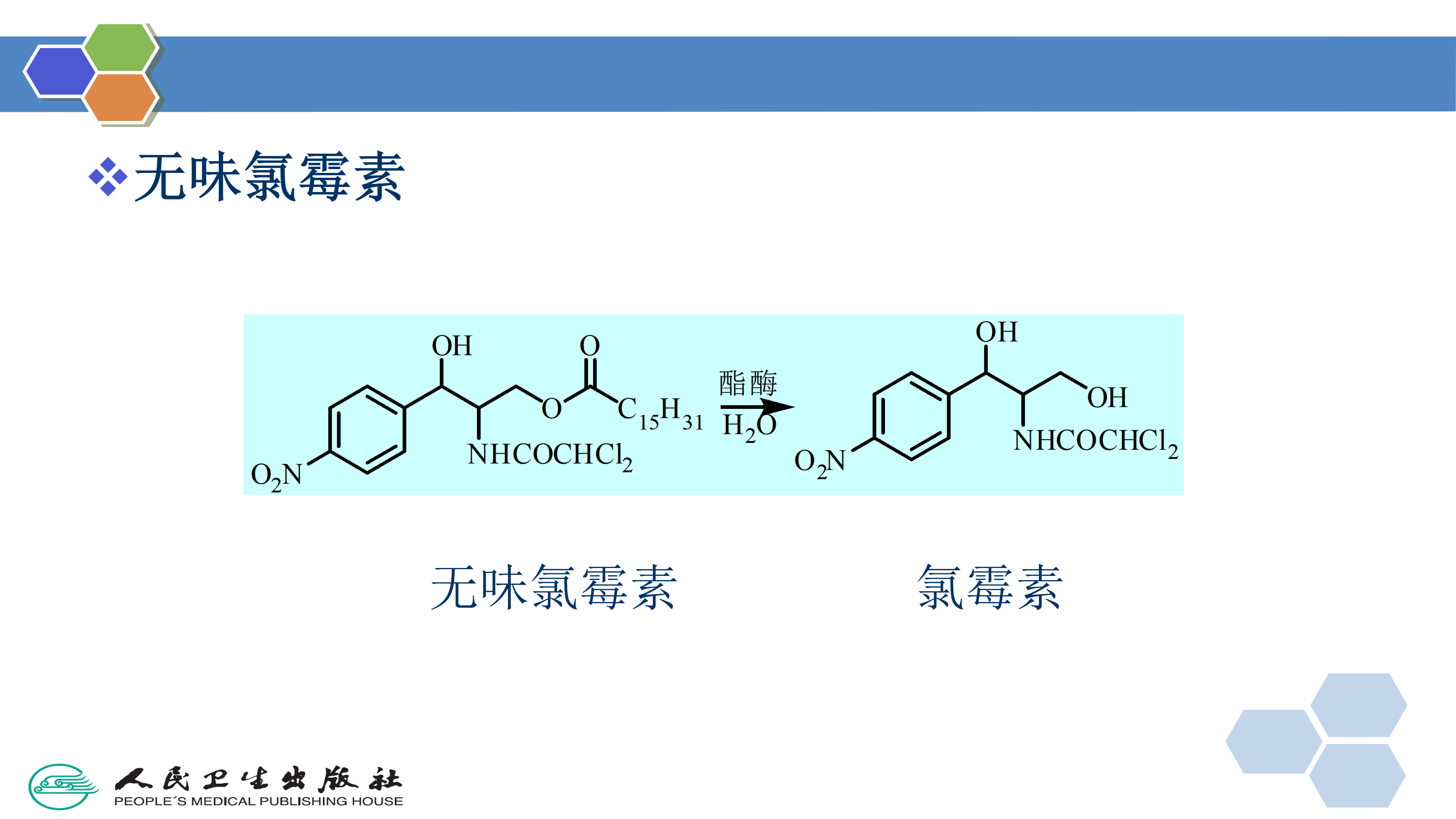
4. 改善药物的水溶性、稳定性、克服不良气味或理化性质以适应制剂的需要
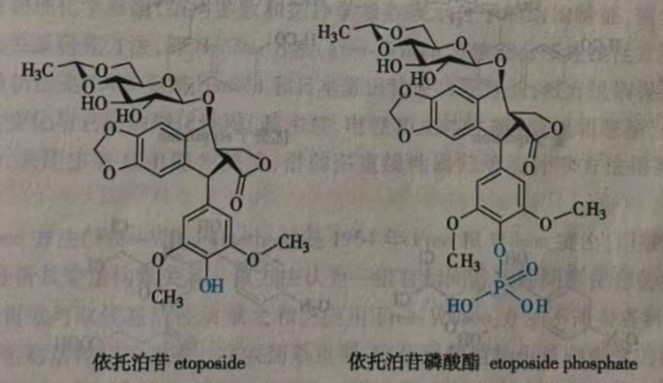
有的药物由于分子中缺少亲水基团而水溶性太小,解决的办法之一就是利用前药原理,在分子中引入一些亲水性基团,增加水溶性,以利于注射给药。如甾体类抗炎药倍他米松、地塞米松、氢化可的松等通过分子中的羟基与磷酸或有机二元酸成酯,制成有良好水溶性的盐类,可以制成针剂。在体内通过酶解而重新释放出母体化合物发挥作用。抗肿瘤药依托泊苷( etoposide)因为水溶性小,制剂中需加入表面活性剂吐温80、聚乙二醇和乙醇,这些物质都有一定毒性。将依托泊苷转变为依托泊苷磷酸酯( etoposide phosphate)后,就可在没有加入有害辅料的条件下,在较短时间内以更高的浓度在体内转运。
有些药物的稳定性不好,可能通过水解、氧化等途径降解。虽然通常情况下通过制剂过程中的防护和选择生产工艺可以克服降解问题,但是,有时候需要通过化学修饰来解决化学性质不稳定的问题。例如,前列腺素E2( prostaglandin E2,PGE2,又称地诺前列酮dinoprostone),是结晶性固体(熔点63℃,室温下稳定期较短,几个月后迅速液化分解)。其不稳定性是由于C-11位羟基发生消除形成前列腺素A2(PGA2)。将地诺前列酮C-9位的羰基制成缩酮类衍生物,固态稳定性明显改善,在胃内酸性条件下易水解为母体药物,是一种口服有效的前药。地诺前列酮与对羟基苯乙酮形成酯,也是克服前者化学不稳定的一种方法,这种结晶性的酯类化合物室温储存22-30个月几乎无降解,仍为白色固体;而母体药物(游离的酸)在室温下放置12个月后有44%~59%降解。