第三节 胎儿附属物的形成与功能
•胎儿-胎盘循环是母胎之间物质交换的基础。
•胎盘合成多种激素、酶和细胞因子等,以维持正常妊娠,但胎盘的屏障作用有限。
•胎膜保持羊膜腔的完整性,对胎儿起到保护作用。
•脐带内的脐动脉、脐静脉血流是母儿之间物质交换的通道。
•羊水对胎儿和母体有保护作用,通过羊膜腔内母儿间液体交换,保持量的相对恒定。
胎儿附属物包括胎盘、胎膜、脐带和羊水,它们对维持胎儿宫内的生命及生长发育起重要作用。
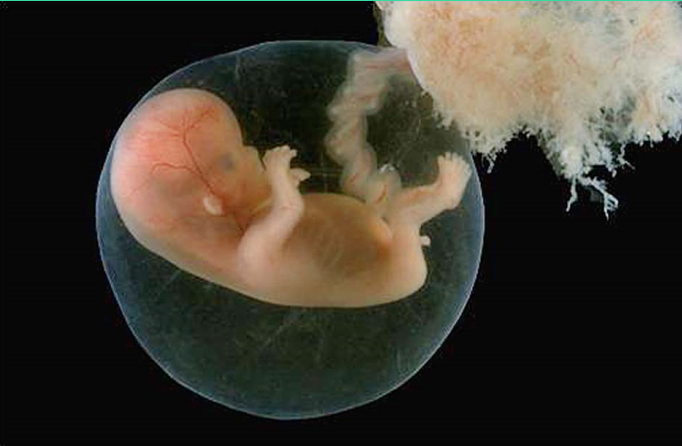
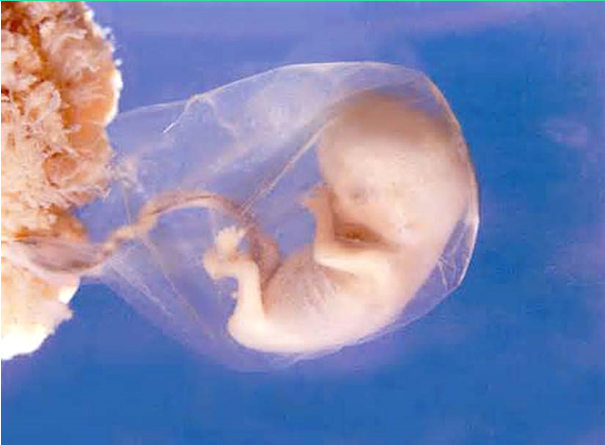
胎儿附属物
一、胎 盘
(一)胎盘的结构
胎盘(placenta)由胎儿部分的羊膜和叶状绒毛膜以及母体部分的底蜕膜构成。
1.羊膜(amnion) 为附着在胎盘胎儿面的半透明薄膜。羊膜光滑,无血管、神经及淋巴。正常羊膜厚0.02~0.05mm,电镜见上皮细胞表面有微绒毛,使羊水与羊膜间进行交换。
2.叶状绒毛膜(chorion frondosum) 为胎盘的主要结构。晚期囊胚着床后,着床部位的滋养层细胞迅速分裂增殖,内层为细胞滋养细胞,是分裂生长的细胞;外层为合体滋养细胞,是执行功能的细胞,由细胞滋养细胞分化而来。滋养层内面有一层胚外中胚层,与滋养层共同组成绒毛膜。与底蜕膜相接触的绒毛营养丰富发育良好,称为叶状绒毛膜。胎盘的主要结构叶状绒毛形成历经3个阶段:①初级绒毛:绒毛膜表面长出呈放射状排列的合体滋养细胞小梁,绒毛膜深部增生活跃的细胞滋养细胞伸入其中,形成合体滋养细胞小梁的细胞中心索;②次级绒毛:初级绒毛继续增长,胚外中胚层长入细胞中心索,形成间质中心索;③三级绒毛:约在受精后第3周末,胚胎血管长入间质中心,绒毛内血管形成。一个初级绒毛干及其分支形成一个胎儿叶,一个次级绒毛干及其分支形成一个胎儿小叶。每个胎盘有60~80个胎儿叶、200个胎儿小叶。
每个绒毛干中均有脐动脉和脐静脉的分支,随着绒毛干一再分支,脐血管越来越细,最终形成胎儿毛细血管进入的三级绒毛,此时,胎儿-胎盘循环建立。绒毛之间的间隙称绒毛间隙(intervillous space)。在滋养细胞侵入子宫壁的过程中,子宫螺旋血管破裂,直接开口于绒毛间隙,绒毛间隙充满母体血液,游离绒毛悬浮于其中,母儿间物质交换在悬浮于母血的绒毛处进行(图4-3)。
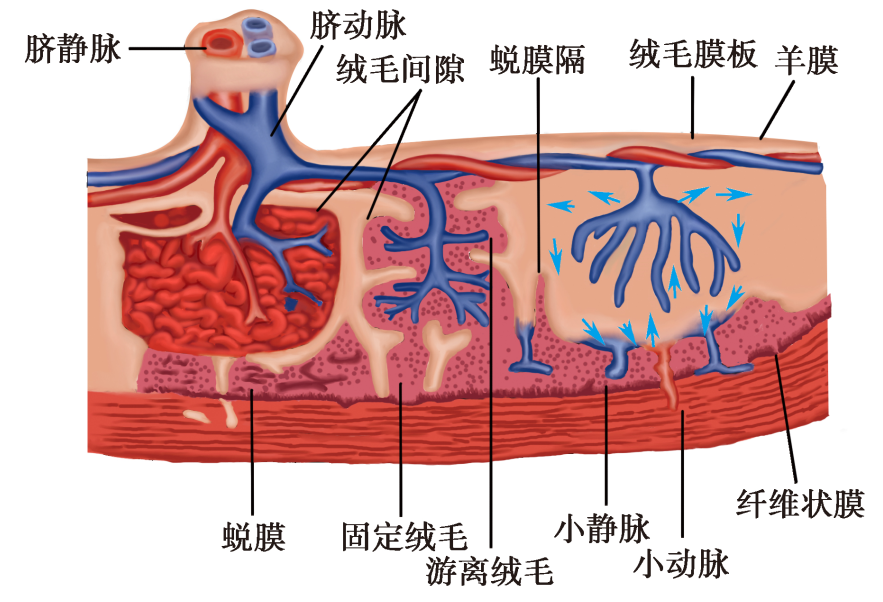
图4-3 胎盘结构与胎儿-胎盘循环模式图
子宫-胎盘循环建立的一个重要环节是子宫螺旋动脉重塑,由两种绒毛外滋养细胞完成;①间质滋养细胞:穿透蜕膜、子宫内膜和子宫肌层内1/3处,聚集在螺旋动脉周围,为血管内滋养细胞的侵入做准备;②血管内滋养细胞:以逆行方式沿螺旋动脉内腔迁移,取代血管内皮,使狭窄肌性管腔转变为扩张的低阻力子宫胎盘血管。妊娠早期迁移的血管内滋养细胞在螺旋动脉末端形成栓子并将其堵塞。至早孕末栓子消失,子宫-胎盘循环得以建立。螺旋动脉重塑障碍可导致子痫前期、胎儿生长受限(fetal growth restaton,FGR)或两者同时发生。重度子痼前期并发FGR时,只有10%的螺旋动脉完全重塑,而正常妊娠螺旋动脉重塑率达96%。
妊娠足月胎盘绒毛表面积达12~14m2,相当于成人肠道总面积。因此,母儿之间交换面积巨大。胎儿体内含氧量低、代谢废物浓度高的血液经脐动脉流至绒毛毛细血管,与绒毛间隙中的母血进行物质交换后,脐静脉将含氧量高、营养丰富的血液带回胎儿体内,以保证胎儿生长发育。胎儿血和母血不直接相通,之间隔有绒毛毛细血管壁、绒毛间质及绒毛滋养细胞层,构成母胎界面(maternal- fetal interface),有胎盘屏障(placental barrier)的作用。
3.底蜕膜 来自胎盘附着部位的子宫内膜,占胎盘很小部分。固定绒毛的滋养层细胞与底蜕膜共同形成绒毛间隙的底,称为蜕膜板。从此板向绒毛膜伸出蜕膜间隔,不超过胎盘厚度的2/3,将胎盘母体面分成肉眼可见的20个左右母体叶。
妊娠足月胎盘呈盘状,多为圆形或椭圆形,重450~650g,直径16~20cm,厚1~3cm,中央厚,边缘薄。胎盘分胎儿面和母体面。胎儿面被覆羊膜,呈灰白色,光滑半透明,脐带动静脉从附着处分支向四周呈放射状分布直达胎盘边缘,其分支穿过绒毛膜板,进入绒毛干及其分支。母体面呈暗红色,蜕膜间隔形成若干浅沟分成母体叶。
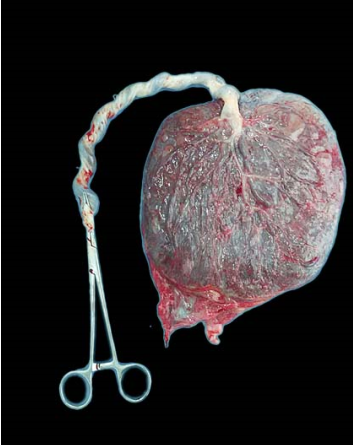
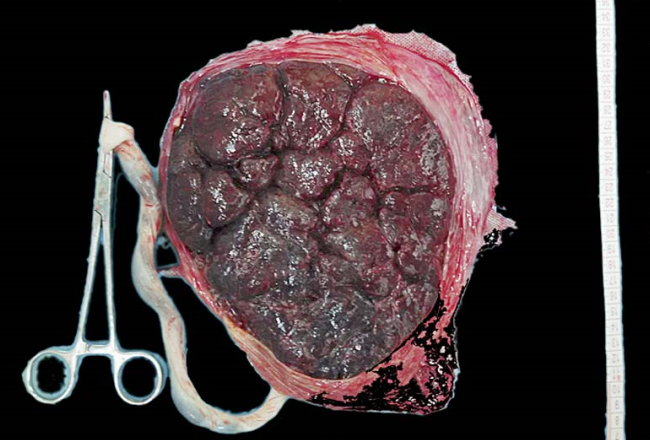
足月胎盘大体结构(胎儿面) 足月胎盘大体结构(母体面)
(二)胎盘的功能
胎盘介于胎儿与母体之间,是维持胎儿宫内生长发育的重要器官。具有物质交换、防御、合成以及免疫等功能。
1.物质交换功能 包括气体交换、营养物质供应和排出胎儿代谢产物等。
(1)气体交换:母儿间O2和CO2在胎盘中以简单扩散方式进行交换,相当于胎儿呼吸系统的功能。子宫动脉血氧分压(PO2)高于绒毛间隙内血PO2和胎儿脐动脉血PO2,但胎儿血红蛋白对O2亲和力强,能从母血中获得充分的O2。CO2的扩散速度比O2快20倍,且胎儿血对CO2亲和力低于母血,故胎儿CO2容易通过绒毛间隙直接向母体迅速扩散。
(2)营养物质供应:葡萄糖是胎儿代谢的主要能源,以易化扩散方式通过胎盘,胎儿体内的葡萄糖均来自母体。氨基酸、钙、磷、碘和铁以主动运输方式通过胎盘。游离脂肪酸、水、钾、钠、镁,维生素A、维生素D、维生素E、维生素K以简单扩散方式通过胎盘。
(3)排出胎儿代谢产物:胎儿代谢产物如尿素、尿酸、肌酐、肌酸等,经胎盘转输入母血,由母体排出体外。
2.防御功能 胎盘屏障作用极为有限。各种病毒(如风疹病毒、巨细胞病毒等)及大部分药物均可通过胎盘,影响胎儿生长发育。细菌、弓形虫、衣原体、梅毒螺旋体不能通过胎盘屏障,但可在胎盘部位形成病灶,破坏绒毛结构后进人胎体感染胚胎及胎儿。母血中免疫抗体如gC能通过胎盘,使胎儿在出生后短时间内获得被动免疫力。
3.合成功能 胎盘合体滋养细胞能合成多种激素、酶、神经递质和细胞因子,对维持正常妊娠起重要作用。
(1)人绒毛膜促性腺激素(human chorionic gonadotropin,hCC):是一种由@、B亚基组成的糖蛋白激素,在受精卵着床后1日可自母血清中测出,妊娠8~10周达高峰,以后迅速下降,产后2周内消失(详见第三十四章第七节“女性内分泌激素测定”)。hCG的功能有:①维持月经黄体寿命,使月经黄体增大成为妊娠黄体,增加甾体激素分泌以维持妊娠;②促进雄激素芳香化转化为雌激素,同时能刺激孕酮的形成;③抑制植物血凝素对淋巴细胞的刺激作用,hCG能吸附于滋养细胞表面,以免胚胎滋养层被母体淋巴细胞攻击;④刺激胎儿皋丸分泌睾酮,促进男胎性分化;⑤能与母体甲状腺细胞TSH受体结合,刺激甲状腺活性。
(2)人胎盘生乳素(human placental lactogen,hPL):是一种单链多肽激素。妊娠5周即可在母体血浆中测出hPL,随妊娠进展其分泌量持续增加,至妊娠39~40周达高峰并维持至分娩,产后迅速下降,产后7小时即测不出。hPL的功能有:①促进乳腺腺泡发育,刺激乳腺上皮细胞合成乳白蛋白、乳酪蛋白和乳珠蛋白,为产后泌乳作准备;②促进胰岛素生成;③通过脂解作用提高游离脂肪酸、甘油浓度,以游离脂肪酸作为能源,抑制对葡萄糖的摄取,将多余葡萄糖运送给胎儿,是胎儿的主要能源,也是蛋白质合成的能源来源;④抑制母体对胎儿的排斥作用。hPL是通过母体促进胎儿发育的“代谢调节因子”。
(3)雌激素:是一种甾体激素,妊娠早期由卵巢黄体产生,妊娠10周后主要由胎儿-胎盘单位合成。至妊娠末期,雌三醇值为非孕妇女的1000倍,雌二醇及雌酮值为非孕妇女的100倍。
雌激素生成过程:母体胆固醇在胎盘内转变为孕烯醇酮后,经胎儿肾上腺胎儿带转化为硫酸脱氢表雄酮(dehydroisoandrosterone,DHAS),再经胎儿肝内16α-羟化酶作用,形成16α-羟基硫酸脱氢表雄酮(16α-OH-DHAS)后,在胎盘合体滋养细胞硫酸酯酶作用下,去硫酸根形成16α-OH-DHA,随后经胎盘芳香化酶作用成为16α-羟基雄烯二酮,最终形成游离雌三醇。
(4)孕激素:妊娠早期由卵巢妊娠黄体产生。妊娠8~10周后,胎盘合体滋养细胞是产生孕激素的主要来源。母血孕酮值随妊娠进展逐渐增高,至妊娠足月达312~624nmol/L,其代谢产物为孕二醇,24小时尿排出值为35~45mg。孕激素在雌激素协同作用下,对妊娠期子宫内膜、子宫肌层、乳腺以及母体其他系统的生理变化起重要作用。
(5)缩宫素酶(oxytocinase):为分子量约30万的糖蛋白。随妊娠进展逐渐增多,至妊娠末期达高值。其生物学意义尚不十分明了,主要作用是灭活缩宫素分子,维持妊娠。胎盘功能不良,如死胎、子痫前期、胎儿生长受限时,血中缩宫素酶降低。
(6)耐热性碱性磷酸酶(heat stable alkaline phosphatase,HSAP):妊娠16~20周母血清中可测出。随妊娠进展而增多,直至胎盘娩出后其值下降,产后3~6日消失。动态测其数值,可作为检查胎盘功能的一项指标。
(7)细胞因子与生长因子:如表皮生长因子(epidermal growth factor,EGF)、神经生长因子、胰岛素样生长因子(insulin like growth factor,IGF)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、白细胞介素(interleukin,IL)-1、2、6、8等。上述因子在胚胎和胎儿营养及免疫保护中起一定作用。
4.免疫功能 胎儿是同种半异体移植物(semiallogenic graft)。正常妊娠母体能容受、不排斥胎儿,其具体机制目前尚不清楚,可能与早期胚胎组织无抗原性、母胎界面的免疫耐受以及妊娠期母体免疫力低下有关。
二、胎 膜
胎膜(fetal membranes)是由外层的平滑绒毛膜(chorion leave)和内层的羊膜组成。囊胚表面非着床部位的绒毛膜在发育过程中缺乏营养逐渐退化萎缩成为平滑绒毛膜。羊膜为无血管膜,结实、坚韧而柔软,与覆盖胎盘、脐带的羊膜层相连。能转运溶质和水,参与以羊水平衡的维持;能合成血管活性肽、生长因子和细胞因子,参与血管张力的调节。至妊娠晚期平滑绒毛膜与羊膜轻轻贴附并能分开。胎膜的重要作用是维持羊膜腔的完整性,对胎儿起到保护作用。胎膜含大量花生四烯酸(前列腺素前身物质)的磷脂,且含能催化磷脂生成游离花生四烯酸的溶酶体,在分娩发动上有一定作用。
三、脐 带
脐带(umbilical cord)是连接胎儿与胎盘的条索状组织,胎儿借助脐带悬浮于羊水中。足月妊娠的脐带长30~100cm,平均约55cm,直径0.8~2.0cm。脐带表面有羊膜覆盖呈灰白色,内有一条脐静脉,两条脐动脉,脐血管周围为含水量丰富来自胚外中胚层的胶样组织,称为华通胶(Wharton jelly),有保护脐血管的作用。脐带是母体与胎儿气体交换、营养物质供应和代谢产物排出的重要通道。脐带受压使血流受阻时,可致胎儿缺氧,甚至危及胎儿生命。
四、羊 水
充满在羊膜腔内的液体,称为羊水(amniotic fluid)。
1.羊水的来源 ①妊娠早期的羊水主要来自母体血清经胎膜进入羊膜腔的透析液;②妊娠中期以后,胎儿尿液成为羊水的主要来源,使羊水的渗透压逐渐降低;③妊娠晚期胎儿肺参与羊水的生成,每日600~800ml液体从肺泡分泌至羊膜腔;④羊膜、脐带华通胶及胎儿皮肤渗出液体,但量少。
2.羊水的吸收 ①约50%由胎膜完成;②胎儿吞咽羊水,足月妊娠胎儿每日可吞咽羊水500~700ml;③脐带每小时能吸收羊水40~50ml;④20孕周前,胎儿角化前皮肤有吸收羊水的功能,但量很少。
3.母体、胎儿、羊水三者间的液体平衡 羊水在羊膜腔内不断进行液体交换,以保持羊水量相对恒定。母儿间的液体交换主要通过胎盘,每小时约3600ml。母体与羊水的交换主要通过胎膜,每小时约400ml。羊水与胎儿间主要通过胎儿消化管、呼吸道、泌尿道以及角化前皮肤进行交换。
4.羊水量、性状及成分 妊娠期羊水量逐渐增加,妊娠38周约1000ml,此后羊水量逐渐减少。妊娠40周羊水量约800ml。过期妊娠羊水量明显减少,可减少至300ml以下。妊娠早期羊水为无色澄清液体。妊娠足月羊水略混浊、不透明,可见羊水内悬有小片状物(胎脂、胎儿脱落上皮细胞、毳毛、毛发、少量白细胞、白蛋白、尿酸盐等)。羊水中含大量激素和酶。足月妊娠时羊水比重为1.007~1.025,pH约为7.20,内含水分98%~99%,1%~2%为无机盐及有机物。
5.羊水的功能
(1)保护胎儿:羊膜腔内恒温,适量的羊水对胎儿有缓冲作用,避免胎儿受到挤压,防止胎肢粘连,避免子宫肌壁或胎儿对脐带直接压迫所致的胎儿窘迫;临产宫缩时,羊水能使宫缩压力均匀分布,避免胎儿局部受压所致的胎儿窘迫。胎儿吞咽或吸入羊水可促进胎儿消化道和肺的发育,孕期羊水过少可引起胎儿肺发育不良。
(2)保护母体:妊娠期减少胎动所致的不适感;临产后,前羊水囊借助楔形水压扩张宫口及阴道;破膜后羊水冲洗阴道,减少感染机会。


