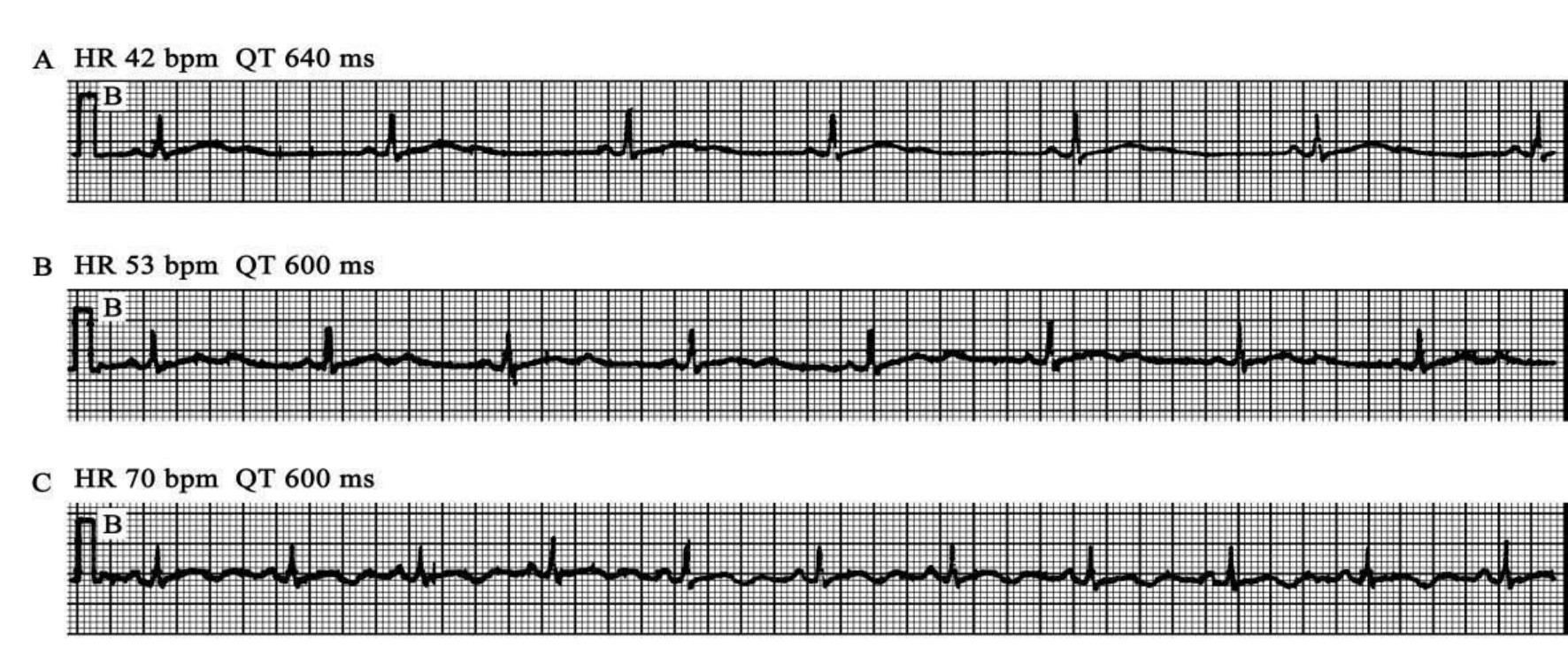
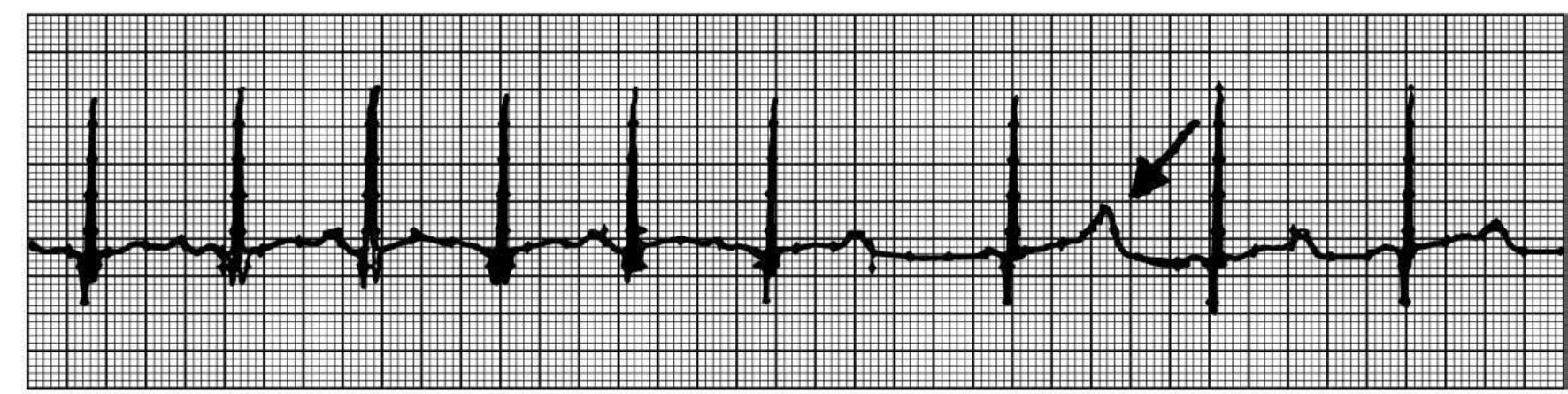
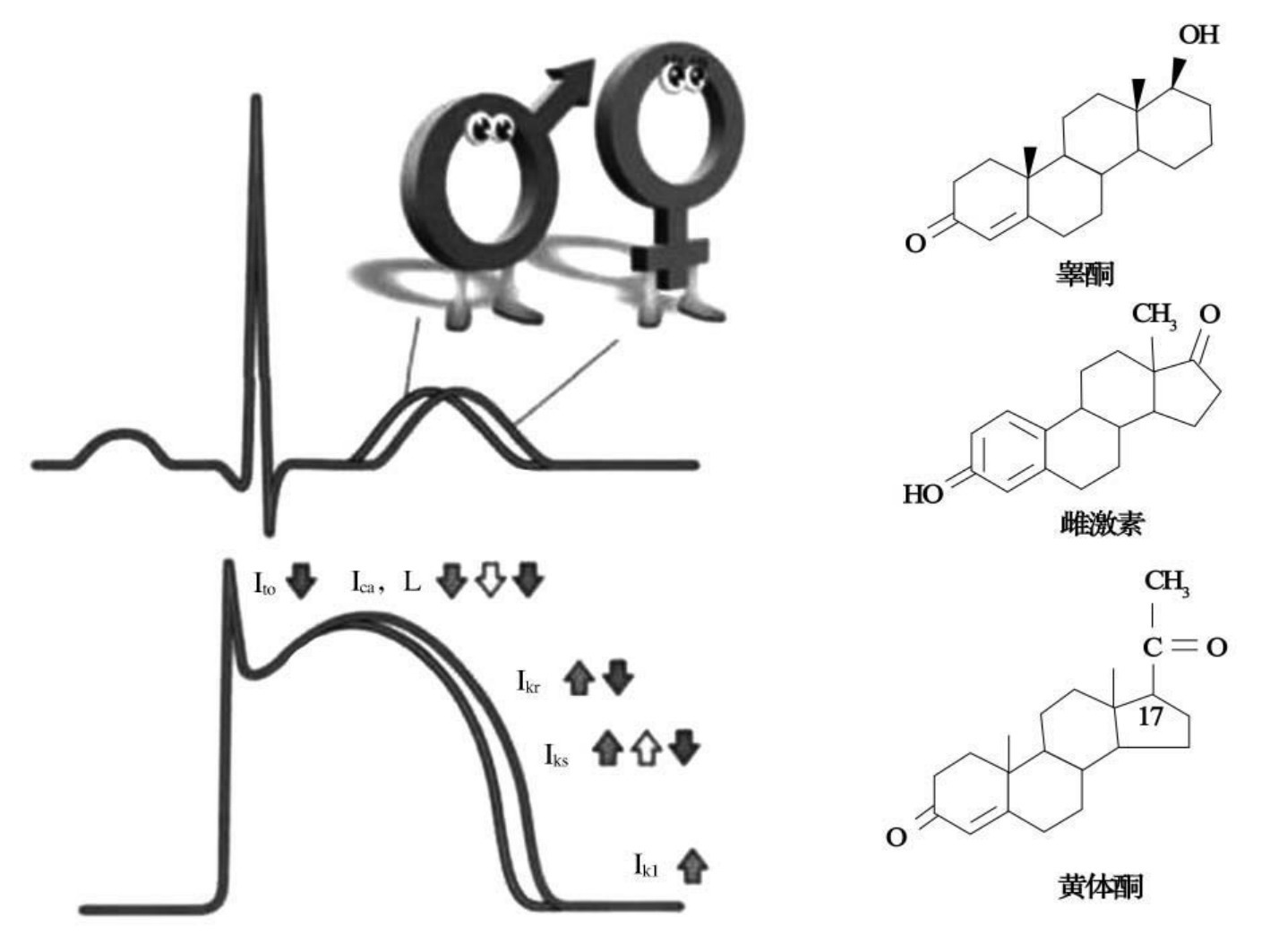
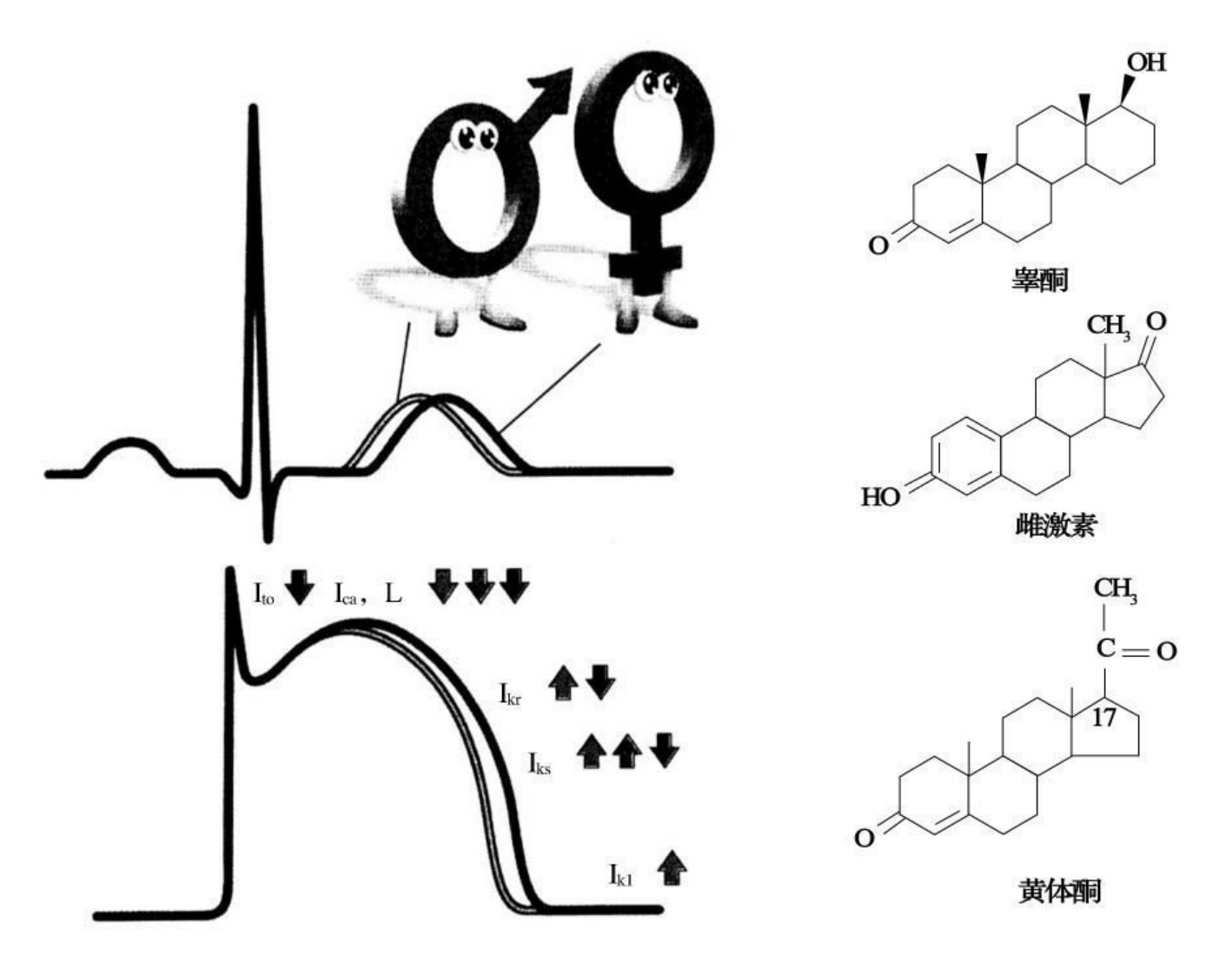
-
1.1主编简介
-
1.2陈 序
-
1.3赵 序
-
1.4周 序
-
1.5第二版 前言
-
1.6上 卷
-
1.6.1第一篇 心电学基本知识
-
1.6.1.1第一章 心脏解剖生理学
-
1.6.1.1.1第一节 心脏的解剖
-
1.6.1.1.2第二节 心脏传导组织的胚胎发育
-
1.6.1.1.3第三节 先天异常的心脏传导系统解剖
-
1.6.1.1.4第四节 心脏的生理
-
1.6.1.2第二章 心脏电生理学基础
-
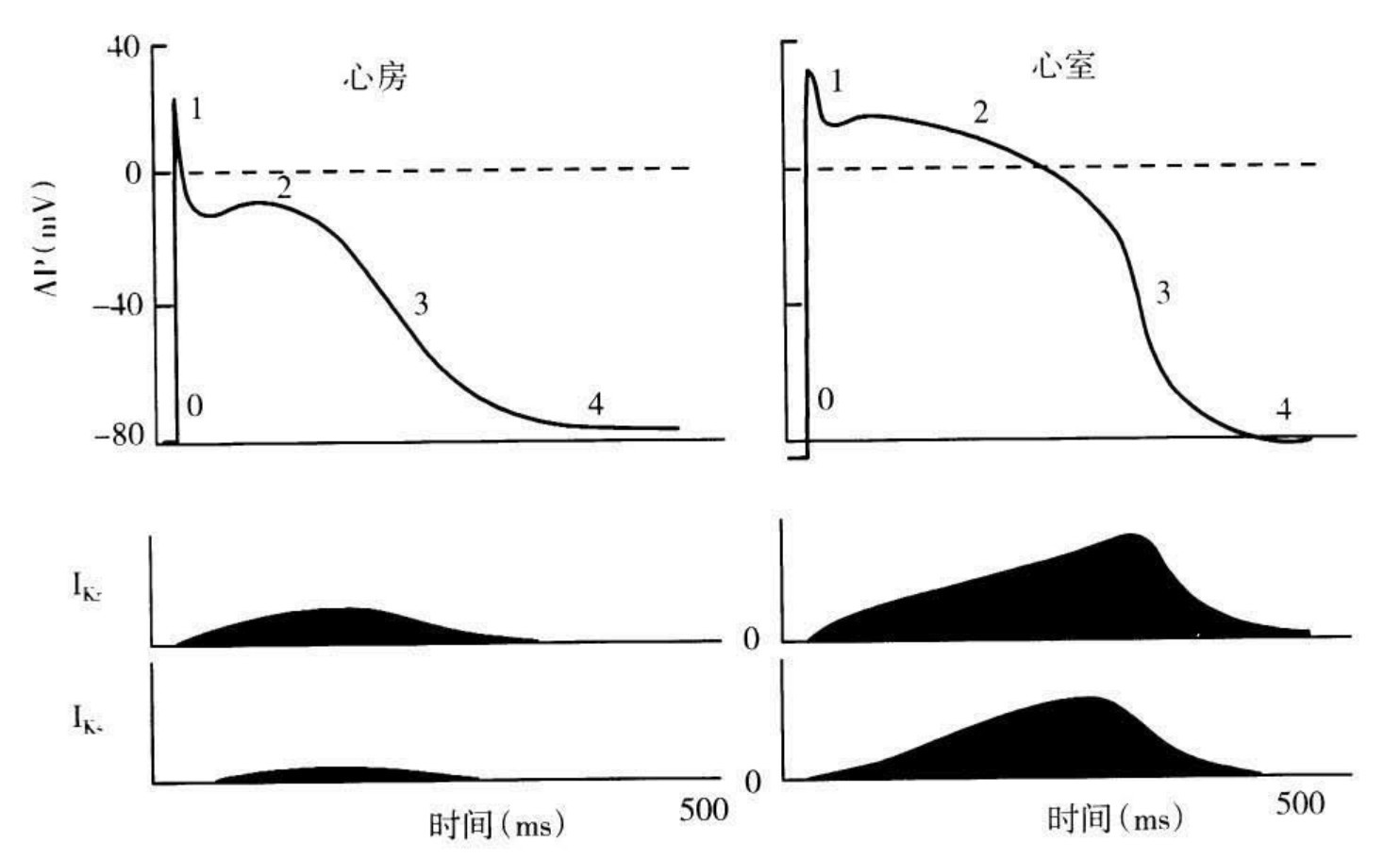
1.6.1.2.1第一节 心肌细胞的生物电现象
-
1.6.1.2.2第二节 心肌细胞及其电活动类型
-
1.6.1.2.3第三节 心肌细胞的电生理特性
-
1.6.1.2.4第四节 影响心肌细胞电生理特性的因素
-
1.6.1.2.5第五节 心律失常的电生理基础
-
1.6.1.2.6第六节 抗心律失常药物的电生理
-
1.6.1.2.7第七节 电解质对心电生理的影响
-
1.6.1.3第三章 心电图发生的原理
-
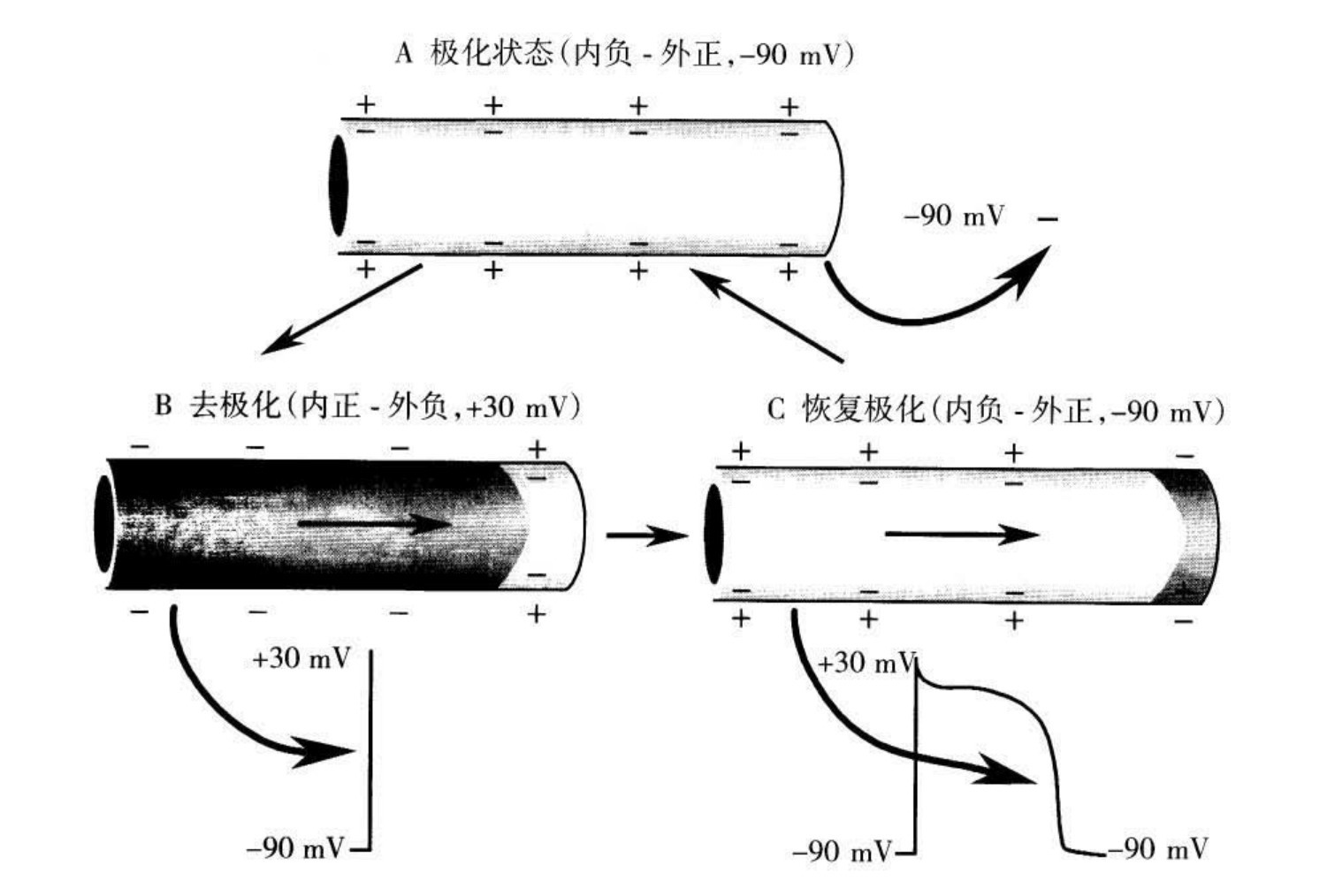
1.6.1.3.1第一节 心肌细胞的除极和复极
-
1.6.1.3.2第二节 心脏的除极与复极
-
1.6.1.3.3第三节 电偶学说及容积导电的概念
-
1.6.1.3.4第四节 心肌细胞的不应期
-
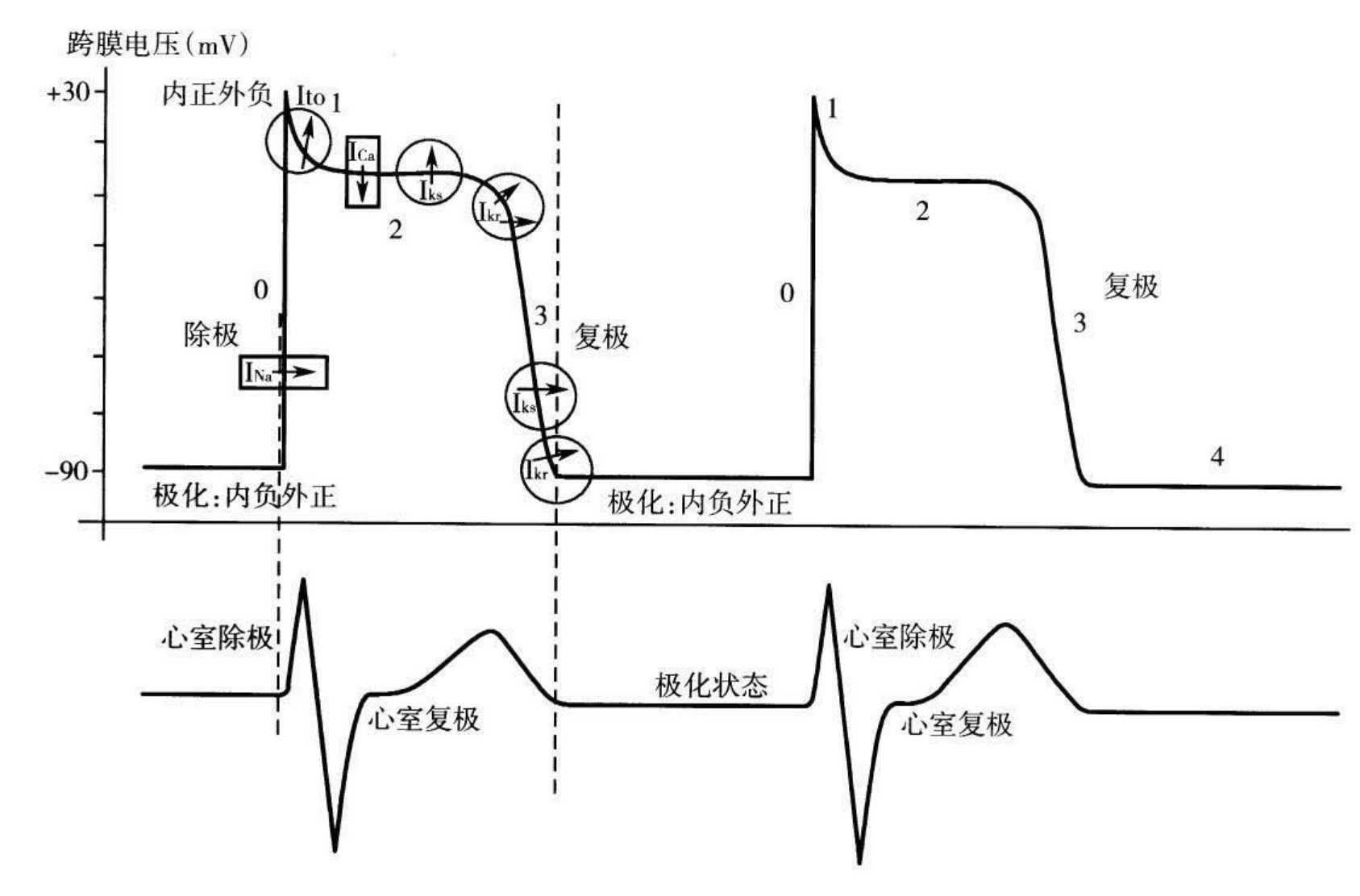
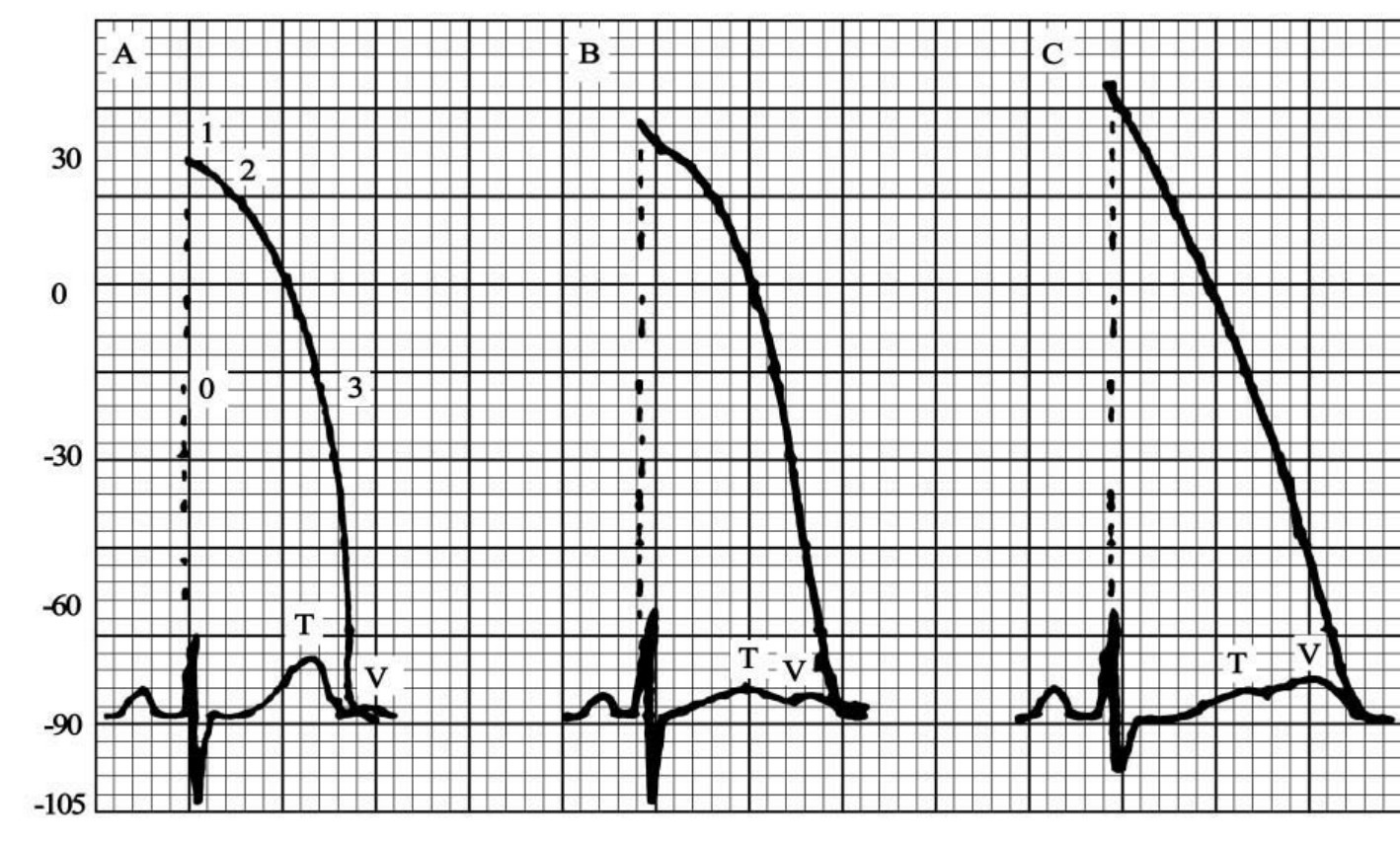
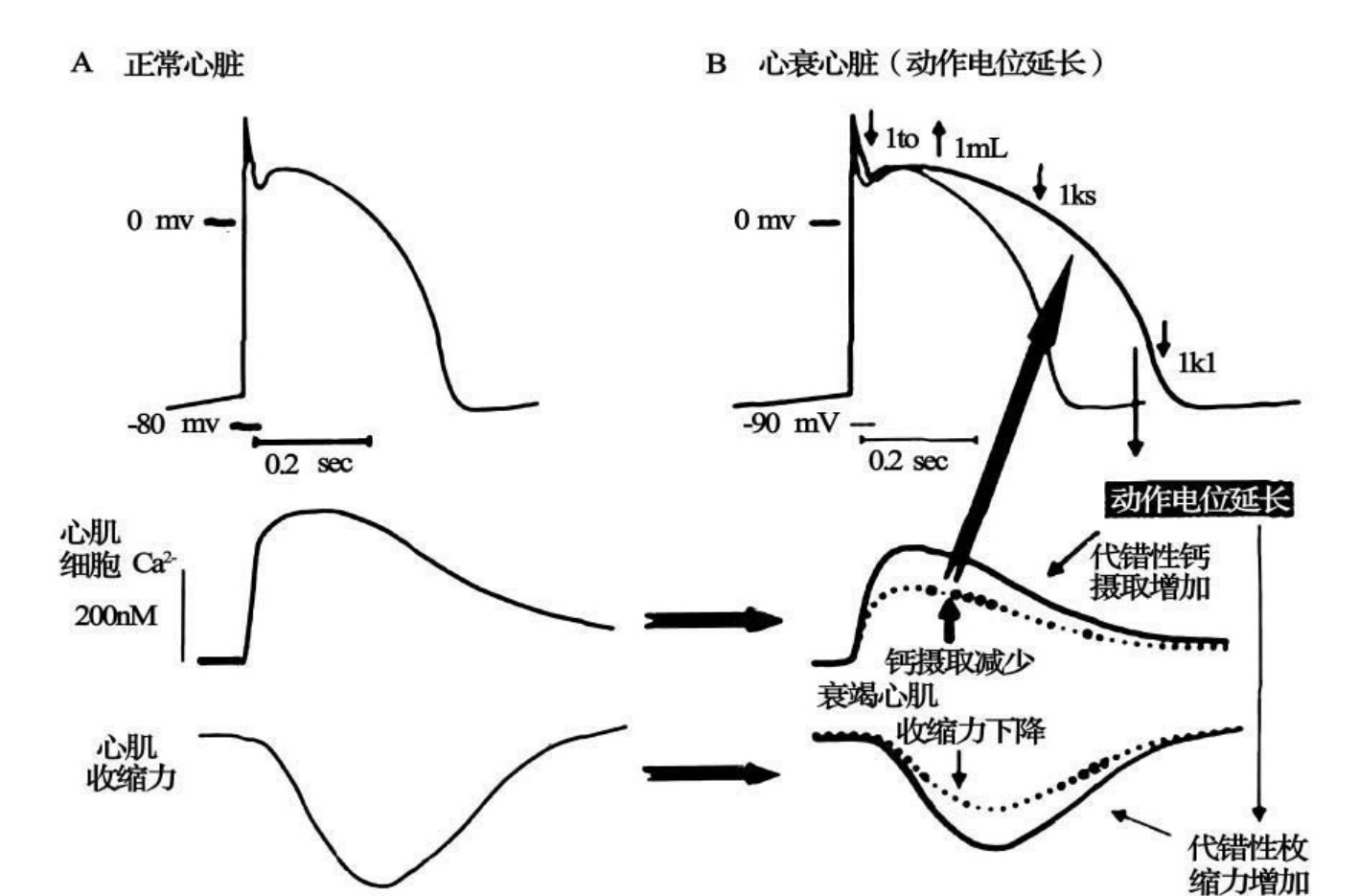
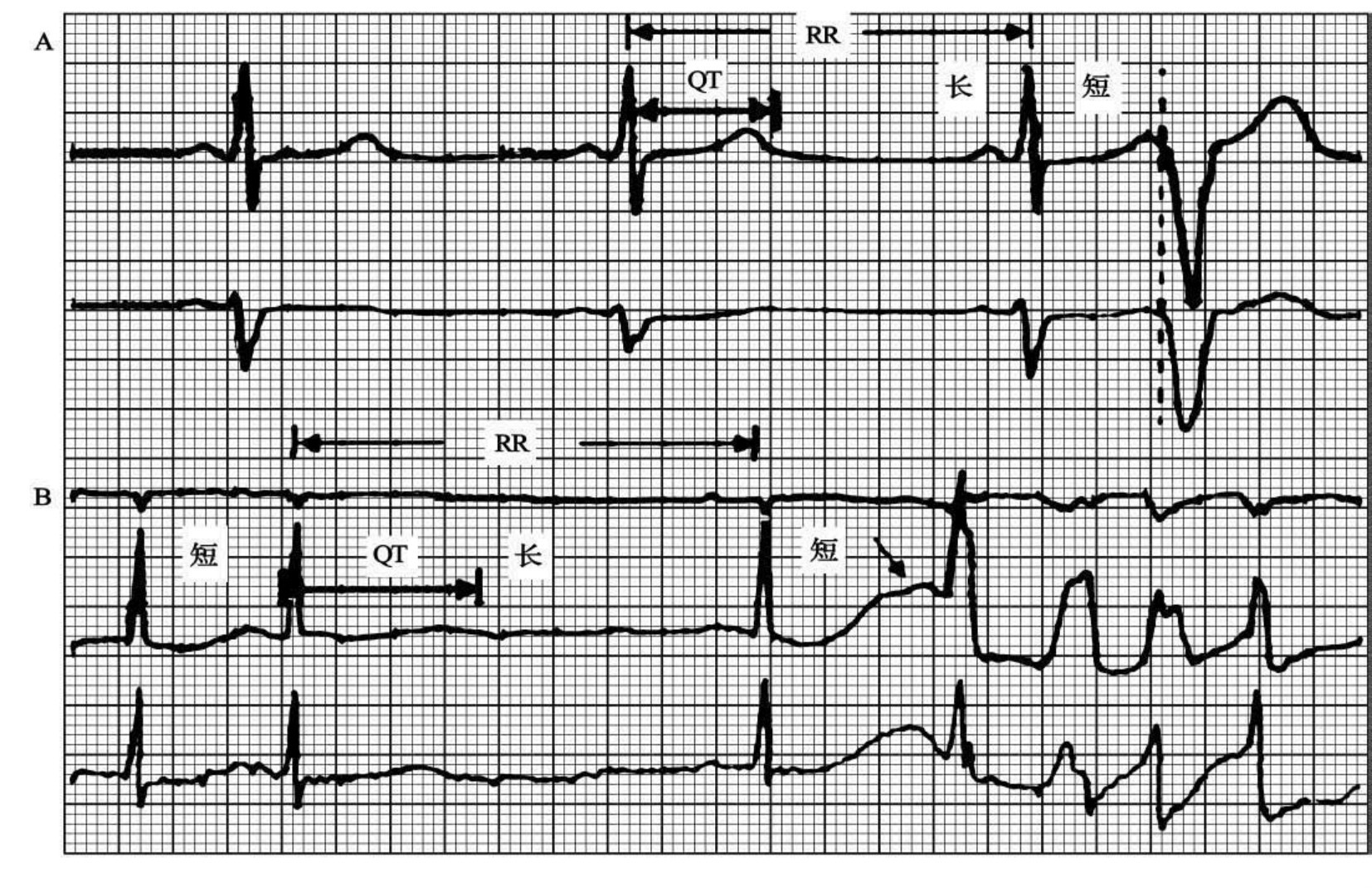
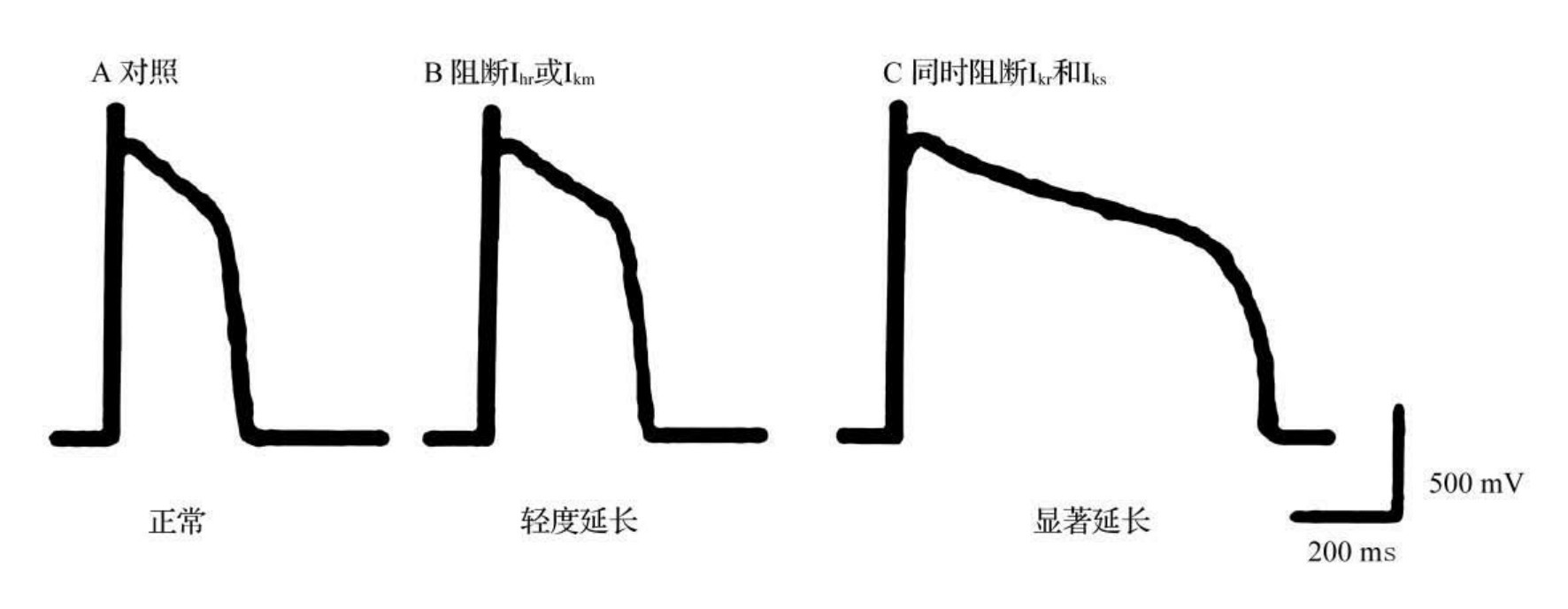
1.6.1.3.5第五节 心肌细胞动作电位与心电图的关系
-
1.6.1.4第四章 心电向量和心电向量图
-
1.6.1.4.1第一节 心电向量基本概念
-
1.6.1.4.2第二节 心电向量的导联体系
-
1.6.1.4.3第三节 心电向量图与心电图的关系
-
1.6.1.4.4第四节 心电向量图的分析、诊断及报告
-
1.6.1.4.5第五节 正常成人心电向量图
-
1.6.1.4.6第六节 常见异常心电向量图
-
1.6.1.5第五章 心电图导联
-
1.6.1.5.1第一节 常用导联
-
1.6.1.5.2第二节 不常用导联
-
1.6.1.6第六章 心电轴、心电位和心室复极差力
-
1.6.1.6.1第一节 心电轴
-
1.6.1.6.2第二节 心电位
-
1.6.1.6.3第三节 心室复极差力
-
1.6.1.7第七章 心电图机及其应用
-
1.6.1.7.1第一节 心电图机的分类
-
1.6.1.7.2第二节 心电图机的主要技术指标
-
1.6.1.7.3第三节 单导联心电图机简介
-
1.6.1.7.4第四节 多导心电图机简介
-
1.6.1.7.5第五节 心电图机常见故障及排除
-
1.6.1.8第八章 正常心电图及常见伪差
-
1.6.1.8.1第一节 心电图记录纸的划线与定标
-
1.6.1.8.2第二节 心电图测量
-
1.6.1.8.3第三节 正常心电图各波、间期的形态、时间及电压
-
1.6.1.8.4第四节 正常心电图波形
-
1.6.1.8.5第五节 心电图各波、间期的正常变异
-
1.6.1.8.6第六节 心电图常见伪差
-
1.6.1.8.7第七节 影响心电图波形的生理因素
-
1.6.1.8.8第八节 影响心电图的技术因素
-
1.6.1.9第九章 心电图及心电生理检查常规及报告规范
-
1.6.1.9.1国内心电图及电生理检查规范
-
1.6.1.9.2第一节 常规心电图检查操作规程
-
1.6.1.9.3第二节 动态心电图检查操作规程
-
1.6.1.9.4第三节 心电图运动负荷试验
-
1.6.1.9.5第四节 远程监测心电图
-
1.6.1.9.6第五节 心率变异性
-
1.6.1.9.7第六节 心室晚电位
-
1.6.1.9.8第七节 T电交替
-
1.6.1.9.9第八节 食管心脏调搏技术
-
1.6.1.9.10第九节 直立倾斜试验
-
1.6.1.9.11第十节 心电图药物试验
-
1.6.1.9.12第十一节 临床心电生理检查工作常规
-
1.6.1.9.13第十二节 心电图报告格式和诊断名词、术语规范化建议(草案)
-
1.6.2第二篇 常见心脏疾病的心电图
-
1.6.2.1第十章 心房、心室扩大与肥厚
-
1.6.2.1.1第一节 心房肥厚与扩大
-
1.6.2.1.2第二节 心室肥厚与扩大
-
1.6.2.2第十一章 心肌缺血
-
1.6.2.2.1第一节 冠状动脉解剖与冠状循环
-
1.6.2.2.2第二节 冠状动脉供血不足的病理生理
-
1.6.2.2.3第三节 冠状动脉供血不足的心电图表现
-
1.6.2.2.4第四节 心脏起搏时心肌缺血的心电图诊断
-
1.6.2.3第十二章 心肌梗死
-
1.6.2.3.1第一节 概述
-
1.6.2.3.2第二节 急性心肌梗死的心电图变化原理
-
1.6.2.3.3第三节 急性心肌梗死的心电图特征及其演变分期
-
1.6.2.3.4第四节 心肌梗死深度及范围判断
-
1.6.2.3.5第五节 心肌梗死的定位诊断
-
1.6.2.3.6第六节 不同部位心肌梗死的心电图和心电向量图诊断
-
1.6.2.3.7第七节 心电图在急性心肌梗死诊断中作用变化
-
1.6.2.3.8第八节 急性心肌梗死的分型及对心肌梗死时心电图改变的新认识
-
1.6.2.3.9第九节 不典型心肌梗死的心电图诊断
-
1.6.2.3.10第十节 多发性心肌梗死的心电图诊断
-
1.6.2.3.11第十一节 复发性心肌梗死的心电图诊断
-
1.6.2.3.12第十二节 急性心肌梗死合并心律失常
-
1.6.2.3.13第十三节 心肌梗死合并束支传导阻滞
-
1.6.2.3.14第十四节 心肌梗死合并预激综合征的心电图诊断
-
1.6.2.3.15第十五节 心肌梗死合并室壁瘤
-
1.6.2.3.16第十六节 对急性心肌梗死心电图改变的新认识
-
1.6.2.3.17第十七节 心肌梗死的心电图鉴别诊断
-
1.6.2.3.18第十八节 再灌注后获益的心电图变化
-
1.6.2.3.19第十九节 心电图判断梗死的相关冠状动脉
-
1.6.2.3.20第二十节 心肌梗死心电图与临床
-
1.6.2.4第十三章 心肌炎、心肌病、心包炎和心脏肿瘤
-
1.6.2.4.1第一节 心肌炎
-
1.6.2.4.2第二节 心肌病
-
1.6.2.4.3第三节 心包炎和心包积液
-
1.6.2.4.4第四节 心脏肿瘤
-
1.6.2.5第十四章 心肌损害
-
1.6.2.5.1第一节 概述
-
1.6.2.5.2第二节 心肌损害的病因及心电图改变
-
1.6.2.6第十五章 先天性心脏病
-
1.6.2.6.1第一节 概 述
-
1.6.2.6.2第二节 房间隔缺损
-
1.6.2.6.3第三节 室间隔缺损
-
1.6.2.6.4第四节 肺动脉瓣狭窄
-
1.6.2.6.5第五节 动脉导管未闭
-
1.6.2.6.6第六节 法洛四联症
-
1.6.2.6.7第七节 右位心
-
1.6.2.6.8第八节 先天性主动脉缩窄
-
1.6.2.6.9第九节 先天性三尖瓣异常
-
1.6.2.6.10第十节 主动脉瓣膜或主动脉瓣下狭窄
-
1.6.2.6.11第十一节 其他先天性心脏病
-
1.6.2.6.12第十二节 原发传导系统退化症
-
1.6.2.6.13第十三节 先天性房室传导阻滞
-
1.6.2.7第十六章 后天性心脏疾病
-
1.6.2.7.1第一节 风湿性心脏病
-
1.6.2.7.2第二节 肺源性心脏病
-
1.6.2.7.3第三节 高血压及高血压心脏病
-
1.6.2.7.4第四节 心内膜炎
-
1.6.2.7.5第五节 二尖瓣脱垂
-
1.6.2.8第十七章 全身性疾病的心电图改变
-
1.6.2.8.1第一节 呼吸系统疾病心电图改变
-
1.6.2.8.2第二节 神经系统疾病心电图改变
-
1.6.2.8.3第三节 内分泌系统疾病心电图改变
-
1.6.2.8.4第四节 消化系统疾病心电图改变
-
1.6.2.8.5第五节 泌尿系统疾病心电图改变
-
1.6.2.8.6第六节 肌肉疾病与心电图改变
-
1.6.2.8.7第七节 中毒性疾病心电图改变
-
1.6.2.8.8第八节 阻塞性睡眠呼吸暂停综合征
-
1.6.2.9第十八章 老年心电图
-
1.6.2.9.1第一节 老年人心电图研究概况
-
1.6.2.9.2第二节 老年人心血管增龄性变化
-
1.6.2.9.3第三节 老年心电图表现
-
1.6.2.10第十九章 药物影响及电解质紊乱
-
1.6.2.10.1第一节 药物影响的心电图改变
-
1.6.2.10.2第二节 电解质紊乱的心电图
-
1.6.2.11第二十章 麻醉、低温时的心电图改变
-
1.6.2.11.1第一节 围手术期麻醉药对循环系统的影响
-
1.6.2.11.2第二节 麻醉期间非麻醉药因素对循环系统功能的影响
-
1.6.2.11.3第三节 低温麻醉时的心电图变化
-
1.6.2.12第二十一章 心搏骤停及心肺复苏术中的心电图改变
-
1.6.2.12.1第一节 心搏骤停(猝死)先兆的心电图改变
-
1.6.2.12.2第二节 心搏骤停时的心电图改变
-
1.6.2.12.3第三节 心肺复苏过程中伴发的心律失常
-
1.6.2.13第二十二章 急性心肌梗死溶栓治疗中的心电图表现
-
1.6.2.13.1第一节 急性心肌梗死再灌注的病理生理
-
1.6.2.13.2第二节 急性心肌缺血再灌注有效性心电图
-
1.6.2.13.3第三节 急性心肌缺血再灌注损伤性心电图
-
1.6.2.14第二十三章 心脏血管手术及创伤时的心电图表现
-
1.6.2.14.1第一节 心脏外伤时的心电图表现
-
1.6.2.14.2第二节 心脏血管手术并发心律失常
-
1.6.2.14.3第三节 经皮冠状动脉腔内成形术前后的心电图变化
-
1.6.2.14.4第四节 冠状动脉内粥样硬化斑块旋磨术前后的心电图变化
-
1.6.2.14.5第五节 冠状动脉旁路移植术前后的心电图变化
-
1.6.2.14.6第六节 激光心肌血管重建术前后的心电图变化
-
1.6.2.14.7第七节 心脏射频消融术前后的心电图变化
-
1.6.2.14.8第八节 心脏导管检查及冠状动脉造影过程中的心电图变化
-
1.6.2.15第二十四章 心脏综合征的心电图改变
-
1.6.2.15.1第一节 X综合征
-
1.6.2.15.2第二节 S<sub>Ⅰ</sub>S<sub>Ⅱ</sub>S<sub>Ⅲ</sub>综合征
-
1.6.2.15.3第三节 两点半综合征
-
1.6.2.15.4第四节 早期复极综合征
-
1.6.2.15.5第五节 心肌震荡综合征
-
1.6.2.15.6第六节 加速传导综合征(短P-R综合征)
-
1.6.2.15.7第七节 P-R间期过度延长综合征
-
1.6.2.15.8第八节 阿-斯综合征
-
1.6.2.15.9第九节 慢-快综合征
-
1.6.2.15.10第十节 快-慢综合征
-
1.6.2.15.11第十一节 运动员心脏综合征
-
1.6.2.15.12第十二节 单纯T波倒置综合征
-
1.6.2.15.13第十三节 孤立负性T波综合征
-
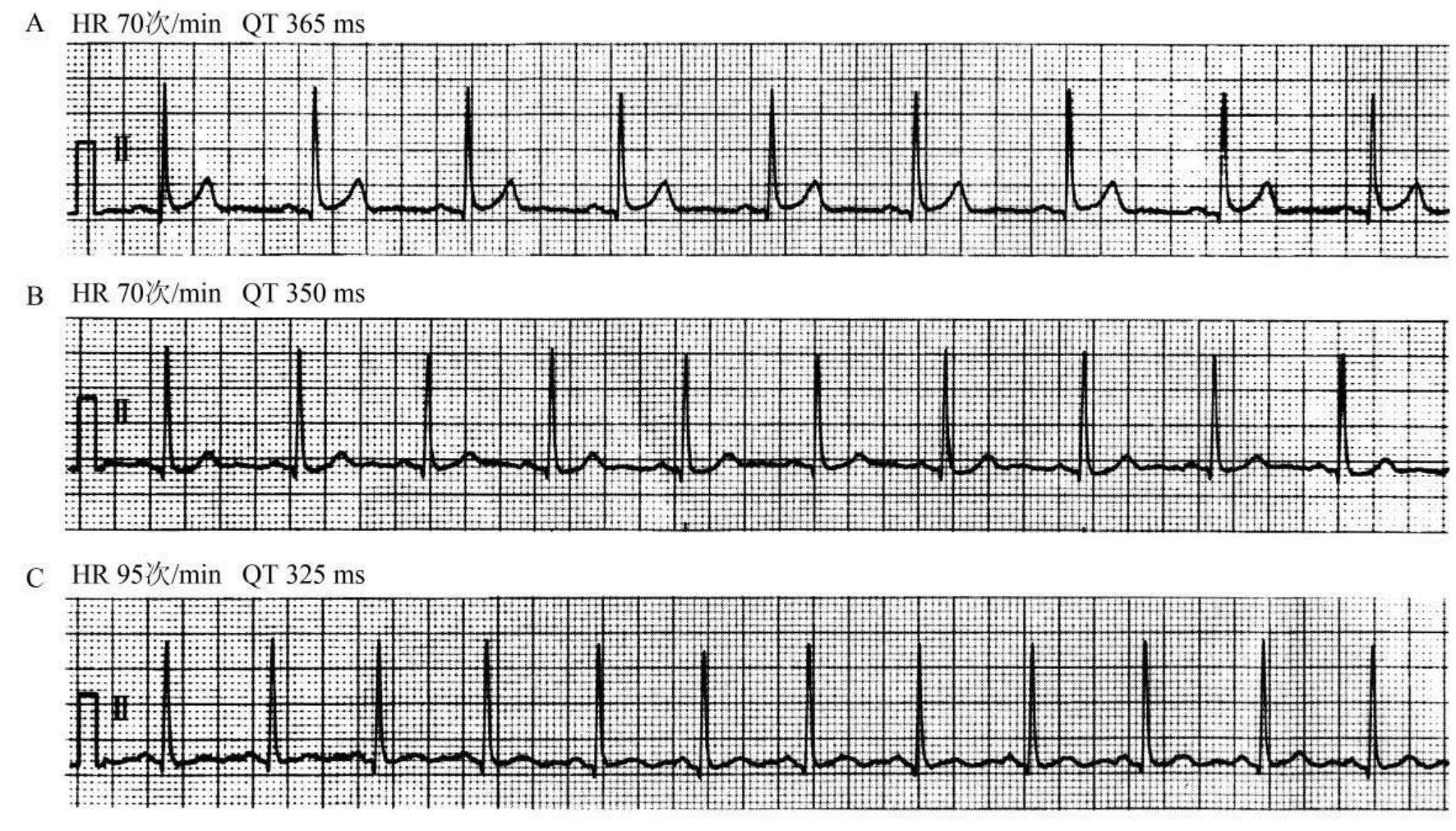
1.6.2.15.14第十四节 长Q-T综合征
-
1.6.2.15.15第十五节 短Q-T综合征
-
1.6.2.15.16第十六节 β受体亢进综合征
-
1.6.2.15.17第十七节 心神经官能症
-
1.6.2.15.18第十八节 直背综合征
-
1.6.2.15.19第十九节 复极延缓综合征
-
1.6.2.15.20第二十节 颈动脉窦综合征
-
1.6.2.15.21第二十一节 T<sub>V1</sub>>T<sub>V5</sub>综合征
-
1.6.2.15.22第二十二节 致心律失常性右心室发育不良综合征
-
1.6.2.15.23第二十三节 心脏震击猝死综合征
-
1.6.2.15.24第二十四节 左心室心尖球囊综合征
-
1.6.2.15.25第二十五节 小心脏综合征
-
1.6.2.15.26第二十六节 迷走神经性心律失常综合征
-
1.6.2.15.27第二十七节 心动过速后综合征
-
1.6.2.15.28第二十八节 卢山—铃木综合征
-
1.6.2.15.29第二十九节 Brugada综合征
-
1.6.2.15.30第三十节 急性冠状动脉综合征
-
1.6.2.15.31第三十一节 J波综合征
-
1.6.2.15.32第三十二节 病态窦房结综合征
-
1.6.2.15.33第三十三节 肌袖综合征
-
1.6.2.16第二十五章 心脏性猝死
-
1.6.2.16.1第一节 概述
-
1.6.2.16.2第二节 心脏性猝死的电生理
-
1.6.2.16.3第三节 心脏性猝死的心电图
-
1.6.2.16.4第四节 心脏性猝死的心电学预测
-
1.6.3第三篇 心律失常
-
1.6.3.1第二十六章 心律失常总论
-
1.6.3.1.1第一节 概述
-
1.6.3.1.2第二节 心律失常的诊断与分析方法
-
1.6.3.1.3第三节 心律失常治疗
-
1.6.3.2第二十七章 窦性心律失常
-
1.6.3.2.1第一节 概述
-
1.6.3.2.2第二节 窦性心动过速
-
1.6.3.2.3第三节 窦性心动过缓
-
1.6.3.2.4第四节 窦性心律不齐
-
1.6.3.2.5第五节 窦性并行心律
-
1.6.3.2.6第六节 窦房结功能障碍
-
1.6.3.3第二十八章 游走心律及特殊的房性心律
-
1.6.3.3.1第一节 游走心律
-
1.6.3.3.2第二节 特殊的房性心律
-
1.6.3.4第二十九章 逸搏与逸搏心律
-
1.6.3.4.1第一节 概述
-
1.6.3.4.2第二节 窦性逸搏和逸搏心律
-
1.6.3.4.3第三节 房性逸搏和逸搏心律
-
1.6.3.4.4第四节 房室交界性逸搏和逸搏心律
-
1.6.3.4.5第五节 室性逸搏和逸搏心律
-
1.6.3.4.6第五节 短阵型室性心动过速
-
1.6.3.4.7第六节 持续型室性心动过速
-
1.6.3.4.8第七节 特发性室性心动过速
-
1.6.3.4.9第八节 分支性室性心动过速
-
1.6.3.4.10第九节 束支折返性室性心动过速
-
1.6.3.4.11第十节 双向性室性心动过速
-
1.6.3.4.12第十一节 单形性室性心动过速
-
1.6.3.4.13第十二节 多源性和多形性室性心动过速
-
1.6.3.4.14第十三节 并行心律性室性心动过速
-
1.6.3.4.15第十四节 尖端扭转型室性心动过速
-
1.6.3.4.16第十五节 极短联律间期多形性室性心动过速
-
1.6.3.4.17第十六节 短Q-T综合征与多形性室性心动过速
-
1.6.3.4.18第十七节 长Q-T综合征与多形性室性心动过速
-
1.6.3.4.19第十八节 室性心动过速与临床
-
1.6.3.5第三十三章 非阵发性心动过速
-
1.6.3.5.1第一节 概述
-
1.6.3.5.2第二节 非阵发性窦房交界性心动过速
-
1.6.3.5.3第三节 非阵发性房性心动过速
-
1.6.3.5.4第四节 非阵发性交界性心动过速
-
1.6.3.5.5第五节 交界性异位性心动过速
-
1.6.3.5.6第六节 双重性房室交界性心律
-
1.6.3.5.7第七节 非阵发性室性心动过速
-
1.6.3.5.8第八节 非阵发性心动过速与临床
-
1.6.3.6第三十四章 心房扑动和心房颤动
-
1.6.3.6.1第一节 概 述
-
1.6.3.6.2第二节 心房扑动
-
1.6.3.6.3第三节 心房颤动
-
1.6.3.6.4第四节 混乱性心房性心律
-
1.6.3.7第三十五章 心室扑动和心室颤动
-
1.6.3.7.1第一节 概述
-
1.6.3.7.2第二节 心室扑动
-
1.6.3.7.3第三节 心室颤动
-
1.6.3.7.4第四节 心室扑动和心室颤动的临床
-
1.6.3.8第三十六章 干扰与干扰性脱节
-
1.6.3.8.1第一节 概述
-
1.6.3.8.2第二节 干扰
-
1.6.3.8.3第三节 干扰性脱节
-
1.6.3.9第三十七章 折返激动
-
1.6.3.9.1第一节 概述
-
1.6.3.9.2第二节 折返激动形成的条件
-
1.6.3.9.3第三节 折返激动的分类及其发生机制
-
1.6.3.9.4第四节 折返激动诱发、维持与消除
-
1.6.3.9.5第五节 窦房结折返
-
1.6.3.9.6第六节 心房内折返
-
1.6.3.9.7第七节 房室交接区折返
-
1.6.3.9.8第八节 房室折返
-
1.6.3.9.9第九节 心室内折返
-
1.6.3.9.10第十节 反复搏动
-
1.6.3.9.11第十一节 临床意义
-
1.6.3.10第三十八章 反复搏动与反复心律
-
1.6.3.10.1第一节 概述
-
1.6.3.10.2第二节 反复搏动与反复心律的定义
-
1.6.3.10.3第三节 产生反复搏动的条件
-
1.6.3.10.4第四节 反复搏动的发生机制
-
1.6.3.10.5第五节 反复搏动的分类
-
1.6.3.10.6第六节 反复搏动的鉴别诊断
-
1.6.3.10.7第七节 反复搏动与反复心律的临床意义
-
1.6.3.11第三十九章 并行心律及并行性心动过速
-
1.6.3.11.1第一节 概 述
-
1.6.3.11.2第二节 并行心律发生的机制
-
1.6.3.11.3第三节 并行心律的分类及心电图基本特征
-
1.6.3.11.4第四节 窦性并行心律
-
1.6.3.11.5第五节 房性并行心律
-
1.6.3.11.6第六节 房室交接性并行心律
-
1.6.3.11.7第七节 室性并行心律
-
1.6.3.11.8第八节 房室旁路性并行心律
-
1.6.3.11.9第九节 特殊类型的并行心律
-
1.6.3.11.10第十节 并行心律鉴别诊断
-
1.6.3.11.11第十一节 并行心律临床意义
-
1.6.3.12第四十章 心脏传导阻滞
-
1.6.3.12.1第一节 概 述
-
1.6.3.12.2第二节 窦房传导阻滞
-
1.6.3.12.3第三节 心房内传导阻滞
-
1.6.3.12.4第四节 房室传导阻滞
-
1.6.3.12.5第五节 室内传导阻滞
-
1.6.3.12.6第六节 频率依赖性传导阻滞
-
1.6.3.13第四十一章 心室预激和预激综合征
-
1.6.3.13.1第一节 概 述
-
1.6.3.13.2第二节 WPW综合征
-
1.6.3.13.3第三节 LGL综合征
-
1.6.3.13.4第四节 变异型预激综合征(Mahaim纤维)
-
1.6.3.14第四十二章 遗传性心律失常
-
1.6.3.14.1第一节 概 述
-
1.6.3.14.2第二节 长Q-T综合征
-
1.6.3.14.3第三节 短Q-T综合征
-
1.6.3.14.4第四节 Brugada综合征
-
1.6.3.14.5第五节 致心律失常性右心室发育不良
-
1.6.3.14.6第六节 儿茶酚胺敏感性多形性室性心动过速
-
1.6.4第四篇 常见心电现象、心电图部分相关概念及心电特波
-
1.6.4.1第四十三章 常见心电现象
-
1.6.4.1.1第一节 隐匿性传导
-
1.6.4.1.2第二节 差异性传导
-
1.6.4.1.3第三节 意外传导
-
1.6.4.1.4第四节 文氏现象
-
1.6.4.1.5第五节 1∶2房室传导性心动过速
-
1.6.4.1.6第六节 单向传导与单向传导阻滞
-
1.6.4.1.7第七节 传入阻滞与传出阻滞
-
1.6.4.1.8第八节 频率依赖性传导现象
-
1.6.4.1.9第九节 跳跃传导与双径路传导现象
-
1.6.4.1.10第十节 分层传导阻滞
-
1.6.4.1.11第十一节 多径路传导现象
-
1.6.4.1.12第十二节 抑制性传导与递减传导现象
-
1.6.4.1.13第十三节 跨越传导现象及越顶现象
-
1.6.4.1.14第十四节 临界相传导现象
-
1.6.4.1.15第十五节 窦室传导现象
-
1.6.4.1.16第十六节 心脏电交替现象
-
1.6.4.1.17第十七节 心电阶梯现象、起步现象与手风琴样效应
-
1.6.4.1.18第十八节 节律重整现象
-
1.6.4.1.19第十九节 蝉联现象
-
1.6.4.1.20第二十节 二联律法则及长短周期现象
-
1.6.4.1.21第二十一节 拖带现象
-
1.6.4.1.22第二十二节 钩拢现象
-
1.6.4.1.23第二十三节 Ro n T及Ro nP现象
-
1.6.4.1.24第二十四节 抑制现象与总和现象
-
1.6.4.1.25第二十五节 连缀现象
-
1.6.4.1.26第二十六节 混沌现象
-
1.6.4.1.27第二十七节 穗尖现象与V<sub>3</sub>现象
-
1.6.4.1.28第二十八节 起搏器奔放现象
-
1.6.4.1.29第二十九节 起搏器滞后现象
-
1.6.4.1.30第三十节 电力衰竭现象
-
1.6.4.1.31第三十一节 灶性重激现象
-
1.6.4.1.32第三十二节 逆配对现象
-
1.6.4.1.33第三十三节 窦性心律震荡现象
-
1.6.4.1.34第三十四节 折返现象
-
1.6.4.1.35第三十五节 干扰现象
-
1.6.4.1.36第三十六节 心脏早复极现象
-
1.6.4.1.37第三十七节 干扰性脱节现象
-
1.6.4.1.38第三十八节 不均匀传导现象
-
1.6.4.1.39第三十九节 心尖现象
-
1.6.4.1.40第四十节 温醒现象与冷却现象
-
1.6.4.1.41第四十一节 电紧张性调频现象
-
1.6.4.1.42第四十二节 短-长-短周期现象
-
1.6.4.1.43第四十三节 电张调整性T波改变及T波记忆现象
-
1.6.4.2第四十四章 心电图部分相关概念
-
1.6.4.2.1第一节 F导联与Cabrera导联
-
1.6.4.2.2第二节 心电—机械分离
-
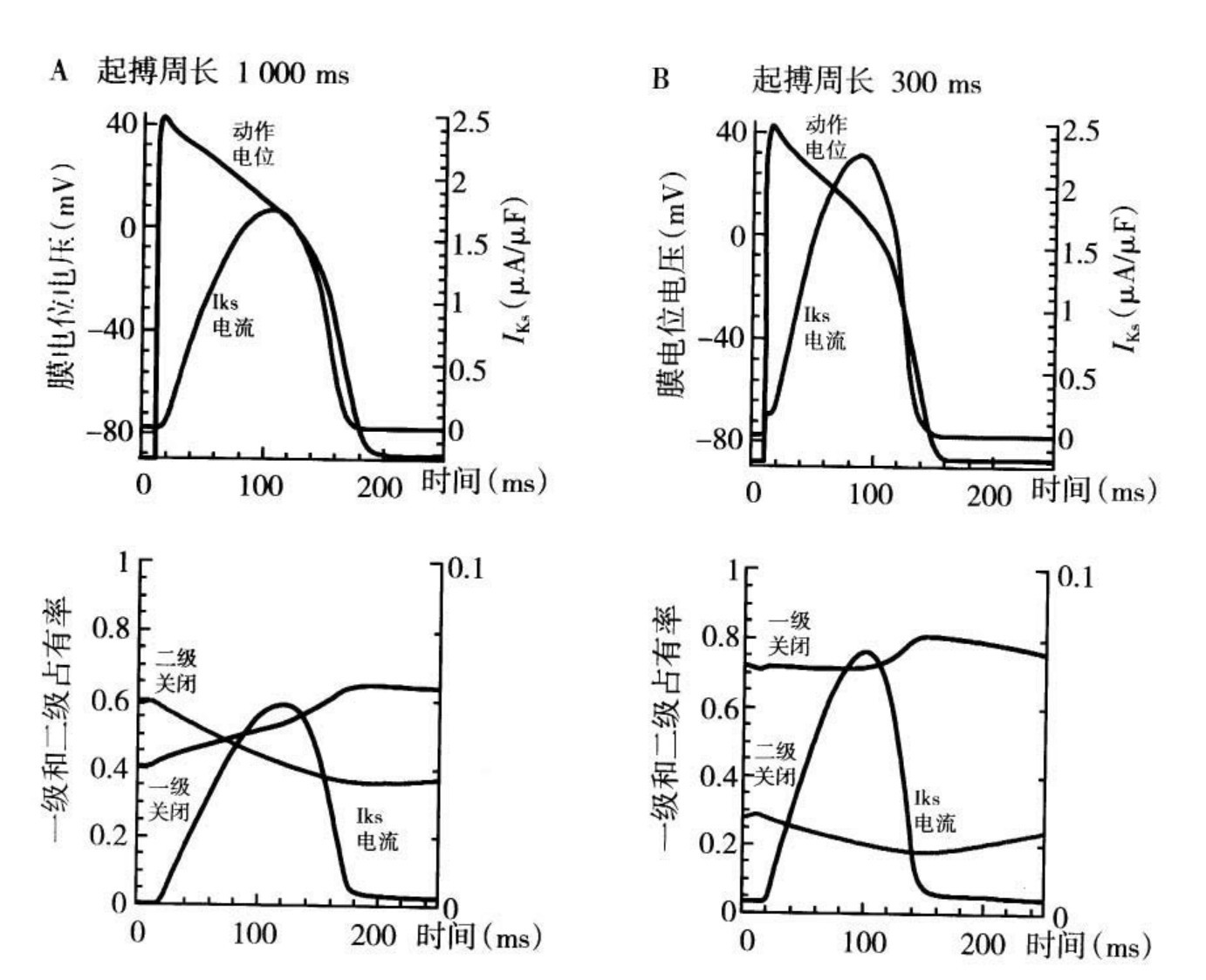
1.6.4.2.3第三节 膜反应性和膜反应曲线
-
1.6.4.2.4第四节 起搏细胞和非起搏细胞
-
1.6.4.2.5第五节 心肌M细胞
-
1.6.4.2.6第六节 代偿间歇与特殊的代偿间歇
-
1.6.4.2.7第七节 晚电位、后电位、激后电位和起搏器脉冲的后电位
-
1.6.4.2.8第八节 体表心脏等电位标测图
-
1.6.4.2.9第九节 电异步状态
-
1.6.4.2.10第十节 正相性逆行P波和房间隔阻滞型P波
-
1.6.4.2.11第十一节 逆行性P波、异位性P波和交感性P波
-
1.6.4.2.12第十二节 P波离散度
-
1.6.4.2.13第十三节 隐匿性交界性夺获
-
1.6.4.2.14第十四节 无人区心电轴
-
1.6.4.2.15第十五节 迷走神经心动过速
-
1.6.4.2.16第十六节 无休止心动过速
-
1.6.4.2.17第十七节 坏死Q波、等位Q波、位置Q波
-
1.6.4.2.18第十八节 期前收缩指数与易颤指数
-
1.6.4.2.19第十九节 Mac ruz指数、Mor r is指数与IPIV1
-
1.6.4.2.20第二十节 So k o l ow-Ly on指数与Co r ne l l指数
-
1.6.4.2.21第二十一节 融合波
-
1.6.4.2.22第二十二节 频率优势控制规律
-
1.6.4.2.23第二十三节 新“心脏规律”
-
1.6.4.2.24第二十四节 功能性心搏骤停
-
1.6.4.2.25第二十五节 心室重复反应
-
1.6.4.2.26第二十六节 触发活动与触发性心律失常
-
1.6.4.2.27第二十七节 再灌注损伤与再灌注心律失常
-
1.6.4.2.28第二十八节 并行心律
-
1.6.4.2.29第二十九心肌顿抑和心肌冬眠
-
1.6.4.2.30第三十节 临界心率与反常临界心律
-
1.6.4.2.31第三十一节 促心律失常和致心律失常
-
1.6.4.2.32第三十二节 P-R指数
-
1.6.4.2.33第三十三节 过早搏动后节律顺延
-
1.6.4.2.34第三十四节 QTc、QOT、QTa、QTr、JTc间期和QT/Ta比值
-
1.6.4.2.35第三十五节 V i/ VT比值
-
1.6.4.2.36第三十六节 心室复极时间变异性
-
1.6.4.2.37第三十七节 QT离散度
-
1.6.4.2.38第三十八节 心肌桥
-
1.6.4.2.39第三十九节 Wellens综合征
-
1.6.4.2.40第四十节 Andersen-Tawil综合征
-
1.6.4.2.41第四十一节 濒死心电图
-
1.6.4.2.42第四十二节 P-R间期过度延长综合征与房室同步不良
-
1.6.4.2.43第四十三节 心脏变时功能测定
-
1.6.4.2.44第四十四节 慢性心率增快
-
1.6.4.2.45第四十五节 获得性Brugada综合征
-
1.6.4.2.46第四十六节 心脏摇摆综合征
-
1.6.4.2.47第四十七节 转向灯原理
-
1.6.4.2.48第四十八节 钟摆样束支阻滞
-
1.6.4.2.49第四十九节 同源心室分离
-
1.6.4.2.50第五十节 Mas que r a d i ng束支阻滞
-
1.6.4.2.51第五十一节 心肌缺血阈
-
1.6.4.2.52第五十二节 缺血指纹
-
1.6.4.2.53第五十三节 缺血心电图的拇指法则
-
1.6.4.2.54第五十四节 酶学性心肌梗死
-
1.6.4.2.55第五十五节 Edeiken型ST段抬高
-
1.6.4.2.56第五十六节 Coumel定律
-
1.6.4.2.57第五十七节 Lenegre病与Lev病
-
1.6.4.2.58第五十八节 Bix法则
-
1.6.4.2.59第五十九节 草堆原理
-
1.6.4.2.60第六十节 室性期前收缩的分级与危险分层
-
1.6.4.2.61第六十一节 心房静止
-
1.6.4.2.62第六十二节 心动过速性心肌病
-
1.6.4.2.63第六十三节 预激性心动过速
-
1.6.4.2.64第六十四节 心室夺获
-
1.6.4.2.65第六十五节 心室复极储备
-
1.6.4.2.66第六十六节 T波峰末(Tp-Te)间期测定
-
1.6.4.2.67第六十七节 交感风暴
-
1.6.4.2.68第六十八节 心率减速力测定
-
1.6.4.2.69第六十九节 缝隙连接与传导
-
1.6.4.2.70第七十节 折返性期前收缩
-
1.6.4.2.71第七十一节 DeltaT50——一种新的方法评估心室复极变异
-
1.6.4.2.72第七十二节 震荡电位、边界电位和后电位
-
1.6.4.2.73第七十三节 无休止性心动过速
-
1.6.4.2.74第七十四节 微伏级T波电交替测定
-
1.6.4.2.75第七十五节 流产型心肌梗死
-
1.6.4.2.76第七十六节 胸导联心电图移行区指数
-
1.6.4.2.77第七十七节 心房碎裂电位
-
1.6.4.2.78第七十八节 心肌瘢痕心电图指数
-
1.6.4.2.79第七十九节 超速抑制
-
1.6.4.2.80第八十节 波峰碰撞
-
1.6.4.2.81第八十一节 正常心电图、大致正常心电图、正常变异心电图、可疑心电图及不正常心电图
-
1.6.4.2.82第八十二节 不恰当的期前收缩
-
1.6.4.2.83第八十三节 24导联心电图
-
1.6.4.2.84第八十四节 迷走性间歇性房室阻滞
-
1.6.4.2.85第八十五节 迷走神经介导性心房颤动
-
1.6.4.2.86第八十六节 双重心律
-
1.6.4.2.87第八十七节 其他有关概念
-
1.7下 卷
-
1.7.1三级目录
-
1.7.1.1第四十五章 心电图特殊波
-
1.7.1.1.1第一节 J波(osborn波)
-
1.7.1.1.2第二节 U波
-
1.7.1.1.3第三节 Epsilon波
-
1.7.1.1.4第四节 Delta波
-
1.7.1.1.5第五节 Brugada波
-
1.7.1.1.6第六节 Niagara瀑布样T波
-
1.7.1.1.7第七节 Lambda波
-
1.7.1.1.8第八节 非梗死性Q波
-
1.7.1.1.9第九节 Wolff波
-
1.7.1.1.10第十节 QRs碎裂波
-
1.7.1.1.11第十一节 CFAE电位(心房碎裂波)与肌袖房性心律失常
-
1.7.1.1.12第十二节 Pardee波
-
1.7.1.1.13第十三节 喜马拉雅P波
-
1.7.1.1.14第十四节 QRs波群丑征
-
1.7.1.1.15第十五节 圆顶尖角T波
-
1.7.1.1.16第十六节 圆顶尖峰型P'波
-
1.7.1.1.17第十七节 巨R波
-
1.7.1.1.18第十八节 窄高QRs波
-
1.7.1.1.19第十九节 同源心室分离波
-
1.7.1.1.20第二十节 交感肺型P波
-
1.7.1.1.21第二十一节 巨大T波
-
1.7.2第五篇 小儿心电图
-
1.7.2.1第四十六章 小儿心电图概论
-
1.7.2.1.1第一节 小儿心电图检查指征
-
1.7.2.1.2第二节 小儿心电图描记注意事项
-
1.7.2.1.3第三节 小儿心电图特征及其正常参考值
-
1.7.2.1.4第四节 小儿心电图分析方法
-
1.7.2.2第四十七章 心房扩大与心室肥大
-
1.7.2.2.1第一节 心房扩大
-
1.7.2.2.2第二节 心室肥大
-
1.7.2.3第四十八章 心包炎、心肌炎与心肌病
-
1.7.2.3.1第一节 心包炎
-
1.7.2.3.2第二节 心肌炎与心肌病
-
1.7.2.4第四十九章 先天性心脏病
-
1.7.2.5第五十章 药物作用及电解质紊乱对心电图的影响
-
1.7.2.5.1第一节 洋地黄类引起的心律失常
-
1.7.2.5.2第二节 其他药物与心律失常
-
1.7.2.5.3第三节 电解质紊乱对心电图的影响
-
1.7.2.6第五十一章 小儿心律失常
-
1.7.2.6.1第一节 概 述
-
1.7.2.6.2第二节 窦性心律失常
-
1.7.2.6.3第三节 期前收缩
-
1.7.2.6.4第四节 阵发性心动过速
-
1.7.2.6.5第五节 扑动和颤动
-
1.7.2.6.6第六节 心脏传导阻滞
-
1.7.2.6.7第七节 预激综合征
-
1.7.2.6.8第八节 全身性疾病引起的心律失常
-
1.7.2.6.9第九节 其他原因引起的心律失常
-
1.7.2.7第五十二章 小儿心电向量图
-
1.7.2.8第五十三章 胎儿心电图
-
1.7.2.8.1第一节 胎儿心电图描记方法
-
1.7.2.8.2第二节 正常胎儿心电图
-
1.7.2.8.3第三节 异常胎儿心电图
-
1.7.3第六篇 心电图鉴别诊断及复杂、疑难心电图的阅读与分析
-
1.7.3.1第五十四章 心电图各波段异常的鉴别诊断
-
1.7.3.1.1第一节 P波异常的鉴别诊断
-
1.7.3.1.2第二节 P-R间期异常
-
1.7.3.1.3第三节 Q波异常
-
1.7.3.1.4第四节 QRs波群异常
-
1.7.3.1.5第五节 ST段异常
-
1.7.3.1.6第六节 T波异常
-
1.7.3.1.7第七节 Q-T间期异常
-
1.7.3.1.8第八节 U波异常的鉴别诊断
-
1.7.3.2第五十五章 房室肥大的鉴别诊断
-
1.7.3.2.1第一节 心房肥大的鉴别诊断
-
1.7.3.2.2第二节 心室肥大的鉴别诊断
-
1.7.3.2.3第三节 双侧心室肥大的鉴别诊断
-
1.7.3.3第五十六章 非梗死Q波的鉴别诊断
-
1.7.3.3.1第一节 心脏病变引起的Q波
-
1.7.3.3.2第二节 非心脏原因引起的Q波
-
1.7.3.4第五十七章 心律失常的鉴别诊断
-
1.7.3.4.1第一节 P波形态多变的鉴别
-
1.7.3.4.2第二节 提早出现的心搏
-
1.7.3.4.3第三节 延迟出现的心搏
-
1.7.3.4.4第四节 心率缓慢而规则
-
1.7.3.4.5第五节 心率快而不规则
-
1.7.3.4.6第六节 心室律不整
-
1.7.3.4.7第七节 房性二联律
-
1.7.3.4.8第八节 室性二联律
-
1.7.3.4.9第九节 P波与QRs波群完全无关
-
1.7.3.5第五十八章 现代诊疗技术在心电图鉴别诊断中的应用
-
1.7.3.5.1第一节 动态心电图
-
1.7.3.5.2第二节 食管导联心电图
-
1.7.3.5.3第三节 食管心房调搏术
-
1.7.3.5.4第四节 心脏固有频率测定
-
1.7.3.5.5第五节 窦房结心电图
-
1.7.3.5.6第六节 希氏束电图
-
1.7.3.5.7第七节 体表心脏等电位标测图
-
1.7.3.5.8第八节 心腔内心电图
-
1.7.3.5.9第九节 心室晚电位
-
1.7.3.6第五十九章 心电图试验在心电图鉴别诊断中的应用
-
1.7.3.6.1第一节 阿托品试验
-
1.7.3.6.2第二节 异丙基肾上腺素试验
-
1.7.3.6.3第三节 按压颈动脉窦试验
-
1.7.3.6.4第四节 心得安试验
-
1.7.3.6.5第五节 心电图运动负荷试验
-
1.7.3.7第六十章 复杂、疑难心电图的阅读与分析
-
1.7.3.7.1第一节 复杂、疑难心电图分析方法
-
1.7.3.7.2第二节 复杂、疑难心电图梯形图诊断技术及应用
-
1.7.3.7.3第三节 宽QRs波群心动过速的诊断与鉴别诊断
-
1.7.3.7.4第四节 快速识别宽QRs心动过速为室性心动过速简易五步法
-
1.7.3.7.5第五节 心电散点图呈现的房室结功能不应期及对宽QRS波的鉴别
-
1.7.3.7.6第六节 窄QRS波群心动过速的诊断与鉴别诊断
-
1.7.3.7.7第七节 房室结及折返径路内双径路、多径路传导的心电图分析
-
1.7.3.7.8第八节 特殊类型的室性期前收缩
-
1.7.3.7.9第九节 心电图二联律伴发特殊心电现象的分析
-
1.7.3.7.10第十节 并行心律伴发特殊心电现象的分析
-
1.7.3.7.11第十一节 心房颤动心电图分析的难点解析
-
1.7.3.7.12第十二节 心电图长间歇伴心电特殊现象的解析
-
1.7.3.7.13第十三节 房室交接性逸搏伴多种心电现象的解析
-
1.7.3.7.14第十四节 双侧束支主干部阻滞心电图分析方法
-
1.7.3.7.15第十五节 复杂窦房、房室传导阻滞心电图分析方法
-
1.7.3.7.16第十六节 预激综合征中复杂、疑难心电图的分析方法与技巧
-
1.7.3.7.17第十七节 高钾血症复杂心电图分析
-
1.7.3.7.18第十八节 急性心肌梗死不典型心电图分析方法与判读
-
1.7.3.7.19第十九节 复杂心电现象心电图的分析方法及技巧
-
1.7.3.7.20第二十节 心律失常的诊断误区
-
1.7.3.7.21第二十一节 动态心电图在复杂疑难心电图分析中的应用
-
1.7.4第七篇 起搏、动态运动、电生理心电图及派生心电图
-
1.7.4.1第六十一章 起搏心电图
-
1.7.4.1.1第一节 心脏起搏基础
-
1.7.4.1.2第二节 人工心脏起搏器植入技术
-
1.7.4.1.3第三节 起搏心电图分析技术及注意事项
-
1.7.4.1.4第四节 起搏心电图图形
-
1.7.4.1.5第五节 单腔起搏器心电图
-
1.7.4.1.6第六节 双腔起搏器心电图
-
1.7.4.1.7第七节 频率适应性起搏器心电图
-
1.7.4.1.8第八节 生理性起搏心电图
-
1.7.4.1.9第九节 起搏故障心电图
-
1.7.4.1.10第十节 与起搏器有关的心律失常
-
1.7.4.1.11第十一节 人工心脏起搏器的选用原则及进展
-
1.7.4.1.12第十二节 起搏器的程控及遥测简介
-
1.7.4.1.13第十三节 起搏器与临床
-
1.7.4.2第六十二章 动态心电图
-
1.7.4.2.1第一节 动态心电图的产生和发展
-
1.7.4.2.2第二节 动态心电图检查的临床应用和适应证选择
-
1.7.4.2.3第三节 动态心电图系统的设备与基本技术指标
-
1.7.4.2.4第四节 如何防止动态心电图的干扰与伪差
-
1.7.4.2.5第五节 动态心电图的编辑
-
1.7.4.2.6第六节 动态心电图报告书写
-
1.7.4.2.7第七节 动态心电图新技术及临床应用
-
1.7.4.2.8第八节 无症状性心肌缺血的动态心电图诊断
-
1.7.4.2.9第九节 动态心电图诊断中常见的一些问题
-
1.7.4.2.10第十节 植入式Holter
-
1.7.4.3第六十三章 心脏负荷试验
-
1.7.4.3.1第一节 运动负荷试验
-
1.7.4.3.2第二节 心脏药物负荷试验和其他负荷试验
-
1.7.4.3.3第三节 儿童负荷试验
-
1.7.4.4第六十四章 电生理检查及电生理心电图
-
1.7.4.4.1第一节 无创电生理检查及电生理心电图
-
1.7.4.4.2第二节 有创心内电生理检查及心腔内心电图
-
1.7.4.4.3第三节 窦房结电图
-
1.7.4.4.4第四节 希氏束电图
-
1.7.4.4.5第五节 单相动作电位
-
1.7.4.4.6第六节 心脏刺激术
-
1.7.4.4.7第七节 心脏介入诊断及治疗中的心电图
-
1.7.4.5第六十五章 心电监测与远程心电监测技术
-
1.7.4.5.1第一节 各种心电监测技术
-
1.7.4.5.2第二节 心电信息管理网络及技术
-
1.7.4.6第六十六章 食管导联心电图和食管心脏电生理检查
-
1.7.4.6.1第一节 食管导联心电图
-
1.7.4.6.2第二节 食管心脏电生理检查技术
-
1.7.4.6.3第三节 心脏不应期测定
-
1.7.4.6.4第四节 窦房结及房室交接区功能检测
-
1.7.4.6.5第五节 房室结双径路及多径路检测
-
1.7.4.6.6第六节 预激综合征电生理检查
-
1.7.4.6.7第七节 阵发性折返性室上性心动过速
-
1.7.4.6.8第八节 常见的电生理现象
-
1.7.4.6.9第九节 食管心脏电生理检查诊断心律失常的优点与不足
-
1.7.4.7第六十七章 经食管心脏起搏及电复律
-
1.7.4.7.1第一节 经食管心脏负荷试验
-
1.7.4.7.2第二节 经食管心室起搏
-
1.7.4.7.3第三节 经食管心脏电复律
-
1.7.4.8第六十八章 派生心电图
-
1.7.4.8.1第一节 正交导联心电图
-
1.7.4.8.2第二节 立体心电图
-
1.7.4.8.3第三节 心率变异性
-
1.7.4.8.4第四节 高频心电图临床应用及研究
-
1.7.4.8.5第五节 信号平均心电图与心室晚电位的临床应用
-
1.7.4.8.6第六节 频谱心电图
-
1.7.4.8.7第七节 压力感受器敏感性测定及应用
-
1.7.4.9第六十九章 心磁图
-
1.7.4.9.1第一节 仪器与检测方法
-
1.7.4.9.2第二节 心磁图的特点
-
1.7.4.9.3第三节 正常心磁图
-
1.7.4.9.4第四节 心磁图的临床应用
-
1.7.4.9.5第五节 评价与展望
-
1.7.4.10第七十章 心电散点图
-
1.7.4.10.1第一节 概述
-
1.7.4.10.2第二节 非线性混沌理论
-
1.7.4.10.3第三节 混沌与心电学的结合
-
1.7.4.10.4第四节 心电散点图的发展
-
1.7.4.10.5第五节 心电散点图基础
-
1.7.4.10.6第六节 窦性心律的散点图
-
1.7.4.10.7第七节 心律失常的心电散点图
-
1.7.4.10.8第八节 疑难动态心电图的散点图分析
-
1.7.4.10.9第九节 心电散点图软件
-
1.7.4.11第七十一章 心电治疗技术与心电图
-
1.7.4.11.1第一节 心脏起搏术
-
1.7.4.11.2第二节 射频消融术
-
1.7.4.11.3第三节 电除颤与电转复术
-
1.7.4.11.4第四节 24小时动态血压监测的临床应用
-
1.7.5第八篇 心电图与临床
-
1.7.5.1第七十二章 心电图临床诊断中的几个问题
-
1.7.5.1.1第一节 概述
-
1.7.5.1.2第二节 心电图临床应用适应证选择
-
1.7.5.1.3第三节 心电图报告的出具及阅读
-
1.7.5.1.4第四节 临床心电图数据库的建立
-
1.7.5.1.5第五节 心电图诊断名词、术语规范化建议
-
1.7.5.1.6第六节 心电图正常值范围概念更新
-
1.7.5.1.7第七节 计算机心电图自动诊断的认识
-
1.7.5.1.8第八节 注意心电图的个体差异
-
1.7.5.1.9第九节 心电图诊断失误的原因分析及对策
-
1.7.5.2第七十三章 心律失常的心电图与临床
-
1.7.5.2.1第一节 心电图判断良恶性室性心律失常的价值
-
1.7.5.2.2第二节 病理性与功能性室性期前收缩的鉴别诊断和处理
-
1.7.5.2.3第三节 恶性心律失常的心电图与临床
-
1.7.5.2.4第四节 无创心电技术预测恶性心律失常及心脏性猝死
-
1.7.5.2.5第五节 心室电风暴
-
1.7.5.2.6第六节 自主神经与心律失常
-
1.7.5.2.7第七节 房室交界区和束支不应期在体表心电图的测定
-
1.7.5.2.8第八节 不需要治疗的心律失常
-
1.7.5.2.9第九节 抗心律失常药物的致心律失常作用
-
1.7.5.3第七十四章 心肌缺血、心肌梗死的心电图与临床
-
1.7.5.3.1第一节 心电图预测急性心肌梗死相关血管的价值
-
1.7.5.3.2第二节 临床心肌缺血与心电图
-
1.7.5.3.3第三节 巨R形ST段抬高的特性及其临床意义
-
1.7.5.3.4第四节 急性心肌梗死猝死预警心电图
-
1.7.5.4第七十五章 心脏移植与心电图
-
1.7.5.5第七十六章 ST-T改变的临床问题
-
1.7.5.6第七十七起搏器与临床
-
1.7.5.6.1第一节 植入起搏器的适应证
-
1.7.5.6.2第二节 起搏器安装技术的常见并发症及其处理
-
1.7.6参考文献
1
心电图学