-
1 理论教学
-
2 实践演练

![]()
掌握了解化学渗透学说、电子传递链组成。
![]()
一、氧化磷酸化的概念及类型
伴随着放能的氧化作用而进行的磷酸化称为氧化磷酸化作用( oxidativephosphorylation)
(一)底物水平磷酸化
代谢底物在分解代谢中,有少数脱氢或脱水反应,引起代谢物分子内部能量重新分布,
形成某些高能中间代谢物,这些高能中间代谢物中的高能键,可以通过酶促磷酸基团转移
反应,直接使ADP 磷酸化生成ATP,这种作用称为底物水平磷酸化(substrate-level
phosphorylation)。
(二)电子传递链磷酸化
电子传递链磷酸化是指利用代谢物脱下的2H(NADH+H+或FADH2)经过电子传递链(呼吸链)传递到分子氧形成水的过程中所释放出的能量,使ADP 磷酸化生成ATP 的作用。简言之,H 经呼吸链氧化与ADP 磷酸化为ATP反应的偶联,就是电子传递链磷酸化(electron transport chainphosphorylation),又称氧化磷酸化。
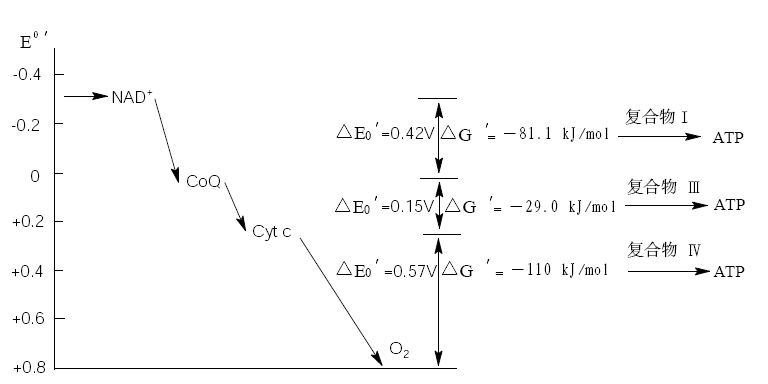
三、氧化磷酸化的偶联部位和P/O 比
呼吸链中的氧化是放能过程(exergoniccprocess),ADP 的磷酸化是吸能过程(endergonic process),两者只有偶联起来才能形成ATP。电子在呼吸链中按顺序逐步传递放自由能,其中释放自由能较多足以用来形成ATP的电子传递部位称为偶联部位(couplingsite)。实验证明,呼吸链的四个复合物中,复合物Ⅰ、Ⅲ、Ⅳ是偶联部位,复合物Ⅱ不是偶联部位。NADH 经呼吸链氧化要通过复合物Ⅰ、Ⅲ和Ⅳ三个偶联部位,所以形成3 个ATP;FADH2(来自于琥珀酸脱氢)经呼吸链氧化只通过复合物Ⅲ和Ⅳ二个偶联部位,只形成2 个ATP

四、氧化磷酸化的作用机理
化学渗透偶联学说
化学渗透偶联学说(chemiosmotic-couplinghypothesis)是由英国生物化学工作者P.
Mitchell 于1961 年最先提出的,并已得到较多支持与公认,因此P. Mitchell 于1978 年获得诺贝尔化学奖。其主要论点是认为呼吸链存在于线粒体内膜之上,当氧化进行时,呼吸
链起质子泵作用,质子被泵出线粒体内膜的外侧,造成了膜内外两侧间跨膜的质子电化学
梯度(即质子浓度梯度和电位梯度,合称为质子移动力),这种跨膜梯度具有的势能被膜
上ATP 合成酶所利用,使ADP 与Pi 合成ATP。其要点分述如下:
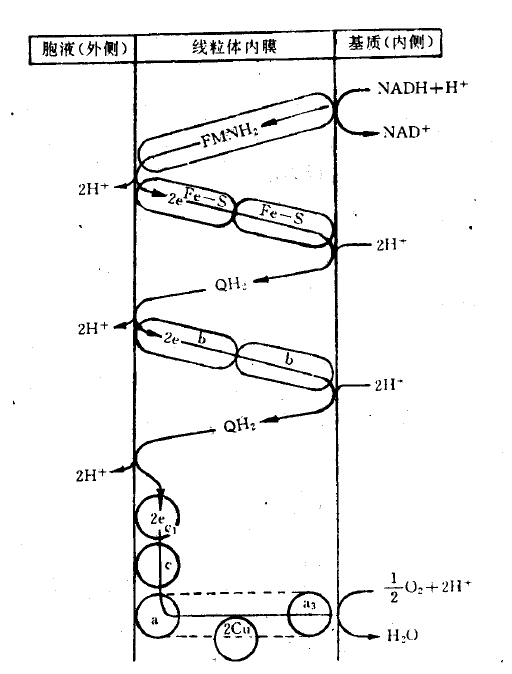
1. 呼吸链中递氢体和电子传递体在线粒体内膜中是间隔交替排列的,并且都有特定的
位置,催化反应是定向的。
2. 递氢体有氢泵的作用,当递氢体从线粒体内膜内侧接受从NADH+H+ 传来的氢后,
可将其中的电子(2e -)传给位于其后的电子传递体,而将两个H+ 质子从内膜泵出到膜外
侧,在电子传递过程中,每传递一对电子就泵出6 个H+ 质子(见图6-10)。
3. 内膜对H+ 不能自由通过,泵出膜的外侧H+ 不能自由返回膜内侧,因而使线粒体
内膜外侧的H+ 质子浓度高于内侧,造成H+ 质子浓度的跨膜梯度,此H+ 浓度差使外侧的
pH 较内侧的pH 低1.0 单位左右,并使原有的外正内负的跨膜电位增高,此电位差中就包
含着电子传递过程中所释放的能量,好象电池两极的离子浓度差造成电位差含有电能一
样。这种H+ 质子梯度和电位梯度就是质子返回内膜的一种动力。
4. 利用线粒体内膜上的ATP 合成酶的特点,将膜外侧的2H+ 转化成膜内侧的2H+,
与氧生成水,即H+ 通过ATP 酶的特殊途径,返回到基质,使质子发生逆向回流。由于
H+ 浓度梯度所释放的自由能,偶联ADP 与无机磷酸合成ATP,质子的电化学梯度也随之
消失
化学渗透学说是较为公认的对氧化磷酸化作用机理有一定说服力的学说。但远不够成
熟,其递氢体和电子传递体的顺序以及三个磷酸化的偶联部位与前述的呼吸链不完全一
致,故有待于进一步研究。
五、氧化磷酸化的解偶联剂和抑制剂
(一)解偶联剂
某些化合物能够消除跨膜的质子浓度梯度或电位梯度,使ATP 不能合成,这种既不直
接作用于电子传递体也不直接作用于ATP 合酶复合体,只解除电子传递与ADP磷酸化偶
联的作用称为解偶联作用,其实质是光有氧化过程(电子照样传递)而没有磷酸化作用。
这类化合物被称为解偶联剂(uncouplers)。
人工的或天然的解偶联剂主要有下列三种类型:
1.化学解偶联剂
2,4-二硝基苯酚(2,4-dinitrophenol,DNP)是最早发现的也是最典型的化学解偶联剂
(chemicaluncoupling agent),其特点是呈弱酸性和脂溶性,在不同的pH 环境中可释放
H+和结合H+:在pH 7.0 的环境中,DNP 以解离形式存在,不能透过线粒体膜;在酸性环
境中,解离的DNP 质子化,变为脂溶性的非解离形式,能透过膜的磷脂双分子层,同时
把一个质子从膜外侧带入到膜内侧,因而破坏电子传递形成的跨膜质子电化学梯度,起着
消除质子浓度梯度的作用,抑制ATP的形成。
2. 离子载体
有一类脂溶性物质能与某些阳离子结合,插入线粒体内膜脂双层,作为阳离子的载体,
使这些阳离子能穿过线粒体内膜。它和解偶联剂的区别在于它是作为H+离子以外的其它
一价阳离子的载体。例如,由链霉菌产生的抗菌素缬氨霉素(valinomycin)能与K+离子
配位结合形成脂溶性复合物,穿过线粒体内膜,从而将膜外的K+转运到膜内。又如,短
杆菌肽(gramicidin)可使K+、Na+及其它一些一价阳离子穿过内膜。这类离子载体
(ionophore)由于增加了线粒体内膜对一价阳离子的通透性,消除跨膜的电位梯度,消耗
了电子传递过程中产生的自由能,从而破坏了ADP 的磷酸化过程。
3.解偶联蛋白
解偶联蛋白(uncouplingprotein)是存在于某些生物细胞线粒体内膜上的蛋白质,为
天然的解偶联剂。如动物的褐色脂肪组织的线粒体内膜上分布有解偶联蛋白,这种蛋白构
成质子通道,让膜外质子经其通道返回膜内而消除跨膜的质子浓度梯度,抑制ATP 合成而
产生热量以增加体温。
六、线粒体的穿梭系统
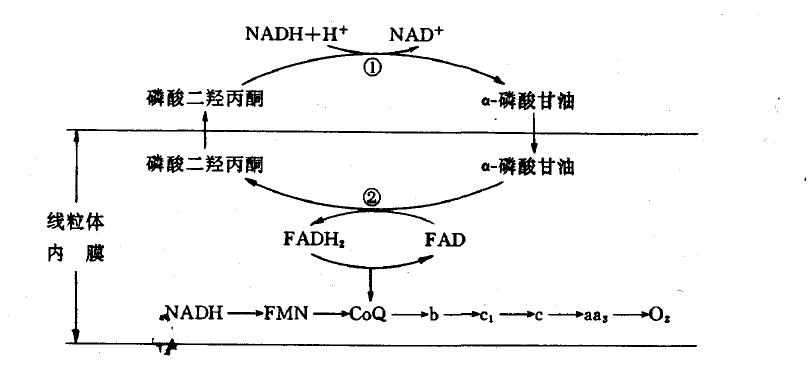
(一)磷酸甘油穿梭系统
胞液中的NADH 在两种不同的α-磷酸甘油脱氢酶的催化下,以α-磷酸甘油为载体穿
梭往返于胞液和线粒体之间,间接转变为线粒体内膜上的FADH2 而进入呼吸链,这种过
程称为磷酸甘油穿梭(glycerolphosphate shuttle)。
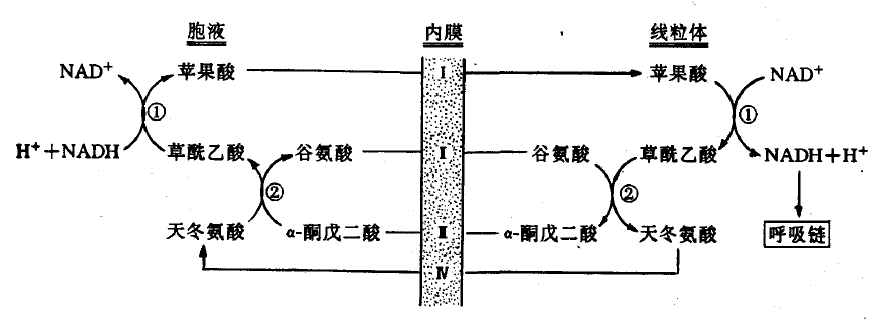
(二)苹果酸-天冬氨酸穿梭系统
苹果酸-天冬氨酸穿梭系统(malate-aspartate shuttle)需要两种谷-草转氨酶、两种苹果
酸脱氢酶和一系列专一的透性酶共同作用
七、能荷
(一)能荷的概念
能荷的大小可
以说明生物体中ATP、ADP、AMP 系统的能量状态。能荷(energycharge)的定义可用下
式表示:
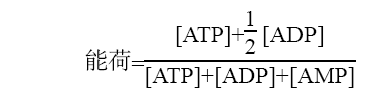
![]()
线粒体呼吸链复合物II活性比色法定量检测试剂盒
线粒体呼吸链复合物II,通常称为琥珀酸-辅酶Q还原酶或琥珀酸脱氢酶(Succinate-CoenzymeQReductase;Succinate Dehydrogenase),是线粒体电子传递链与三羧酸循环链接的载体:含有四个亚单位,包括共价结合的辅基黄素腺嘌呤二核苷酸(flavin adenine dinucleotide;FAD)和三个铁硫中心(Fe-S clusters),以及细胞色素b亚单位,其最特征性的酶活性是丙二酸钠敏感的琥珀酸-辅酶Q还原酶。复合物II催化琥珀酸(succinate)被氧化为富马酸(fumarate),线粒体内电子由供体FAD传递到内膜上辅酶Q受体(泛醌;ubiquinone)的能量转移反应,进行呼吸链传递。该酶异常会导致嗜铬细胞瘤(paraganglioma)、肾上腺嗜铬细胞瘤(pheochromocytoma)和Leigh综合征。基于琥珀酸底物,通过琥珀酸-辅酶Q还原酶的催化,氧化为富马酸,同时氧化型二氯酚靛酚(dichlorophenal-indophenol;DCPIP)转化为还原型二氯酚靛酚(dichlorophenal-indophenol;DCPIPH2),在分光光度仪下产生吸光峰值的变化(600nm波长),由此定量测定琥珀酸-辅酶Q还原酶的特异活性。其适合于各种纯化线粒体样品(动物、人体、酵母)以及细胞或组织裂解悬液样品的琥珀酸-辅酶Q还原酶的特异性活性检测。可用于衰老、能量代谢、蛋白组学、病理生理学、神经病变等研究。
![]()


